3-2醛
选修5 3-2醛课件1(2个)
汞盐
O
CH3-C-H O
2)乙烯氧化法 ) 2CH2 钯盐
CH2 + O2加压、加热 2CH3-C-H
布置作业
P.59 5
++OH-+2H AgOH+2 NH3H2O=[Ag(NH3)2]亮的银 2O
出现漂 Ag++NH3H2O→AgOH +NH4+
镜 ②水浴加热生成银镜 :在配好的上述银
氨溶液中滴入三滴乙醛溶液, 氨溶液中滴入三滴乙醛溶液,然后把试管 放在热水浴中静置。 放在热水浴中静置。
乙醛能被弱氧化剂氧化
CH3CHO+ 2Ag(NH3)2OH CH3COONH4 + (银氨溶液) + 氧化剂 +2Ag↓+3NH3+H2O 还原剂
(1)试管内壁必须洁净; )试管内壁必须洁净; (2)必须水浴; )必须水浴; (3)加热时不可振荡和摇动试管; )加热时不可振荡和摇动试管; (4)须用新配制的银氨溶液; )须用新配制的银氨溶液; (5)乙醛用量不可太多; )乙醛用量不可太多; 浸泡, (6)实验后,银镜用 )实验后,银镜用HNO3浸泡,再用水洗
2、乙醛的氧化:在上述蓝色浊液中加 、乙醛的氧化: 砖红色 还原剂 氧化剂 乙醛溶液, 入0.5ml乙醛溶液, 乙醛溶液 加热至沸腾。 加热至沸腾 沸腾。 乙醛能否被强氧化剂氧化?? 乙醛能否被强氧化剂氧化
Cu CH3COOH+ 2O↓ +2H2O
常用的氧化剂: 常用的氧化剂: 银氨溶液、新制的Cu( 银氨溶液、新制的 (OH)2、O2、 ) 酸性KMnO4溶液、酸性K2Cr2O7溶液等。 酸性 溶液、酸性 溶液等。 银镜反应注意事项
2) 加成反应 )
3-2《醛》课件(人教版化学选修5)

碳原子价 态改变
HC
乙醛的氧化反应: H
HO
CH
极性键
H C CH
O
H
⑴乙醛的氧化反应
①燃烧
在点燃的条件下,乙醛能在空气或氧气中燃
烧。乙醛完全燃烧的化学方程式为: 2CH3CHO+5O2 点燃 4CO2+4H2O
②催化氧化 2CH3CHO+O2 催化剂 2CH3COOH
催化氧 H O
化机理
H C CH
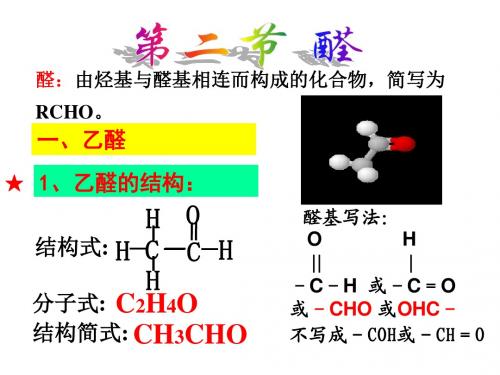
⒉乙醛的分子结构:
分子式: C2H4O
HO
结构式:
HC CH
结构简式: CH3CHO H
官能团: -CHO 不能写成-COH
图3-12 乙醛分子的比例模型
图3-11 乙醛的核磁共振氢谱
通过乙醛的核磁共振氢谱,你能获取什么信 息?请你指出两个吸收峰的归属。
醛基上的氢
甲基上的氢
吸收峰较强的为甲基上的氢原子,较弱的为 醛基上的氢原子,二者面积比约为3:1
由苯二氯甲烷水解制得。它用途广泛,可用于生产苯甲
醇、苯胺、苯甲酮和杀虫剂等产品,也是苯甲醛系香料
最基本的原料,是某些合成医药产品、塑料添加剂的最
基本原料。由于苯甲醛具有独特的甜味、芳香味和杏仁
气味,因此它也是合成香精香料的一种重要中间体,苯
甲醛也是合成诸如玫瑰香和茉莉香等香料的第一步,这
些香料广泛用于各种香皂和香水中。
根据乙醛的结构——预测乙醛的性质
H HC
O 不饱和
CH
H
烯烃和醛都有不饱和双键,能发生加成反应, 这是两者的共性。但是,C=O双键和C=C双键结构 不同,产生的加成反应也不一样。因此,能跟烯 烃起加成反应的试剂(如溴),一般不跟醛发生 加成反应。
甲醛释放标准

美国木制品甲醛释放量新限令开始正式生效2011-01-05 00:00:00美国去年颁布的《复合木制品甲醛标准法案》已于今年1月3日正式生效,并在今后两年内分步实施更高的标准。
该法案对在美国供应、销售或制造的硬木胶合板、中密度纤维板及刨花板等复合木制品制定了统一的甲醛释放标准,显著高于目前我国及世界各国的通行标准,号称目前世界上最严厉的甲醛释放标准。
具体实施时间表如下:硬木胶合板单芯板(HWPW-VC):甲醛释放量≤0.05ppm。
硬木胶合板复合芯板(HWPW-CC):甲醛释放量≤0.08ppm,2011年1月3日开始生效,直至2012年6月30日;2012年7月1日起,甲醛释放量≤0.05ppm。
中密度纤维板(MDF):甲醛释放量≤0.21ppm,2011年1月3日开始生效,直至2011年6月30日;2011年7月1日起,甲醛释放量≤0.11ppm。
薄型中密度纤维板(Thin-MDF):甲醛释放量≤0.21ppm,2011年1月3日开始生效,直至2012年6月30日;2012年7月1日起,甲醛释放量≤0.13ppm。
刨花板(PB),甲醛释放量≤0.18ppm,2011年1月3日开始生效,直至2011年6 月30日;2011年7月1日起,甲醛释放量≤0.09ppm。
美国颁布的木制品甲醛释放量新限令,将对我国木制品出口造成较大负面影响,杭州检验检疫局2010年的数据显示,杭州局辖区所有出口木制品中有21%输往美国,而目前我国再生板材除少数已通过美国加州CARB认证的产品外,大多数产品都不能满足美国新法规的要求。
因此相关出口生产企业应科学调整出口产品种类和生产计划,进一步改进生产工艺,建立并完善质量管理体系和出口木制品有毒有害物质自检自控体系,尽量使用已经通过CARB认证企业的原辅料,确保原辅料质量安全,同时密切关注其他国家可能采取的跟进措施,积极拓展国内外营销渠道,开发新的国际市场。
美国加利福尼亚州:降低复合木制品甲醛释放标准2008年4月18日美国加利福尼亚州行政法规办公室通过了由空气资源委员会提议制定的《有毒空气控制测量法规》(ATCM),旨在减少复合木制品甲醛释放。
选修5 3-2 醛

新 制 氢 氧 化 铜
3.化学性质 (1)氧化反应 ②与新制Cu(OH)2的反应 弱氧化剂 Cu(OH)2 Cu 2+ + 2OH-
CH3CHO +2Cu(OH)2
蓝色 CH3COOH+ NaOH
CH3COOH+Cu2O↓+2H2O 红色
CH3COONa + H2O
CH3CHO + 2Cu(OH)2 + NaOH △
(4)CH2=CH—CH2OH
在日常生活中我们都会有这样的 疑问, 为什么有的人喝酒“千杯万 杯都不醉”,而有的人喝一点酒后就 面红耳赤,情绪激动甚至酩酊大醉? 酒量的大小到底与什么有关呢?
人的酒量大小,与酒精在人体内的代谢
产物和过程有很大关系。乙醇进入人体内,首 先在乙醇脱氢酶的作用下氧化为乙醛,然后又 在乙醛脱氢酶的作用下将乙醛氧化为乙酸,并 进一步转化为CO2和H2O。如果人体内这两种 脱氢酶的含量都很大的话,酒精的代谢速度就 很快。但如果人体内这两种脱氢酶的 原来如 含量不够大, 例如缺少乙醛脱氢酶, 此啊! 饮酒后就会引起体内乙醛积累,导 致血管扩张而脸红。
3、醛的分类:
饱和醛、不饱和醛 脂肪醛
R
一元醛
醛
芳香醛
二元醛 多元醛
4.饱和一元醛通式:CnH2n+1CHO或CnH2nO 5.最简单的醛:甲醛(HCHO)
甲醛俗名蚁醛,是一种无色、有强烈刺激 性气味的气体,易溶于水,质量分数为35 %~40%的水溶液叫做福尔马林,具有杀菌、 防腐性能等。
为求延长保质期 不良奸 商竟然给冰鲜鱼浸甲醛 保鲜
1.完成课本58页的“学与问”,59 页的课后习题。 2.完成世纪金榜本节课对应的基础 自主演练。
3-2醛

10%NaOH
氢氧化铜的制备:
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4
乙醛的氧化:
CH3CHO + 2Cu(OH)2 + NaOH CH3COONa + Cu2O↓ + 3H2O
1、氧化反应 (3)催化氧化
乙醛在一定温度和催化剂存在的条件 下,也能被空气中的氧气氧化成乙酸: (工业制乙酸)
O 2CH3—C—H + O2
催化剂 △
2CH3COOH
乙醛能否使下列几种溶液褪色? 1、溴水
2、酸性KMnO4溶液
3、酸性K2Cr2O7溶液 都能,乙醛被这些强氧化剂氧化。
3、化学性质 2、加成反应 O H3C-C-H +H2
5. 常见的醛: 甲醛(蚁醛): HCHO
无色有刺激性气味的气体,易溶于水。 35%~40%的甲醛水溶液叫做福尔马林,具有 杀菌、防腐性能。
自然界的许多植物中含有醛,其中许多具有特 殊的香味,可作为植物香料使用。如桂皮含肉 桂醛,杏仁含苯甲醛。 CH2=CH-CHO CHO
肉桂醛
苯甲醛
二、乙醛 1、分子结构:
A、CH3CH2OH
B、HO-CH2-CH-CH3 C、HOCH2CH2CH2OH D、CH3-CH-∣ CH-CH -CH3 ∣ OH OH
∣
OH
讨论:哪些有机物通过化学反应使溴水褪色?
①、含C=C或C≡C键的有机物; ②、酚、醛 讨论:哪些有机物可使酸性KMnO4溶液褪色? ①、含C=C或C≡C键的有机物
3-2醛

2CH3CHO+O2 △ 2CH3COOH
小结: 乙醇
氧化 乙醛 还原
氧化
乙酸
氧化反应
①催化氧化
2CH3-C-H + O2 O= O=
催化剂 △
2CH3-C-OH 乙酸
b.
燃烧 2CH3CHO+5O2
点燃 4CO2+4H2O
c. 被弱氧化剂氧化
Ⅰ 银镜反应
1、 配置银氨溶液:取一洁净试管,加入 2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水, 至生成的沉淀恰好溶解。
2、水浴加热形成银镜:在配好的上述银氨 溶液中滴入三滴乙醛溶液,然后把试管 注意:水浴加热时不可振荡和摇动试管 放在热水浴中静置。 CH3CHO+2 Ag(NH3)2OH 水浴 还原剂 氧化剂 CH3COONH4 +2Ag +3NH3+H2O 碱性环境下,乙醛被氧化成乙酸后又与 反应生成乙酸铵 NH3
注意:银镜反应要求在碱性环境下进行,
但氨水不应过量太多
• 在洁净的试管里加入1 mL2%的AgNO3溶液,然后一边摇动试 Ag++NH3· 2O=AgOH ↓+ NH4+ H 管,一边逐滴滴入2%的稀氨水,至最初产生的沉淀恰好溶解 AgOH+2 NH3· 2O=[Ag(NH3)2]++OH-+2H2O H 为止(这时得到的溶液叫做银氨溶液)。再滴入3滴乙醛,振 荡后把试管放在热水中温热。 或:AgOH+2 NH3· 2O=[Ag(NH3)2] OH+2H2O H • 不久可以看到,试管内壁上附着一层光亮如镜的金属银。
H
(1)加成反应 这个反应属于 氧化反应还是 根据加成反应的概念写出CH3CHO 还原反应? 和H2 加成反应的方程式。
人教版-高二化学选修5教案:3-2----乙醛 醛类-------

第二节 乙醛 醛类本节重点知识1.熟记醛类物质的2种性质(1)还原性[与Ag(NH 3)2OH 、Cu(OH)2、O 2、溴水、KMnO 4(H +)溶液反应]; (2)氧化性(与H 2反应)。
2.明确1个转化关系 RCH 2OH ――→H 2RCHO ――→[O]RCOOH 3.掌握4个重要的反应CH 3CHO +2Ag(NH 3)2OH ――→△CH 3COONH 4+2Ag ↓+3NH 3+H 2O(检验醛基的存在)CH 3CHO +2Cu(OH)2+NaOH ――→△CH 3COONa +Cu 2O ↓+3H 2O(检验醛基的存在)2CH 3CHO +O 2――→催化剂△2CH 3COOH CH 3CHO +H 2――→催化剂△CH 3CH 2OH第一部分 课前延伸案1.(1)乙醇的催化氧化的方程式为 。
(2)乙二醇的催化氧化的方程式为(3)上述两个反应有机产物中的官能团是 ,由烃基与 相连而构成的化合物称为醛,饱和一元醛的通式为 。
第二部分 课内探究案探究点一 乙醛的性质1.乙醛是 色,具有刺激性气味的 体,密度比水 ,易 ,易 ,能跟水、乙醇等 。
2.按表中要求完成下列实验并填表:与新制的氢氧化铜悬浊液反应有产生NaOH溶液与CuSO4溶液反应制得有生成新制的Cu(OH)2是一种氧化剂,将乙醛,自身被还原为知识点1.乙醛的分子组成与结构乙醛的分子式是OHC42,结构式是,简写为CHOCH3。
注意对乙醛的结构简式,醛基要写为—CHO(OHC-)而不能写成—COH(HOC-)。
知识点2.乙醛的物理性质乙醛是无色、具有刺激性气味的液体,密度小于水,沸点为C8.20。
乙醛易挥发,易燃烧,能与水、乙醇、氯仿等互溶。
注意 因为乙醛易挥发,易燃烧,故在使用纯净的乙醛或高浓度的乙醛溶液时要注意防火。
知识点3.乙醛的化学性质从结构上乙醛可以看成是甲基与醛基()相连而构成的化合物。
由于醛基比较活泼,乙醛的化学性质主要由醛基决定。
醛的知识点总结归纳

醛的知识点总结归纳一、醛的基本概念醛是一类含有醛基(-CHO)的有机化合物,通式为R-CHO,其中R代表烷基或芳基。
醛是一种常见的有机化合物,在生物、化工和医药等领域广泛应用。
二、醛的命名和结构1. 命名法:(1)简称法:以醛基为主链的基本名是乙醛;(2)IUPAC命名法:以乙醛为例,正式名称是乙醛。
2. 结构特点:醛的结构特点是分子中含有酸酐基,也就是C=O键和-H(或者其他基团)连接的碳原子。
三、醛的性质1. 物理性质:(1)醛一般是无色液体,有刺激性气味;(2)醛具有较高的沸点和溶解度;(3)醛易挥发,可以自由沸腾。
2. 化学性质:(1)醛对氧气敏感,易发生氧化反应;(2)醛具有亲电性,易发生加成反应;(3)醛可以氧化成羧酸。
四、醛的制备方法1. 氧化法:将烃类氧化得到醛;2. 加氢法:用氢气和催化剂将酮还原成醛;3. 氢化法:用无色气体将酰氯转化为醛。
五、醛的用途1. 化工上:醛是制备酸醛树脂、醇醛树脂和脲醛树脂的原料;2. 生物上:醛是生物合成过程中的重要中间体;3. 医药上:醛是合成有机化合物的原料。
六、醛的应用1. 甲醛:用于制备甲醛树脂,主要用于家具、装饰材料和纺织品防霉防蛀;2. 乙醛:用于制备乙醛树脂,主要用于生产装饰涂料和包装涂料;3. 丙醛:用于制备丙醛树脂,主要用于粘合剂和密封材料。
七、醛的安全性1. 甲醛:甲醛是一种有毒的气体,会导致呼吸道疾病和癌症;2. 乙醛:乙醛是一种易燃和易爆的化合物,需要谨慎处理;3. 丙醛:丙醛会对皮肤和黏膜产生刺激作用,需要避免接触。
八、醛的发展前景随着环保意识的增强,醛类化合物的绿色和低成本的制备方法将会得到更多关注和研究。
同时,醛的应用领域也将会不断扩大和深化,为相关产业的升级和发展提供更多的机遇。
总结:醛作为一类有机化合物,在各个领域有着重要的应用价值。
但是,醛类化合物也具有一定的危险性,需要谨慎使用和处理。
随着科技的不断进步,醛的制备技术和应用领域也将会得到更多的发展和完善,为人类社会的绿色和可持续发展做出更多的贡献。
国标甲醛等级

国标甲醛等级
摘要:
1.甲醛概述
2.国标甲醛等级的划分
3.甲醛等级对人体健康的影响
4.如何降低甲醛污染
正文:
【甲醛概述】
甲醛是一种常见的有机化合物,化学式为HCHO,广泛应用于建筑、家具、装饰材料等产业。
然而,甲醛同时也是一种有害物质,长时间接触或吸入甲醛可能导致人体健康问题。
【国标甲醛等级的划分】
为了保护人体健康,我国对甲醛释放量制定了严格的标准。
国标甲醛等级主要分为三个等级:
1.E0 级:甲醛释放量小于或等于0.5mg/L,是目前最高的甲醛释放标准,适用于家具、地板等室内装修材料。
2.E1 级:甲醛释放量小于或等于1.5mg/L,适用于一般室内装修材料。
3.E2 级:甲醛释放量小于或等于5.0mg/L,适用于较低要求的室内装修材料。
【甲醛等级对人体健康的影响】
甲醛等级越高,释放的甲醛量越多,对人体健康的影响也越大。
长时间居
住在高甲醛浓度的环境中,可能导致以下健康问题:
1.刺激呼吸道,引发咳嗽、哮喘等呼吸道疾病。
2.导致皮肤过敏、瘙痒等问题。
3.影响生育能力,甚至导致胎儿畸形。
4.增加患癌症的风险。
【如何降低甲醛污染】
为了保障身体健康,降低甲醛污染,可以采取以下措施:
1.选择低甲醛释放的装修材料,如E0 级或E1 级的家具、地板等。
2.保持室内通风,新装修后尽量延长通风时间。
3.利用活性炭、绿植等吸附甲醛。
4.定期进行室内空气质量检测,发现甲醛超标时及时采取治理措施。
甲基醛结构式

甲基醛结构式甲基醛(Methanal)是一种有机化合物,也称为甲醛。
它的化学结构式为HCHO。
甲基醛是一种无色有刺激性气味的液体,具有广泛的应用领域。
本文将介绍甲基醛的结构式及其相关性质和应用。
一、甲基醛的结构式甲基醛的化学式为CH2O,结构式如下:H|C=O|H甲基醛分子由一个碳原子、一个氧原子和两个氢原子组成。
碳原子与氧原子之间形成一个双键,碳原子上连接一个氢原子,氧原子上连接一个氢原子。
这种结构使甲基醛具有高活性和一些特殊的性质。
二、甲基醛的性质1. 物理性质:(1)甲基醛是无色液体,在常温下呈气体态。
它具有刺激性气味,能够引起眼睛和呼吸道不适。
(2)甲基醛具有较低的沸点和熔点。
它的沸点为-19°C,熔点为-92°C。
(3)甲基醛可溶于水,容易与其他有机溶剂混溶。
2. 化学性质:(1)甲基醛是一种亲电试剂。
由于其氧原子上的孤电子对,它能够与亲核试剂形成加成反应,生成相应的加合物。
(2)甲基醛容易发生聚合反应,形成聚甲醛。
这种聚合产物可以用于合成具有特殊性质的材料,如酚醛树脂。
(3)甲基醛在强酸或强碱存在下可以发生缩合反应,形成糖类化合物。
这种缩合反应在生物体内起重要作用,参与糖代谢过程。
三、甲基醛的应用1. 工业应用:(1)甲基醛是一种重要的化工原料,广泛用于合成其他有机化合物,如甲醛树脂、甲醛胶等。
(2)甲基醛可用作防腐剂,具有杀菌和防腐效果。
在木材保护、纺织品加工、皮革制品等行业得到广泛应用。
(3)甲基醛可以用于制备草甘膦等农药,在农业生产中具有杀虫、除草的作用。
2. 医学应用:(1)甲基醛作为消毒剂具有强烈的杀菌作用,常用于医疗器械的灭菌和消毒。
(2)甲基醛可以用来制备染色剂、药物和化妆品等医学产品。
3. 其他应用:(1)甲基醛被广泛应用于纤维、胶粘剂、涂料和塑料等工业领域。
(2)甲基醛可以用作燃料电池的燃料,具有较高的能量密度和电化学性能。
总结:甲基醛是一种重要的有机化合物,具有刺激性气味和广泛的应用领域。
3-3 醛、酮 (教学课件)——高中化学人教版(2019)选择性必修三

【想一想】 1. 如何配置银氨溶液?写出此过程中涉及到的化学方程式
取1 mLቤተ መጻሕፍቲ ባይዱ2%的AgNO3溶液于洁净试管中,一边振荡试管,一边逐滴滴入 2%的稀氨水,至生成的沉淀恰好完全溶解,制得银氨溶液。
AgNO3+NH3·H2O=AgOH↓+NH4NO3 AgOH+2NH3·H2O=Ag(NH3)2OH+2H2O
【学习任务一】认识常见的醛、酮
甲醛:无色有强烈刺激性气味的气体,易溶于水 防腐杀菌剂(消毒、浸制标本)(水溶液称福尔马林);制药,香料,染料。 注意:儿童房甲醛超标易诱发儿童白血病
苯甲醛:最简单的芳香醛,是一种有苦杏仁味的无色液体,制造染料、香料及药物 的重要原料
乙醛:无色有强烈刺激性气味的液体,密度比水小,易挥发,容易燃烧,能与水、乙醇 等互溶。
【想一想】 2. 实验过程中有些同学没有得到光亮的银镜,可能的原因有哪些?
①试管内壁必须光滑、洁净; ②实验的银氨溶液应现配现用; ③必须用水浴加热,不可用酒精灯直接加热; ④加热时不能振荡和摇动试管。 3. 试管内部光亮的银镜,如何除去?
可用稀硝酸浸泡,再用水洗除去。
(2)与新制Cu(OH)2悬浊液反应
②与银氨溶液反应的化学方程式
CH3CHO+2Ag(NH3)2OH 水浴加热 CH3COONH4+2Ag↓+3NH3+H2O 1. 该反应可以用来检验分子中是否存在醛基 2. 工业上可用银镜反应对玻璃涂银制镜和制保温瓶瓶胆。 【想一想】能发生银镜反应的一定是醛类物质吗? 还原性糖(葡萄糖)、甲酸、甲酸某酯
丙酮的物理性质:无色透明液体,沸点56.2℃,易挥发,能与水、乙醇等互溶
【学习任务二】认识醛、酮的化学性质
1.请分析醛的结构特点,①分析含有何种官能团,是否含有不饱和键? ②找出极性键的位置,根据基团的相互影响,思考哪些极性键容易断裂?
高二化学选修5课件:3-2 醛

b.乙醛被银氨溶液氧化的方程式: CH3CHO+2Ag(NH3)2OH CH3COONH4+3NH3+H2O △ ――→ 2Ag↓+
第三章 烃的含氧衍生物
②乙醛被新制Cu(OH)2氧化 在加热条件下,乙醛与新制氢氧化铜悬浊液发生反应。 实验中看到的沉淀是氧化亚铜。涉及的主要化学反应是: Cu +2OH ===Cu(OH)2↓,CH3CHO+2Cu(OH)2
)人 教 Leabharlann 化 学第三章 烃的含氧衍生物
【解析】
已知甲醛的4个原子是共平面的,
提
示了羰基的碳原子所连接的3个原子也是共平面的。因此, 苯环(本身是共平面的一个环)有可能代替乙烯的1个H。OH 也有可能代替甲醛的1个H,B、C都可能在一个平面上。乙 烯的6个原子是共平面的,苯环代替了1个H,可以共平面。 只有苯乙酮,由于—CH3的C位于四面体的中心,3个H和羰
人 教 版 化 学
性能等。
第三章 烃的含氧衍生物
【答案】 1.C2H4O CH3CHO 2.烃基 醛基
3.无
4.无
刺激性
刺激性
液
气
小
易
20.8℃
水
乙醇
人 教 版 化 学
第三章 烃的含氧衍生物
5.(1)CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3+H2O (2)CH3CHO+2Cu(OH)2 Cu2O↓+2H2O 催化剂 (3)2CH3CHO+O2 ――→ 2CH3COOH △ 催化剂 (4)CH3CHO+H2 ――→ CH3CH2OH △ △ ――→
人 教 版 化 学
乙醛的还原性强而氧化性弱。乙醛发生氧化反应生成乙酸,
属于加氧氧化,乙醛发生还原反应生成乙醇,属于加氢还 原。
3-2 醛

C
H
C
H
C
H
极性键
O
醛基中碳氢键较活泼, 能被氧化成相应羧酸。
H
H
H C H
O
不饱和
C
极性键
H
烯烃和醛都含有不饱和双键,能发生加成反 应,这是两者的共性。但是,C=O双键和C=C双键 结构不同,发生的加成反应也不一样。因此,能 跟烯烃起加成反应的试剂(如溴),一般不跟醛 发生加成反应。 醛基中碳氧双键能发生加成反应。
家庭净化室内甲醛的植物
芦荟
龙舌兰
吸收甲醛的植物—猎醛香草 猎醛香草(又名:净 清香草)是一种挥发性芳 香植物,它释放的芳香 精油是由香茅醇、柠檬 烯等多种香精成分组成 的。 猎醛香草经中国室内环境监测工作委员会检 测该植物在24小时内吸收甲醛有效率达91%、氨 70%,猎醛香草具有真绿色,纯环保的特点,并且 清除甲醛的功效更持久不间断。
甲醛—室内污染的罪魁祸首
新装修房屋中甲醛超标的新闻媒体报道
/edu/ppt/ppt_playVideo.action?mediaVo.resId =55cee46faf508f0099b1c65c
木板中为什么含甲醛? 市面上的家具、地板可分两大类。一类称之为实木 ,另外一类为复合木材 ( 板材 ) 。前者为天然原木直接锯 切后成形,未经复合拼接处理的木材。后者是由天然木 材切锯后经粘接复合、表面覆以贴面而成。因为目前市 面上所用的粘着剂是以甲醛为主要原料制成的,所以复 合板材一般都会散发出一种刺激性的气体,即甲醛。 甲醛污染主要来源于人造板材 、内墙涂料、黏合剂、塑料壁纸 、 地毯以及购置的木质家具等。
自然界植物中的醛
CHO CH=CH—CHO
用于配制肥皂用香精,用作 食品的增香剂。用于口香糖对口 腔可起到杀菌和除臭双重功效。
5-3-2醛
练习:请写出C5H10O的同分异构体
复习引入
分子结构 物理性质 化学性质 用途制法 课堂小结 巩固练习
注意:醛和酮互为官能团异构
CHO 或
O CH
友 情
醛基不能写成-COH 或-CH=O
二、乙醛的物理性质
复习引入
分子结构 物理性质 化学性质 用途制法 课堂小结 巩固练习
乙醛是无色、有刺激性气味的 液体,密度比水小,易挥发(沸点 20.8º C),易燃烧, 能跟水、乙醇、 氯仿等互溶。 思考:乙醛、苯、CCl4均为无色液 体,如何用最简便的方法鉴别?
Ⅰ
复习引入
分子结构 物理性质 化学性质 用途制法 课堂小结 巩固练习
银镜反应
RCHO + 2[Ag(NH3)2]+ + 2OH RCOO + NH4++2Ag +3NH3+ H2O Ⅱ 与新制的氢氧化铜反应
△
RCHO + 2Cu(OH)2 RCOOH + Cu2O
+ 2H2O
d.使酸性KMnO4溶液和溴水褪色Байду номын сангаас
Ⅱ
复习引入
分子结构 物理性质 化学性质 用途制法 课堂小结 巩固练习
与新制的氢氧化铜反应
现象:有砖红色(Cu2O)沉淀生成 化学反应方程式: 2Cu(OH)2+CH3CHO
△
Cu2O↓+CH3COOH+H2O
复习引入
分子结构 物理性质 化学性质 用途制法 课堂小结 巩固练习
1、氢氧化铜悬浊液一定要现用现制, 且碱一定要过量 配制新制的Cu(OH)2悬浊液:在 2ml10%NaOH溶液中滴入 2%CuSO4溶液 4~6滴,振荡。 2、实验时应加热到沸腾 3、1mol醛基 ~ 1mol Cu2O
15级3,2醛
2、乙醛的物理性质:
无色、具有刺激性气味的液体,密度比水小, 沸点20.8℃,易挥发,易燃烧,能和水、乙 醇、乙醚、氯仿等互溶。
★
3、乙醛的化学性质
(1) 加成反应
CH3CHO+H2
Ni
CH3CH2OH
也是 还原反应: 有机物分子中加入氢原子或失去 氧原子的反应。 那么氧化反应呢: 有机物分子中加入 氧原 子或失去氢原子的反应
KMnO4
HCOOH
2)与弱氧化剂的反应 甲醛与新制氢氧化铜的反应 ①:新制 Cu(OH)2反应
实验操作
1、配制新制的Cu(OH)2悬浊液:在2ml10%
NaOH溶液中滴入2%CuSO4溶液4~8滴,振荡。 碱必须过量 Cu2++2OH-= Cu(OH)2 2、甲醛的氧化:在上述蓝色浊液中加0.5ml 加热至沸腾。 甲醛溶液,
Ⅱ
与新制的氢氧化铜反应
c.使酸性KMnO4溶液和溴水褪色
课堂练习
某有机物的结构简式为CH2=CH-CHO,下 列对其化学性质的判断中,不正确的是( D ) A.能被银氨溶液氧化 B.能使酸性高锰酸钾溶液褪色
C.1mol该有机物只能与1molBr2发生加成反应
D.1mol该有机物只能与1molH2发生加成反应
★
6:醛基的检验
(1)、哪些有机物中含有—CHO? 醛、HCOOH(甲酸)、HCOOR(甲酸某酯)、葡萄糖、 麦芽糖 (2)、怎样检验醛基的存在? 银镜反应,新制的Cu(OH)2 (3)若某有机物同时含有双键和醛基,如何证明该 有机物确实含有醛基,双键? 【例】已知柠檬醛的结构简式为
CH3C=CHCH2CH2CH=CHCH
3:直接加热;
2:此反应必须在NaOH过量,碱性条件下才发生。 应用:
戊醛,2-戊酮,3-戊酮的鉴别方法

戊醛,2-戊酮,3-戊酮的鉴别方法戊醛、2-戊酮、3-戊酮是常见的三种化合物,它们在一些领域中广泛应用,例如有机合成、香料制造、医药生产等。
在这些应用中,它们的纯度及鉴别至关重要。
本文将介绍戊醛、2-戊酮、3-戊酮的鉴别方法。
一、理论基础1.1 戊醛戊醛,结构式为CH3CH2CH2CH2CHO,也称为丁醛,是一种饱和脂肪醛。
戊醛在纯态下是一种无色液体,有强烈的刺激臭味,易挥发、易燃、难溶于水,但易溶于有机溶剂。
1.2 2-戊酮3-戊酮,结构式为CH3COCH2CH2CH3,也称为戊酮,是一种饱和酮类化合物。
在纯态下,3-戊酮是一种无色液体,有弱的甜味和果香味,熔点为-79.9°C,沸点为146°C。
二、实验步骤及结果步骤1:将待测物与多孔瓷坩埚中的活性铜粉混合。
加入适量的环己烷搅拌混合,然后慢慢加入浓硫酸,观察溶液颜色变化。
结果:戊醛与活性铜粉和浓硫酸反应,生成一种紫色的化合物。
反应方程式:2Cu + O2 + 2H2SO4 → CuSO4·SO2 + 2H2O步骤1:将待测物分别加入两个试管中。
步骤2:向第一试管中加入一滴百倍量的2, 4-二硝基苯肼溶液和氢氧化钠溶液,搅拌后,加入5mL的10%的硫酸。
结果:2-戊酮与2,4-二硝基苯肼反应,生成一种橙红色的沉淀,是一种可溶性化合物。
C4H9COCH2CH3 + 2,4-二硝基苯肼→ CH3CH2C(NO2)2NHNH2 + H2O而3-戊酮不与氨基甲酸乙酯缩合,不产生橙红色沉淀。
结果:3-戊酮与氢氧化钠和碘化钠反应,生成一种含碘化合物,加入苯乙酮后,溶液中的含碘化合物被还原,出现紫色沉淀,是三碘苯乙酮。
三、结论通过上述实验步骤,可以鉴别戊醛、2-戊酮和3-戊酮。
戊醛能够与活性铜和浓硫酸反应生成紫色沉淀,而2-戊酮与2,4-二硝基苯肼反应生成橙红色可溶性沉淀且不与氨基甲酸乙酯缩合,而3-戊酮能与氢氧化钠和碘化钠反应,形成含碘化合物,加入苯乙酮后被还原出现紫色沉淀。
2,3,4-三羟基苯甲醛的质量标准

1. 三羟基苯甲醛的概述三羟基苯甲醛(2,3,4-trihydroxybenzaldehyde)是一种重要的有机化合物,具有多种生物活性和药用价值。
它常被用作药物合成的中间体,也可作为酶促反应的底物,具有很高的研究和应用价值。
由于其广泛的用途,制定和遵守三羟基苯甲醛的质量标准具有重要意义。
2. 三羟基苯甲醛的质量标准的重要性三羟基苯甲醛作为一种重要的有机合成中间体,其质量直接影响到药物合成等领域的产品质量。
制定、实施和严格执行三羟基苯甲醛的质量标准,不仅可以保证产品的稳定性和可靠性,也可以保护消费者的安全和权益,促进行业的健康发展。
对三羟基苯甲醛的质量标准要求必须严格、全面和周密,以确保其质量符合相应的标准和法规要求。
3. 三羟基苯甲醛的质量标准的深度评估制定和评估三羟基苯甲醛的质量标准需要从多个角度进行深入评估。
需要考虑其化学性质、物理性质和理化指标等方面的要求,以确保产品的纯度、稳定性和可控性;还需要从生产工艺、检测方法和质量管理体系等方面进行深入的研究和评估,以确保产品的生产过程和质量控制符合规范和标准要求。
4. 三羟基苯甲醛的质量标准的广度评估除了在生产和检测方面进行深入评估外,还需要考虑三羟基苯甲醛的产品应用领域和相关产业链条,以确保质量标准的广度覆盖到相关的行业和领域。
还需要考虑国际上的相关标准和规范,以确保质量标准的广度符合国际通行的标准,提高产品的国际竞争力和市场份额。
5. 我对三羟基苯甲醛的个人观点和理解在评估和制定三羟基苯甲醛的质量标准时,我认为应该充分考虑到其生产、检测、应用和国际化等多个方面的要求,确保质量标准的深度和广度得到充分的考量。
还应该注重其安全性、可持续性和环保性,促进相关产业的健康发展和可持续发展。
在制定和执行质量标准时,应该充分发挥政府、企业和社会的作用,形成合力,确保质量标准的有效实施和落地。
6. 总结回顾三羟基苯甲醛作为一种重要的有机合成中间体,其质量标准的深度和广度评估至关重要。
3,3-二甲基丁醛 合成装置 制造方法

3,3-二甲基丁醛合成装置制造方法
3,3-二甲基丁醛是一种有机化合物,其分子式为C6H12O,是一种无色液体,具有较强的刺激性气味。
3,3-二甲基丁醛在工业上有广泛的应用,比如用于制造纤维素材料、涂料等。
1. 合成装置
该合成装置主要包括反应釜、冷却器、加料泵、控制系统等,如图所示。
反应釜:选用一种适合的反应釜,可选用带搅拌器的不锈钢反应釜,反应釜的大小根据生产要求而定,一般来说,1 m3的反应釜可以满足需求。
冷却器:反应釜后面设有冷却器,冷却器可采用水冷却或空气冷却方式,可以使反应过程中温度保持稳定。
加料泵:反应釜设有加料口,需要用泵将原料加入反应釜中。
泵的选择要考虑到泵的流量、压力等因素。
控制系统:反应过程中需要监测温度、压力、加料量等。
可选用PLC控制系统进行全自动化操作,也可以人工操作。
2. 制造方法
步骤一:准备原料
原料主要包括环己烷、甲醛、硫酸、氢氧化钠等。
步骤二:反应过程
首先,在反应釜中加入一定量的环己烷和甲醛,然后加入一定量的催化剂和一定量的硫酸和氢氧化钠,开始进行反应。
反应过程中需要控制反应温度、反应压力等因素,反应时间一般为2-3小时。
反应完成后,将反应物进行分离。
将反应釜中的反应物用分离漏斗分离,分离出的上层液体为3,3-二甲基丁醛,下层液体为副产物。
分离出的3,3-二甲基丁醛可进行后续处理,制备出所需要的产品。
以上就是3,3-二甲基丁醛的合成装置及制造方法的详细介绍。
该方法简单、易操作,且效率高,适用于工业规模的生产。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
课题醛的性质和应用主备人王喜珠备课
2014-4-25 审核人
时间
【学习目标】
掌握乙醛的结构、主要性质和用途和醛基和醛类的概念
了解甲醛的性质和应用及酚醛树脂的制备方法、用途
学习重点:结构决定性质。
学习难点:结构分析法
学习方法:
合作学习、学案导学、实验探究
1. 书写乙醇的催化氧化的化学方程式
乙醛是由____基跟____基组成,其官能团是_________。
醛是_____ ___的化合物。
其通式是_________,饱和一元醛通式是
【思考】同碳原子数的醇和醛在分子组成和结构的区别是怎样的?
2.通过什么实验可以鉴别葡萄糖和淀粉呢?
一、乙醛
1.乙醛的物理性质
乙醛是_____色的_____体,具有_______气味。
沸点_____,_ ___挥发。
溶解性______。
2.乙醛的化学性质
(1)加成反应:乙醛与氢气反应的化学方程式
_______ _。
【思考】该反应的机理是怎样的?是氧化反应还是还原反应?
(2)氧化反应
A.银镜反应:
向硝酸银溶液中逐滴加入过量的氨水,实验现象为_______________ _
反应的离子方程式是________
再向其中滴入几滴乙醛溶液放在水浴中,实验现象为________________,
反应的离子方程式是________________
据此反应,可应用于__________________________。
【思考】a.在实验中如何制备银氨溶液?
b.某同学在银镜反应实验中,没有得到光亮的银镜,试分析造成实验失败的可能的原因。
B.乙醛与氢氧化铜溶液反应:
向盛有NaOH溶液的试管中,逐滴滴入CuSO4溶液,实验现象为______________,离子方程式为_______ __ ____,然后加入几滴乙醛,加热至沸腾,实验现象为___ _____,发生反应的化学方程式为_____ ,
据此反应,可应用于________________________。
【思考】某同学在做此实验时,将CuSO4溶液与NaOH溶液混合后,再加入几滴乙醛并加热至沸腾,没有出现砖红色沉淀,试分析买验失败的原因。
3.乙醛的用途:列举乙醛的重要用途
二、甲醛
1.甲醛的分子式_________,结构简式________。
【思考】(1)从结构上看甲醛与其他醛类,有什么区别?
(2)在甲醛中的两个氢原子有没有区别?
2.甲醛的物理性质:甲醛又叫________,_______色________气味的________体。
溶解性_________,福尔马林是质量分数含___________的甲醛水溶液。
3.列举甲醛的重要用途:
4.甲醛的化学性质(写出反应的化学方程式):
(1)与氢气加成__ ___________
(2)银镜反应__________________________
(3)与新制得的氢氧化铜溶液反应_________
(4)与苯酚发生缩聚反应____________。
