河南省临颍县南街高级中学2020届高三下学期第一次月考化学试题 Word版含答案
安徽省阜阳市2023-2024学年高一下学期4月月考化学试题含答案

2023级高一下学期第一次教学质量检测化学(答案在最后)考生注意:1.本试卷分选择题和非选择题两部分。
满分100分,考试时间75分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。
选择题每小题选出答案后,用2B 铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第二册第五章~第六章。
5.可能用到的相对原子质量:H1C12N14O16Na23S32Fe56一、选择题(本题共14小题,每小题3分,共计42分。
在每小题列出的四个选项中,只有一项是符合题目要求的)1.化学与生产、生活密切相关,下列说法中错误的是A.陶瓷的主要原料是黏土,陶瓷可用于生产绝缘材料、卫生洁具等B.“天和”核心舱腔体使用的氮化硼陶瓷属于新型无机非金属材料C.风力发电可以减少对化石燃料的依赖,发电时机械能转化为电能、热能D.废旧电池中含有重金属,属于有害垃圾,故采用深挖填埋的方式处理【答案】D【解析】【详解】A .陶瓷的主要原料是黏土、石英等物质,陶瓷可用于生产绝缘材料、卫生洁具等,A 正确;B .氮化硼陶瓷属于新型无机非金属材料,B 正确;C .风力发电可减少火力发电的量,从而减少对化石燃料的依赖,风力发电时风吹动叶片,叶片旋转发电,机械能转化为电能、热能,C 正确;D .废旧电池中含有重金属,深埋会污染土壤,应集中交给专门的处理部门处理,D 错误;故答案选D 。
2.氨的催化氧化是工业制硝酸的重要步骤,反应方程式为()3224NH 5O 4NO 6H O g Δ++催化剂。
下列物质表示的化学反应速率最快的是A.()113v NH 0.8mol L min --=⋅⋅B.v(O 2)=1.25mol·L -1·min -1C.()11v NO 0.02mol L s --=⋅⋅D.v(H 2O)=1.2mol·L -1·min -1【答案】C【解析】【详解】比较速率时需要转化为同一物质同一单位进行比较,或者速率除以各自的系数比较大小。
2020届高三化学精准培优专练:十六 弱电解质电离平衡及电离平衡常数 Word版含答案

1.影响电离平衡的因素典例1.常温下,在pH =5的CH 3COOH 溶液中存在如下电离平衡:CH 3COOH CH 3COO −+H +,对于该平衡,下列叙述正确的是( )A .加入水时,平衡向右移动,CH 3COOH 电离常数增大B .加入少量CH 3COONa 固体,平衡向右移动C .加入少量NaOH 固体,平衡向右移动,c (H +)减小D .加入少量pH =5的硫酸,溶液中c (H +)增大 2.电离平衡常数的应用典例2.分析下表,下列选项错误的是( )弱酸 CH 3COOH HCN H 2CO 3 电离常数 (25℃)1.8×10-54.9×10-10K a1=4.3×10-7 K a2=5.6×10-11A .CH 3COO -、HCO -3、CN -在溶液中可以大量共存B .向食醋中加入水可使CH 3COOH 的电离平衡向电离方向移动C .相同物质的量浓度的Na 2CO 3和NaCN 溶液,后者pH 较大D .pH =a 的上述3种酸溶液,加水后溶液的pH 仍相同,则醋酸中加入水的体积最小 3.强弱电解质的比较典例3.某温度下,相同体积、相同pH 的氨水和氢氧化钠溶液加水稀释时的pH 变化曲线如图所示,下列判断正确的是( )A .a 点导电能力比b 点强B .b 点的K w 值大于c 点C .与盐酸完全反应时,消耗盐酸体积V a >V c培优点十六 弱电解质电离平衡及电离平衡常数一.弱电解质电离平衡及电离平衡常数的应用D .a 、c 两点的c (H +)相等 4.实验探究典例4.25℃时,0.1 mol·L -1 HA 溶液中c (H +)c (O H -)=108,0.01 mol·L -1 BOH 溶液pH=12。
请回答下列问题:(1)0.1 mol·L -1 HA 溶液pH= ,HA 的电离常数K a 为 ,BOH 是 (填“强电解质”或“弱电解质”)。
2024届河南省许昌市重点中学高三3月份第一次模拟考试化学试卷含解析

2024届河南省许昌市重点中学高三3月份第一次模拟考试化学试卷注意事项1.考生要认真填写考场号和座位序号。
2.试题所有答案必须填涂或书写在答题卡上,在试卷上作答无效。
第一部分必须用2B 铅笔作答;第二部分必须用黑色字迹的签字笔作答。
3.考试结束后,考生须将试卷和答题卡放在桌面上,待监考员收回。
一、选择题(每题只有一个选项符合题意)1、以PbO为原料回收铅的过程如下:Ⅰ.将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbC14的溶液;Ⅱ.电解Na2PbCl4溶液后生成Pb,原理如图所示。
下列判断不正确的是A.阳极区的溶质主要是H2SO4B.电极Ⅱ的电极反应式为PbCl42—+2e—=Pb+4Cl—C.当有2. 07 g Pb生成时,通过阳离子交换膜的阳离子为0.04 molD.电解过程中为了实现物质的循环利用,可向阴极区补充PbO2、传感器可以检测空气中SO2的含量,传感器工作原理如下图所示。
下列叙述正确的是( )A.b为电源的正极B.负极反应式Ag - e- + Cl- = AgClC.当电路中电子转移为5×10-5mol时进入传感器的SO2为1.12 mLD.阴极的电极反应式是2HSO3-+2H++2e-= S2O42-+2H2O3、一种碳纳米管新型二次电池的装置如图所示。
下列说法中正确的是A.离子交换膜选用阳离子交换膜(只允许阳离子通过)B.正极的电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-C.导线中通过1mol电子时,理论上负极区溶液质量增加1g D.充电时,碳电极与电源的正极相连4、下列过程中,一定需要通电才能实现的是A.电解质电离B.电化学防腐C.蓄电池放电D.电解精炼铜5、在2L的密闭容器中,发生反应:C(s)+H2O(g)CO(g)+H2(g)+131.5kJ,5min后达到平衡,固体减少了24g,则A.ρ气体不变时反应达到平衡状态B.v正(CO)为2.4mol/(L∙min)C.若容器体积缩小,平衡常数减小D.增大C的量,平衡右移6、热催化合成氨面临的两难问题是:采用高温增大反应速率的同时会因平衡限制导致NH3产率降低。
2020-2021学年河南省高三第一次模拟考试数学(理)试题及答案解析
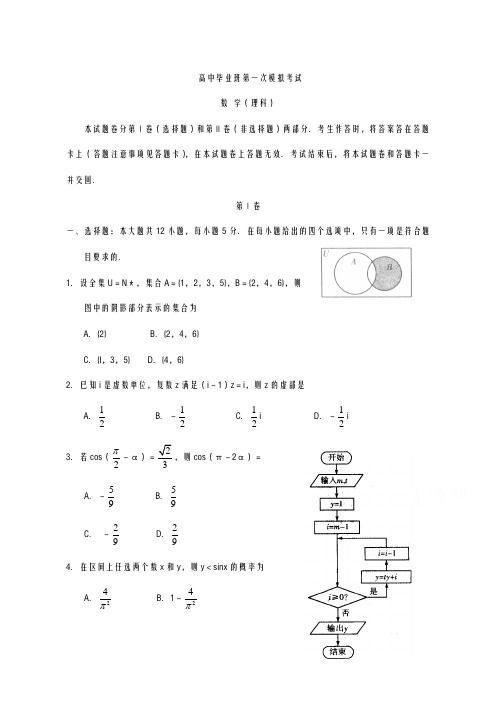
高中毕业班第一次模拟考试数 学(理科)本试题卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分.考生作答时,将答案答在答题卡上(答题注意事项见答题卡),在本试题卷上答题无效.考试结束后,将本试题卷和答题卡一并交回.第Ⅰ卷一、选择题:本大题共12小题,每小题5分.在每小题给出的四个选项中,只有一项是符合题目要求的.1.设全集U =N ﹡,集合A ={1,2,3,5},B ={2,4,6},则图中的阴影部分表示的集合为A .{2}B .{2,4,6}C .{l ,3,5}D .{4,6}2.已知i 是虚数单位,复数z 满足(i -1)z =i ,则z 的虚部是A .12B .-12C .12iD .-12i 3.若cos (2π2,则cos (π-2α)= A .-59 B .59C . -29 D .29 4.在区间上任选两个数x 和y ,则y <sinx 的概率为A .24π B .1-24πC .22πD .1-22π5.将函数y =cos (2x +6π)图象上的点P (4π,t )向右平移m (m >0)个单位长度得到点P ',若P '位于函数y =cos2x 的图象上,则A .t =-12,m 的最小值为12πB .t =32-,m 的最小值为12π C .t =-12,m 的最小值为6π D .t =32-,m 的最小值为6π 6.执行如图所示的程序框图,若输入m =4,t =3,则输出y =A .61B .62C .183D .1847.在31()n x x -的展开式中,所有项的二项式系数之和为4096,则其常数项为A .-1 10B .110C .220D .-2208.已知M 是抛物线C :2y =2px (p >0)上一点,F 是抛物线C 的焦点.若|MF |=p ,K 是抛物线C 的准线与x 轴的交点,则∠MKF =A .15°B .30°C .45°D .60°9.函数f (x )=|x |+2a x (其中a ∈R )的图象不可能是10.已知P 为矩形ABCD 所在平面内一点,AB =4,AD =3,PA 5PC =5PB uu r ·PD uu u r =A.-5 B.-5或0 C.5 D.0 11.某几何体的三视图如图所示,则该几何体的体积为A.16B.13C.1 D.212.已知函数f(x)=(22x-x-1)x e,则方程e2+tf(x)-9e=0(t∈R)的根的个数为A.2 B.3C.4 D.5第Ⅱ卷本卷包括必考题和选考题两部分.第13~21题为必考题.每个试题考生都必须作答.第22~23题为选考题,考生根据要求作答.二、填空题:本大题共4小题,每小题5分.13.双曲线22221x ya b-=(a>0,b>0)的一条渐近线与直线x-y+3=0平行,则此双曲线的离心率为______________.14.若实数x,y满足100,2,x yxy⎧⎪⎨⎪⎩-+≤>≤则221yx+的取值范围是_______________15.《孙子算经》是我国古代内容极其丰富的数学名著,书中有如下问题:“今有圆窖,周五丈四尺,深一丈八尺.问受粟几何?”其意思为:“有圆柱形容器,底面圆周长五丈四尺,高一丈八尺,求此容器能装多少斛米.”则该圆柱形容器能装米_________斛.(古制1丈=10尺,1斛=1.62立方尺,圆周率π≈3)16.在△ABC 中,内角A ,B ,C 的对边分别为a ,b ,c ,且a >b ,a >c .△ABC 的外接圆半径为1,a =3.若边BC 上一点D 满足BD =2DC ,且∠BAD =90°,则△ABC 的面积 为______________.三、解答题:解答应写出文字说明,证明过程或演算步骤.17.(本小题满分12分)已知数列{n a }的前n 项和为n S ,且满足n a =2n S +1(n ∈N ﹡).(Ⅰ)求数列{n a }的通项公式;(Ⅱ)若n b =(2n -1)·n a ,求数列{n b }的前n 项和n T .18.(本小题满分12分)某市为了制定合理的节电方案,供电局对居民用电情况进行了调查,通过抽样,获得了某年200户居民每户的月均用电量(单位:度),将数据按照分成9组,制成了如图所示的频率分布直方图.(Ⅰ)求直方图中m 的值并估计居民月均用电量的中位数;(Ⅱ)从样本里月均用电量不低于700度的用户中随机抽取4户,用X 表示月均用电量不低于800度的用户数,求随机变量X 的分布列及数学期望.19.(本小题满分12分)如图,在三棱柱ABC -A 1B 1C 1中,CA =CB ,侧面ABB 1A 1是边长为2的正方形,点E ,F 分别在线段AA 1,A 1B 1上,且AE =12, A 1F =34,CE ⊥EF (Ⅰ)证明:平面ABB 1A 1⊥平面ABC ;(Ⅱ)若CA ⊥CB ,求直线AC 1与平面CEF 所成角的正弦值.20.(本小题满分12分)已知圆O : 221x y +=过椭圆C :22221y x a b +=(a >b >0)的短轴端点,P ,Q 分别是圆O 与椭圆C 上任意两点,且线段PQ 长度的最大值为3.(Ⅰ)求椭圆C 的方程;(Ⅱ)过点(0,t)作圆O 的一条切线交椭圆C 于M ,N 两点,求△OMN 的面积的最大值.21.(本小题满分12分)已知函数f (x )=2x +2ax +bcosx 在点(2π、f (2π))处的切线方程为y =34π. (Ⅰ)求a ,b 的值,并讨论f (x )在上的增减性;(Ⅱ)若f (x 1)=f (x 2),且0<x 1<x 2<π,求证:12()2x x f '+<0. (参考公式cos θ-cos ϕ=-2sin 2θϕ+sin 2θϕ-)请考生在第22,23题中任选一题作答,如果多做,则按所做的第一题计分.作答时请写清题号.22.(本小题满分10分)选修4—4:坐标系与参数方程在平面直角坐标系xOy 中,直线l 的参数方程为12x t y ⎧⎪⎪⎨⎪⎪⎩==1(t 为参数).以坐标原点为极点,x 轴正半轴为极轴建立极坐标系,圆C 的极坐标方程为ρ=2sin θ.(Ⅰ)判断直线l 与圆C 的交点个数;(Ⅱ)若圆C 与直线l 交于A ,B 两点,求线段AB 的长度.23.(本小题满分10分)选修4—5:不等式选讲已知函数f (x )=|x +2|-|x -2|+m (m ∈R ).(Ⅰ)若m =1,求不等式f (x )≥0的解集;(Ⅱ)若方程f (x )=x 有三个实根,求实数m 的取值范围.。
河南省濮阳市2020届高三第一次模拟考试理综化学试题Word版含解析

B.硝酸根离子得电子转变成铵根离子,在正极发生反响,故B错误;
C.该装置中的总反响为:3Fe+ +2H++H2O=Fe3O4+ ,消耗氢离子,使氢离子浓度减小,pH增大,故C错误;
D. 正极反响为: +8e−+10H+= +3H2O,由反响可知每产生1mol 转移8mol电子,当电路中有 电子转移时,溶液中会有 生成,故D错误;
(二)将馏出液放入分液漏斗中,用适量的CH2Cl2进行萃取作用后置于枯燥的锥形瓶中,并参加适量枯燥剂进行充分,将枯燥好的溶液参加蒸馏烧瓶中,通过一系列操作,最后烧瓶中剩下的橙黄色液体就是柠檬烯。先根据其利用率及产生柠檬烯的体积和密度计算其质量,结合桔子皮质量计算出枯皮中柠檬烯的质量分数。
【详解】(1)甲中长的玻璃导管一端与空气相通,其作用是平安管,能起到平衡压强的作用;蒸馏结束时为防止倒吸现象的发生,应先将乙中的导气管从溶液中移出液面;
B. 假设撤去⑥,那么⑦中的水蒸气逆向进入⑤中,导致FeCl3水解生成Fe(OH)3,Fe(OH)3受热分解变为Fe2O3,B正确;
C. 加热时装置中的空气会与与Fe反响,故应先通入一段时间Cl2,以排尽装置中的空气,防止加热时被被空气氧化,C正确;
D. 枯燥的氯气无漂白性、酸性,D错误;
故合理选项是D。
河南省濮阳市2021届高三毕业班第一次模拟考试
理科综合化学试题
1.化学与生产、生活密切相关。以下说法错误的选项水涂抹被蚊虫叮咬处可减轻疼痛感或瘙痒感
C.向棕黄色的甘蔗汁中参加适量的活性炭搅拌后,甘蔗汁可变为无色
D.石油液化气属于绿色燃料,燃烧时不可能产生有害成分
A. 铁电极的电极反响式:
河南省新野县第一高级中学2024_2025学年高一化学下学期第二次月考试题

2024-2025高一年级下期其次次月考化学试卷可能用到的相对原子质量:H 1 C 12 O 16 Pb 207 Br 80一、选择题(每题3分,共48分)1.锗酸铋(简称BGO)是我国研制胜利的一种性能优良的闪耀晶体材料,其中锗(Ge与碳同主族)元素处于最高价态,铋元素(Bi与氮同主族)的价态与它跟氯形成某种共价氯化物所呈的价态相同,且此氯化物中铋具有8电子稳定结构。
BGO的化学式是()A.Bi3Ge3O15B.Bi4Ge3O12C.Bi4Ge3O16D.Bi3Ge3O122.下列有关化学用语的表示方法中正确的是()A.过氧化氢的电子式B.NH4I的电子式:C.比例模型可以表示二氧化碳分子,也可以表示水分子D.CO2分子的结构式:O=C=O3.下列条件肯定能使反应速率增大的是()①增加反应物的物质的量②上升温度③缩小反应容器的体积④不断分别诞生成物⑤加入MnO2A.全部B.①②⑤C.②③D.②4.元素周期表中未呈周期性改变的是A.原子序数 B.元素性质C.原子半径D.化合价5.能说明氯的非金属性比硫强的事实是()A.氯化氢的酸性强于硫化氢B.氯化氢的稳定性比硫化氢强C.氯气能与水反应而硫不能D.氯原子最外电子层上有7个电子而硫最外电子层上有6个电子6.近年来有多个品牌的手机电池曾发生爆炸事故,公众对电池平安性的重视程度越来越高,燃料电池作为平安性能较好的一类化学电源得到了更快的发展。
一种以联氨(N2H4)为燃料的环保电池工作原理如图所示,工作时产生稳定无污染的物质。
下列说法不正确的是()A.M极生成氮气且电极旁边溶液酸性增加B.负极上每消耗1molN2H4,会有4molH+通过质子交换膜C.正极的电极反应式为:O2+4H++4e-=2H2OD.d口流出的液体是蒸馏水7.有某烷烃与烯烃的混合气体9.00g,该混合气体的密度为相同状况下氢气的11.25倍,将混合气体通过足量溴水,溴水质量增加4.20g,则原混合气体的组成为()A.甲烷、乙烯B.乙烷、乙烯 C .甲烷、丙烯 D.甲烷、丁烯8.下列说法中正确的是()A.质子数相同的微粒肯定属于同一种元素,但不肯定是同种核素B.原子的最外层有1-2个电子的元素都是活泼的金属元素C.同族元素的最外层电子数肯定相同D.在周期表中位于同周期且同族的不同核素,不肯定属于同种元素9.只用一种试剂就可将己烯、甲苯、硝基苯、水、氢氧化钠溶液鉴别开,这种试剂是()A .盐酸B .酸性高锰酸钾溶液C .溴水D .紫色石蕊溶液10.已知丙烷的二氯代物有四种同分异构体,则其六氯代物的异构体数目为()A.三种B.四种C.五种D.六种11.电池式氧传感器原理构造如图,可测定O2的含量。
高一年级下学期第一次月考化学试卷与答案解析(共两套)

高一年级下学期第一次月考化学试卷(一)注意事项:1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5 Fe 56 Mn 55 Ba 137一、选择题1.近年来,总有一些不法商贩为了牟取自身利益。
用硫磺(燃烧硫磺)对银耳进行熏制,使银耳增白。
这些不法商贩所制取的银耳是利用了A.SO2的氧化性 B.SO2漂白性 C.SO2的还原性 D.S的漂白性2.下列关于氮气的说法错误的是A.氮气在通常情况下不燃烧,也不支持燃烧,不能供给呼吸B.液氮可用于医学和高科技领域,制造低温环境C.利用氮气的稳定性,工业上用来替代稀有气体作焊接金属的保护气D.在高温高压、催化剂条件下与氢气反应时,氮气作还原剂3.化学与生产、生活、科技息息相关,下列叙述错误的是A.华为首款5G手机搭载了智能7nm制程SoC“麒麟980”手机芯片的主要成分是二氧化硅B.国产飞机C919用到氮化硅陶瓷是新型无机非金属材料C.小苏打是面包发酵粉的主要成分之一D.水玻璃可用作制备木材防火剂的原料4.碳纳米材料是近年来人们非常关注的一类新型无机非金属材料,下列关于碳纳米材料的说法中不正确的是A.C60是富勒烯的代表物,C60的摩尔质量为720g/molB.碳纳米管可用于生产电池和传感器C.石墨烯与石墨都具有导电性D.石墨烯的性质稳定,在氧气中不能燃烧5.对下列事实的解释错误的是A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定C.常温下,浓硝酸可以用铝制器皿贮存,说明铝与浓硝酸不反应D.将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一种气体,有白色沉淀,则通入的气体可能是NH36.下列物质之间的转化都能一步实现的是A.H2S→S→SO3→H2SO4 B.Si→SiO2→H2SiO3→Na2SiO3C.FeS2→SO2→Na2SO3→Na2SO4 D.N2→NH3→NO2→HNO3→NO27.某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是A.B中现象为溶液蓝色褪去B.装置C的作用是吸收SO2尾气,防止污染空气C.为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色褪去D.反应后,A中溶液的酸性增强8.下列实验用来证明气体SO2的存在,其中正确的是①能使品红溶液褪色②能使沾有酚酞和NaOH溶液的滤纸褪色③通入H2S饱和溶液中有浅黄色沉淀生成④通入足量的NaOH溶液中,再滴入BaCl2溶液,有白色沉淀生成,该沉淀能溶于盐酸⑤通入溴水中,溴水褪色,再滴加BaCl2溶液有白色沉淀产生,该沉淀难溶于稀硝酸A.③⑤能证明 B.①②④能证明 C.都不能证明 D.只有⑤能证明9.下列实验中金属或氧化物可以完全溶解的是A.1mol Cu与含2mol H2SO4的浓硫酸共热B.1mol MnO2与含2mol H2O2的溶液共热C.常温下1mol Al投入足量的浓硫酸中D.常温下1mol Cu投入含4mol HNO3的浓硝酸中10.如图,同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3、②NO2,进行喷泉实验。
河南省漯河市临颍县南街高级中学2020届高三月考英语试卷

英语试卷一、单选题(共20题;共40分)1.The doctor shares his phone number with the patients ________ they need medical assistance.A. if onlyB. as ifC. even thoughD. in case2._________ his high social status, it is really hard for us to ______his joining us in going west to teach children there.A. Considering; opposeB. Considered; prevent fromC. To consider; persuadeD. Being considered; object to3.—I'm thinking of going back to school to get another degree.—Sounds great!_____.A. It all dependsB. Go for itC. Never mindD. No wonder4.—The movie starta at 8:30, and we can have a quick bite before wo go.—_________. See you at 8:10.A. So longB. Sounds greatC. Good luckD. Have a good time5.So little ________ about science that the lecture was _______ my understanding.A. I know; overB. knew I; beyondC. did I know; beyondD. did I know; over6.—Tu Youyou won the 2016 State Preeminent Science and Technology Award for her work against parasitic diseases.—She deserves it. The consequences ________improved human health and reduced suffering are immeasurable.A. in honor ofB. in terms ofC. in defense ofD. in hopes of7.—This wall of air is an effective answer to the problem and it ______ work.—But it is a question to put such a wall of air around the statue.A. mayB. mustC. shouldD. could8. we have accomplished our mission, we hope the situation will return to normalcy.A. As soon asB. BecauseC. ThoughD. Once9.—Would you mind giving your advice on how to improve our business management?—If you make _____ most of the equipment, there will be _____ rise in production.A. the; aB. /; /C. /; aD. the; /10.— I am leaving for America to attend a trade fair tomorrow.— ________. See you in a couple of weeks.A. CongratulationsB. All the bestC. All the betterD. All in all11.Meeting my dear teachers and fellow students after so many years was indeed a warm occasion, ______ I'd strike into my heart forever.A. thatB. oneC. whenD. what12._______ made the school proud was ______ more than 90% of the students had been admitted to key universities.A. What; becauseB. What; thatC. That;whatD. That; because13.When somewhat better ________ academically, he returned home to continue his research.A. equippedB. had equippedC. providedD. providing14.Believe it or not,the young man,______disabled,managed to______a distance of 500 miles within 30 minutes.A. as if; walkB. though; runC. even; coverD. though; cover15.I'm sorry. for my illness, I would have come and lent a helping hand.A. Were it notB. If it were notC. Had it not beenD. If it has not been16.—Did you catch what I said?—Sorry. I ______ a text message just now.A. had answeringB. have answeredC. would answerD. was answering17.Everything _________ smoothly, more jobs created for people allow them to be independent of others.A. ranB. runsC. runningD. to run18.A rescue worker risked his life saving two tourists who _________ in the mountains for two days.A. are trappingB. have been trappedC. were trappingD. had been trapped19.—It's too complex, I think.—______. So we'd better make it easier for students to get involved.A. That's ridiculousB. That's the pointC. That's settledD. That's all right20.“Never for a second,” the boy says, “______ that my father would come to my rescue.”A. I doubtedB. do I doubtC. I have doubtedD. did I doubt二、填空题(共1题;共6分)21.根据短文内容,从短文后的选项中选出能填入空白处的最佳选项,选项中有两项为多余项。
2024届河南省青桐鸣联考高三上学期12月月考化学试题及答案

2024届普通高等学校招生全国统一考试青桐鸣大联考(高三化学)注意事项:1.答卷前,考生务必将自己的姓名、班级、考场号、座位号、考生号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.全卷满分100分,考试时间90分钟。
可能用到的相对原子质量:H:1 N:14 O:16 S:32 Cl:35.5 Fe:56 Bi:209一、选择题:本题共14小题,每小题3分,共42分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 废物改头换面,服务日常生活。
下列说法正确的是A. 钢管表面镀锌可起到防腐的作用,镀锌层破损后,钢管腐蚀速率加快B. 生产豆奶产生的豆渣可加工成面粉和饼干,豆渣中含有的纤维素与淀粉互为同分异构体C. 废弃玻璃磨粉可代替砂子掺入混凝土建造房子,玻璃的生产原料为纯碱、石灰石和石英砂D. 废旧轮胎制成的橡胶粉可掺入沥青中铺路,橡胶均属于天然有机高分子化合物2. 芳香族化合物a、b、c是有机合成的基础原料,下列有关说法错误的是A. a、b均能与NaOH溶液反应B. a、c均能与b发生酯化反应C. b的芳香族同分异构体有3种D. 基态碳原子与氧原子核外未成对电子数相等3. 下列关于化学实验的基本操作正确的是A .制备纯净的()2Fe OH B .收集氨气并进行尾气处理C .量取稀硫酸并排除滴定管中气泡D .用该装置进行喷泉实验A. AB. BC. CD. D4. 设A N 为阿伏加德罗常数的值,下列说法正确的是A. 46 g 2NO 和24N O 的混合气体中所含原子数目为4.5AN B. 乙酸和乙醇发生酯化反应生成1 mol 2H O 时,生成C—O 键的数目为A N C. 56 g Fe 与71 g 2Cl 完全反应,转移电子数目为3A N D. 1 mol/L 23Na CO 溶液中含有+的数目为2A N 5. 下列离子方程式错误的是A. 用过量氨水吸收少量2SO 气体:2232432SO 2NH H O 2NH SO H O +-+⋅=++B. 用3FeCl 溶液腐蚀覆铜板:3222Fe Cu 2Fe Cu ++++=+C. NaClO 溶液中通入少量2SO 气体:2224ClO SO H O Cl SO 2H---+++=++D. 向硫酸酸化的4KMnO 溶液中滴加少量双氧水:2422222MnO 6H 5H O 2Mn 5O 8H O-++++=+↑+6. 通过对已知物质的性质和实验的描述进行类比推测,得出的相应结论正确的是选项已知物质的性质和实验类比推测ACuSO4溶液和过量NaOH 溶液反应生成蓝色沉淀CuSO 4溶液和过量NH 3·H 2O 反应也生成蓝色沉淀的BNaHCO 3溶液与Al 2(SO 4)3溶液反应有沉淀和气体产生NaHCO 3溶液与Fe 2(SO 4)3溶液反应也有沉淀和气体产生C 向Na 2CO 3固体中加入少量水,伴随放热现象向NaHCO 3固体中加入少量水,也伴随放热现象D 少量CO 2通入Ba(OH)2溶液中产生白色沉淀少量CO 2通入BaCl 2溶液中也产生白色沉淀A. AB. BC. CD. D7. 有机物M 和N 是合成药物的中间体,在一定条件下M 可以转化为N ,其过程如图所示,下列说法错误的是A. 该反应类型为消去反应B. 可用金属Na 鉴别M 和NC. M 的分子式为9143C H O D. N 可使酸性4KMnO 溶液褪色8. 某兴趣小组以铝土矿(主要成分为23Al O ,还含有少量23Fe O 和2SiO )为主要原料制备絮凝剂聚合氯化铝()2mAlOH Cl b a ⎡⎤⎣⎦和金属铝的流程如图所示。
2020届高考化学一轮复习化学平衡常数及其应用作业Word版含答案

化学平衡常数及其应用一.选择题(共15小题)1.只改变一个影响因素,下列关于平衡常数K的叙述错误的是()A.K值不变,平衡可能移动B.K值变化,平衡一定移动C.温度变化,K值一定变化D.平衡移动,K值一定变化2.其它条件不变,升高温度下列数据不一定增大的是()A.可逆反应的化学平衡常数KB.0.1mol/LCH3COONa溶液的PHC.水的离子积常数KwD.弱电解质的电离程度3.T2℃时,将1mol X和2mol Y投入2L的密闭容器中,发生反应:X(g)+2Y⇌3Z(g)△H,测得物质X、Y的物质的量随时间变化如表所示,平衡时物质X的体积分数为φ,该反应的平衡常数(K)随温度的变化如图所示,则下列判断正确的是()A.前5min用Z表示的平均反应速率为1.2mol/(L•min)B.T2℃时,对于反应X(g)+Y(g)⇌Z(g)△H′,则2△H′=△HC.T2℃时,若以lmol X、2mol Y和1mol Z充入上述容器中,达到平衡时X的体积分数比φ大D.该反应的正反应是吸热反应,且T1<T24.已知某化学反应的平衡常数表达式为K=,在不同的温度下该反应的平衡常数值分别为:下列有关叙述不正确的是()A.该反应的化学方程式是:CO (g)+H2O (g)⇌CO2(g)+H2(g)B.上述反应的正反应是放热反应C.如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830℃,此时测得CO2为0.4 mol时,该反应为平衡状态D.某温度下,如果平衡浓度符合下列关系式:=,判断此时的温度是1000℃5.已知气相直接水合法制取乙醇的反应为H2O(g)+C2H4(g)⇌CH3CH2OH(g)。
在容积为3L的密闭容器中,当n(H2O):n(C2H4)=1:1时,乙烯的平衡转化率与温度、压强的关系如下图所示:下列说法正确的是()A.a、b两点平衡常数:b>aB.压强大小顺序:P1>P2>P3C.当混合气的密度不变时反应达到了平衡D.其他条件不变,增大起始投料,可提高乙烯转化率6.电石(主要成分为CaC2)是重要的基本化工原料。
2020届高三化学精准培优专练:十五 等效平衡的三种情况 Word版含答案

培优点十五等效平衡的三种情况一.等效平衡的三种情况1.恒温恒容—(△n(g)≠0) 投料换算成相同物质表示时量相同典例1.在恒温恒容的密闭容器,发生反应:3A(g)+B(g)x C(g)。
Ⅰ.将3mol A和2 mol B在一定条件下反应,达平衡时C的体积分数为a;Ⅱ.若起始时A、B、C投入的物质的量分别为n(A)、n(B)、n(C),平衡时C的体积分数也为a。
下列说法正确的是()A.若Ⅰ达平衡时,A、B、C各增加1mol,则B的转化率将一定增大B.若向Ⅰ平衡体系中再加入3mol A和2mol B,C的体积分数若大于a,可断定x>4 C.若x=2,则Ⅱ体系起始物质的量应满足3n(B)>n(A)+3D.若Ⅱ体系起始物质的量满足3n(C)+8n(A)=12n(B),则可判断x=42.恒温恒容— (△n(g)=0)投料换算成相同物质表示时等比例典例2.某温度时,发生反应2HI(g)H2(g)+I2(g),向三个体积相等的恒容密闭容器A、B、C中,分别加入①2mol HI;②3mol HI;③1mol H2与1mol I2,分别达到平衡时,以下关系正确的是()A.平衡时,各容器的压强:②=①=③B.平衡时,I2的浓度:②>①>③C.平衡时,I2的体积分数:②=①=③D.从反应开始到达平衡的时间:①>②=③3.恒温恒压—投料换算成相同物质表示时等比例典例3.已知:T℃时,2H(g)+Y(g)2I(g)ΔH=-196.6 kJ·mol-1。
T℃时,在一压强恒定的密闭容器中,加入4mol H和2mol Y,反应达到平衡后,放出354 kJ的热量。
若在上面的平衡体系中,再加入1mol I气体,T℃时达到新的平衡,此时气体H的物质的量为()A.0.8mol B.0.6mol C.0.5mol D.0.2mol二.对点增分集训1.在恒温恒压的密闭容器中投入2mol SO2和1mol O2,发生反应:2SO2(g)+O2(g)2SO 3(g)。
2020届高三化学精准培优专练:八 氧化性还原性强弱判断的几种方法 Word版含答案

1.根据氧化还原反应的方向判断 典例1.常温下,在溶液中可发生以下反应:①2Fe 2++Br 2==2Fe 3++2Br - ②2Br -+Cl 2==Br 2+2Cl - ③2Fe 3++2I -==2Fe 2++I 2;由此判断下列说法错误的是( )A .氧化性强弱顺序为:Cl 2>Br 2>Fe 3+>I 2B .还原性强弱顺序为:I ->Fe 2+>Br ->Cl -C .②中当有1mol Cl 2被还原时,可生成1mol 氧化产物D .Br 2与I -不能反应2.依据化学反应条件和反应程度进行判断典例2.实验室用下列方法制取氧气①4HCl(浓)+MnO 2====△MnCl 2+Cl 2↑+2H 2O ;②4HCl(浓)+O 22Cl 2+2H 2O③2KMnO 4 +16HCl=2KCl+2MnCl 2 +5Cl 2 ↑+8H 2O试比较上述反应中氧化剂氧化能力的强弱 。
3.根据原电池、电解池的电极反应判断典例3.A 、B 、C 是三种金属,根据下列①、②两个实验:①将A 与B 浸在稀硫酸中用导线相连,A 表面有气泡逸出,B 逐渐溶解;②电解物质的量浓度相同的A 、C 混合盐溶液时,阴极上先析出C (使用惰性电极)。
A 、B 、C 的还原性强弱顺序为( )A .A >B >C B .B >C >A C .C >A >BD .B >A >C1.下列说法正确的是( ) A .阳离子只有氧化性,阴离子只有还原性B .失电子难的原子得电子的能力一定强C .得到电子越多的氧化剂,其氧化性就越强D .要实现Fe 2+→Fe 3+的转化,必须加入氧化剂2.某小组比较Cl ﹣、Br ﹣、I ﹣的还原性,实验如下:培优点八 氧化性还原性强弱判断的几种方法一.氧化性还原性强弱判断的几种方法二.对点增分集训实验1 实验2 实验3装置现象 溶液颜色无明显变化;把蘸浓氨水的玻璃棒靠近试管口,产生白烟溶液变黄;把湿KI 淀粉试纸靠近试管口,变蓝 溶液变深紫色;经检验溶液含单质碘下列对实验的分析不合理的是( )A .实验1中,白烟是NH 4Cl 固体小颗粒B .根据实验1的现象和实验2的现象判断还原性:Br ﹣>C1﹣C .根据实验3的现象判断还原性:I ﹣>Br ﹣D .上述实验中利用了浓H 2SO 4的强氧化性、难挥发性等性质3.碘在地壳中主要以NaIO 3的形式存在,在海水中主要以I ﹣的形式存在,几种微粒之间的转化关系如图所示。
河南创新发展联盟2024-2025学年高一上学期9月月考化学试题

2024—2025年度河南省高一年级月考(一)化学本试卷满分100分,考试用时75分钟。
注意事项:1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教版必修第一册第一章第一节至第二节。
5.可能用到的相对原子质量:H :1 C :12 O :16一、选择题:本题共14小题,每小题3分,共42分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1. “莫道雪融便无迹,雪融成水水成冰。
”下列说法错误的是A. 冰水混合物属于纯净物B. 过氧化氢与水互为同素异形体C. “雪融成水”属于物理变化D. 水既不与酸反应也不与碱反应 2. 当光束通过下列物质时,会出现丁达尔效应的是A. 3FeCl 溶液B. 稀硫酸C. 氢氧化钠溶液D. 稀豆浆 3. 下列物质属于氧化物的是A. 23Fe OB. 4MgSOC. 3NaHCOD. ()4Na Al OH 4. 下列物质能使紫色石蕊试液变红的是A. 硫酸钠溶液B. 硫酸钡浊液C. 稀硝酸D. 氢氧化钾溶液 5. 下列电离方程式书写正确的是A. 22244H SO H SO +−=+ B. 333FeCl Fe Cl +−=+C. 2233K CO 2K CO +−=+D. 2Na S2Na 2S +−=+ 6. 《天工开物》记载了“烧铁器淬于胆矾水中,即成铜色也”。
“胆矾水”为硫酸铜溶液,下列说法错误的是A. 金属活动性:铁>铜B. 铁和铜均不能与氢氧化钠溶液反应C. 硫酸铜溶液能导电,则其为电解质D. 铁与硫酸铜反应的反应类型为置换反应 7. 甲烷、硫化氢催化重整新路线可高效制氢,其反应微观示意图如图,下列说法正确的是的A. 甲具有助燃性B. 乙属于二元酸C. 丙的化学名称为硫化碳D. 常温下,丁易溶于水8. 科学态度是化学学科核心素养的重要组成部分,下列说法正确的是A. 比较:二氧化碳与一氧化碳的组成元素相同,故两者的性质完全相同B. 分类:葡萄糖溶液、氢氧化镁浊液、氢氧化铁胶体均属于纯净物C. 分析:氯化钠固体不导电,因为氯化钠不是电解质D. 推理:碳酸钠属于碳酸盐,则碳酸钙也属于碳酸盐9. 向盛有一定量氧化铁烧杯中不断滴入稀硫酸(如图所示),下列说法正确的是A. 氧化铁的化学式为FeOB. 铁在纯氧中燃烧可得到FeOC. 完全反应后,所得液体属于混合物D. 稀硫酸中所含的微粒仅为H +和24SO −10. 下列反应属于复分解反应的是(下列反应均可发生)A. 氢气和氧气的反应B. 碳酸钡与稀盐酸的反应C. 高温煅烧大理石D. 木炭与水蒸气反应生成一氧化碳和氢气 11. 下列各组离子能在同一溶液中大量共存的是A. 2Fe +、3Al +、2S −、OH −B. 2Ca +、2Mg +、23CO −、23SO −C Ag +、Li +、Cl −、3NO − D. K +、Na +、4MnO −、24SO − 12. 将下列物质加入烧杯所盛的液体中,导电能力可增强的是(不考虑晶体的析出)A. 少量水B. 少量乙醇C. 少量氯化钾固体D. 少量稀硝酸的.13. 下列说法正确的是A. 碱性氧化物一定为金属氧化物B. 石墨能导电,则石墨为电解质C. 仅由一种元素形成的物质一定为纯净物D. 同一种物质,相同条件下,质量分数越大,导电能力越强14. 下列离子方程式书写正确的是A. 将少量氢氧化钡加入硫酸氢钠溶液中:224422H 2OH SO BaBaSO 2H O +−−++++=↓+ B. 将少量二氧化碳通入氯化钙溶液中:2223CaCO H O CaCO 2H ++++=↓+ C. 将氢氧化铝加入稀盐酸中:2OH H H O −++=D. 将氧化镁加入稀硫酸中:22O 2H H O −++=二、非选择题:本题共4小题,共58分。
届高三第三次模拟考试化学试题 Word版含答案

2020-2021学年度(上)高三第三次模拟考试化学试卷满分:100分考试时间:90分钟一.单项选择题(本题共10小题,每小题3分,共30分。
)1.化学与社会、生活、技术密切相关。
下列说法正确的是()A.有人说“一带一路”是“现代丝绸之路”,丝绸的主要成分是蛋白质,属于天然高分子化合物B.《周礼》记载“煤饼烧砺(贝壳)成灰”,并把这种灰称为“蜃”,主要成分为Ca(OH)2 C.晶体硅是“信息革命”的支柱材料,可用于制作光导纤维D.绿色化学的核心是应用化学原理对环境污染进行治理2.N A表示阿伏加德罗常数的值。
下列说法中正确的是()A. 常温下,0.1molCl2与足量NaOH溶液反应,转移的电子数目为0.2N AB. 12g石墨中含有C个数与C—C键的个数比为1:2C. 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3 mol I2转移的电子数为5N AD. 9.2gNO2、N2O4的混合气体中,含有的N原子总数为2N A3.从碘水中提取碘的实验操作是()A.蒸发B.萃取C.过滤D.分液4.铁是人类应用较早,当前应用量最大的金属元素。
下列有关铁及其化合物的说法中正确的是()A.赤铁矿的主要成分是Fe3O4B.铁与水蒸气在高温下的反应产物为Fe2O3和H2C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤D.Fe3+与KSCN产生红色沉淀5.常温下,下列各组离子在指定溶液中一定能大量共存的是()A.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO-3B.0.1 mol·L-1 Na2CO3溶液:K+、Ba2+、NO-3、Cl-C.0.1 mol·L-1 FeCl3溶液:K+、NH+4、I-、SCN-D.能使pH试纸显深红色的溶液:Fe3+、Cl-、Ba2+、Br-能大量共存6.下列反应中属于氧化还原反应,但不属于四种基本反应类型的是()A.CuO + H2Cu + H2O B.2KMnO4 K2MnO4 + MnO2+O2↑C.Fe2O3 + 3CO 2Fe + 2CO2D.NaOH + HCl = NaCl + H2O7.在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.7kJ,下列热化学方程式正确的是()A.CH3OH(l)+3/2O2(g)CO2(g)+2H2O(l)△H= -726.4 kJ/molB.2CH3OH(l)+3O2(g)2CO2(g)+4H2O(g)△H= -1452.8 kJ/molC.2CH3OH(l)+3O2(g)2CO2(g)+4H2O(l)△H= -726.4 kJ/molD.2CH3OH(l)+3O2(g)2CO2(g)+4H2O(g)△H= + 1452.8 kJ/mol8.一氧化氮对SARS病毒有直接抑制作用。
2020届高考化学一轮复习有机化合物的检验和鉴别作业Word版含答案

有机化合物的检验和鉴别一.选择题(共15小题)1.能用来鉴别乙醇、苯和己烯的试剂是()A.金属钠B.溴水C.硫酸铜溶液D.氢氧化钠溶液2.鉴别乙酸、乙醛不能选用的试剂是()A.银氨溶液B.碳酸氢钠C.新制氢氧化铜D.酚酞试液3.下列试剂中,能鉴别乙醇、乙醛和乙酸的是()A.氢氧化钠溶液B.石蕊试液C.新制氢氧化铜D.碳酸钠溶液4.不能鉴别黄色的溴水和碘水的物质是()A.CCl4B.淀粉溶液C.苯D.NaOH溶液5.下列说法错误的是()A.水可以用来鉴别苯和溴苯B.C4H9C1有四种同分异构体C.2﹣甲基丙烷与异丁烷互为同系物D.等物质的量的乙烯和乙醇完全燃烧的耗氧量相等6.有机物X、Y、Z、W的转化关系如图所示。
下列说法不正确的是()A.满足上述反应的X有五种B.Y含有两种官能团C.Z 能发生水解反应D.W 一定能使Br2/CCl4溶液褪色7.由X、Y和Z合成缓释药物M,下列说法不正确的是()A.M在体内能缓慢发生水解反应B.X可以由乙烯通过加成反应和取代反应制备C.1mol Y与NaOH溶液反应,最多能消耗3mol NaOHD.Z由加聚反应制得,其单体的结构简式是CH3CH=CHCOOH8.乙醇、A、B都是重要的有机化工原料,其中A、B是常见的不饱和烃,B分子中含碳量最高,各物质的转化关系图如图,则下列说法不正确的是()A.由题目推出:A是乙烯,B是乙炔B.反应①、②、③的反应类型相同C.A、B、D、E均能使酸性KMnO4溶液褪色D.有机物F中所有原子一定在同一平面上9.如图表示有机物M转化为X、Y、Z、W的四个不同反应。
下列叙述正确的是()A.与X官能团相同的X的同分异构体有9种B.反应②一定属于加成反应C.W分子中含有两种官能团D.Z的分子式为C3H2O10.已知气态烃A的密度是相同状况下氢气密度的14倍,有机物A~E能发生如图所示一系列变化,则下列说法错误的是()A.A分子中所有原子均在同一平面内B.C4H8O2含酯基的同分异构体有4种C.C的水溶液又称福尔马林,具有杀菌、防腐性能D.等物质的量的B、D与足量钠反应生成气体的量相等11.有机物W在工业上常用作溶剂和香料,其合成方法如下:下列说法不正确的是()A.M、N、W均能发生加成反应和取代反应B.N、W组成上相差一个CH2原子团,所以互为同系物C.1molM与1molw完全燃烧消耗O2的物质的量相同D.M苯环上的二氯代物有6种12.由物质a为原料,制备物质d(金刚烷)的合成路线如图所示。
河南省名校联考2024-2025学年高一上学期第一次月考数学试题(含解析)

河南省名校联考2024-2025学年上期高一第一次月考数学注意事项:1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教A版必修第一册前两章。
一、选择题:本题共8小题,每小题5分,共40分.在每小题给出的四个选项中,只有一项是符题目要求的.1.下列关系式正确的是A.3∈QB.—1∈NC. Z⊆ND. Q⊆R2.关于命题q:∀a<b,|a|≤|b|,下列结论正确的是A. q是存在量词命题,是真命题B. q是存在量词命题,是假命题C. q是全称量词命题,是假命题D. q是全称量词命题,是真命题3.已知集合A={x∈Z|3x―1∈Z},则用列举法表示A=A.{—2,0,2,4}B.{—2,0,1,2,4}C.{0,2,4}D.{2,4}4.已知a>0,b>0,c>0,则“a+b>c”是“a,b,c可以构成三角形的三条边”的A.充分不必要条件B.必要不充分条件C.充要条件D.既不充分也不必要条件5.已知正数a,b满足1a +2b=1,则a+2b的最小值为A.9B.6C.4D.36.已知集合A={(x,y)|y=x²+ ax+1},B={(x,y)|y=2x-3},C=A∩B,若C恰有1|真子集,则实数a=A.2B.6C.2或6D.—2或67.某花卉店售卖一种多肉植物,若每株多肉植物的售价为30元,则每天可卖出25株;若每株肉植物的售价每降低1元,则日销售量增加5株.为了使这种多肉植物每天的总销售额不于1250元,则每株这种多肉植物的最低售价为A.25元B.20元C.15元D.10元【高一数学第1页(共4页)】 ·A18.学校统计某班45名学生参加音乐、科学、体育3个兴趣小组的情况,其中有20名学生参加了音乐小组,有21名学生参加了科学小组,有22名学生参加了体育小组,有24名学生只参加了1个兴趣小组,有12名学生只参加了2个兴趣小组,则3个兴趣小组都没参加的学生有A.5名B.4名C.3名D.2名二、选择题:本题共3小题,每小题6分,共18分.在每小题给出的选项中,有多项符合题目要求.全部选对的得6分,部分选对的得部分分,有选错的得0分.9.下列各组对象能构成集合的有A.郑州大学 2024 级大一新生B.我国第一位获得奥运会金牌的运动员C.体型庞大的海洋生物D.唐宋八大家10.已知a>b>0,则使得a+ca >b+cb成立的充分条件可以是A. c=-2B. c=-1C. c=1D. c=211.已知二次函数y=ax²+bx+c(a,b,c为常数,且a≠0)的部分图象如图所示,则A. a+b>0B. abc>0C.13a+b+2c>0D.不等式bx²―ax―c>0的解集为{x|-2<x<1}三、填空题:本题共3小题,每小题5分,共15分.12.已知a=10―6,b=6―2,则a ▲ b.(填“◯”或“<”)13.已知a∈R,b∈R,集合{,则(a―b)³=.14.已知m<n<0,则8nm+n ―2mm―n的最大值为▲ .四、解答题:本题共5小题,共77分.解答应写出文字说明、证明过程或演算步骤.15.(13分)已知全集U=R,集合A={x|-2<x<3},B={x|a-1<x<2a}.(1)若a=2,求A∪B,C∪B;(2)若B⊆A,求a 的取值范围.【高一数学第2页(共4页)】 A116.(15分)给出下列两个结论:①关于x的方程.x²+mx―m+3=0无实数根;②存在0≤x≤2,使(m+1)x―3=0.(1)若结论①正确,求m 的取值范围;(2)若结论①,②中恰有一个正确,求m的取值范围.17.(15分)已知正数a,b,c 满足 abc=1.(1)若c=1,求2a +3b的最小值;(2)求a2+b2+2c2+8ac+bc的最小值.A11918.(17分)已知a∈R,函数y=ax²+(3a+2)x+2a+3.(1)当a=1时,函数y=ax²+(3a+2)x+2a+3的图象与x轴交于A(x₁,0),B(x₂,0)两点,求x31+x32;(2)求关于x的不等式y≥1的解集.19.(17分)设A是由若干个正整数组成的集合,且存在3个不同的元素a,b,c∈A,使得a-b=b-c,则称A 为“等差集”.(1)若集合A=1,3,5,9,B⊆A,且B是“等差集”,用列举法表示所有满足条件的B;(2)若集合.A=1,m,m²―1是“等差集”,求m的值;(3)已知正整数n≥3,证明:{x,x²,x³,…,x"}不是“等差集”.【高一数学第4 页(共4 页)】 A1·数学参考答案1. D 3₃∉Q,-1∉N,N ⊆Z,Q ⊆R2. C 由-2<1,|-2|>|1|,知q 是假命题,且q 是全称量词命题.3. A 因为3=1×3=(--1)×(-3),所以A={-2,0,2,4}.4. B 取a=5,b=3,c=1,满足a+b>c,此时b+c<a,a,b,c 不可以构成三角形的三条边.由a,b,c 可以构成三角形的三条边,得a+b>c.故“a+b>c”是“a,b,c 可以构成三角形的三条边”的必要不充分条件.5. A 因为 1a +2b =1,所以 a +2b =(1a +2b)(a +2b )=5+2b a+2a b.又a>0,b>0,所以 2ba + 2ab ≥22b a⋅2ab =4,当且仅当a=b=3时,等号成立,故a+2b 的最小值为9.6. D 因为C 恰有1个真子集,所以C 中只有1个元素.联立方程组 {y =x 2+ax +1,y =2x ―3,整理得 x ²+(a ―2)x +4=0,则 (a ―2)²―16=0,解得a=-2或6.7. D 设每株多肉植物的售价降低x(x∈N)元,则这种多肉植物每天的总销售额为(30-x)(25+5x)元.由(30-x)(25+5x)≥1 250,得5≤x≤20,故每株这种多肉植物的最低售价为30-20=10元.8. B 如图,由题可知 {a +b +9m +x ―20,a +c +m +z ―21,b +c +m +s ―21,a +b +c +1>22,a +b +z ―12,x +9z +z =24,则 3m=63-2(a+b+c)-(x+y+z)=15,则m=5,从而3个兴趣小组都没参加的学生有45-(a+b+c)-(x+y+z)-m=4名.9. ABD 由题可知,A ,B ,D 中的对象具有确定性,可以构成集合,C 中的对象不具有确定性,不能构成集合.10. AB 由a +c a>b +c b,得 a +c a ―b +cb=b (a +c )―a (b +c )ab=c (b ―a )ab>0.因为a>b>0,所以c<0.11. BCD 由图可知a>0,二次函数 y =ax ²+bx +c 的图象与x 轴相交于(--1,0),(2,0)两点,则 {a ―b +c =0,4a +2b +c =0,整理得 {b =―a ,c =―2a ,则 a+b=0, abc>0,A 不正确,B 正确. 由【高一数学·参考答案 第 1页(共4 页)】 ·A1·{4a―2b+c>0,9a+3b+c>0,得13a+b+2c>0,C正确.因为{b=―a,c=―2a,所以bx²―ax―c=―ax²―ax+2a>0,即x²+x―2<0,,解得-2<x<1,D正确.12.<a―b=10+2―26,因为( 10+2)2=12+45,(26)2=24,45<12(所以(10+2)2<(26)2,则10+2<26,从而a<b.13.8 由a+b,a,2=a²,2,0,得a=0或a=a².若a=0,则a²=0,,不符合集合元素的互异性.若a=a²,则a=0(舍去)或a=1,所以a+b=0,即b=-1,从而((a―b)³=8.14.―18nm+n ―2mm―n―4(m+n)―4(m―n)m+n―(m+n)+(m―n)m―n=3―[4(m―n) m+n +m+nm―n].因为m<n<0,所以4(m―n)m+n >0,m+nm―n>0,则4(m―n)m+n+m+nm―n≥24(m―n)m+n⋅m+nm―n=4,当且仅当m=3n时,等号成立,故的最大值为-(1)由a=2,得B={x|1<x<4}, ... 1分 (1)则或x≥4}. ... 3分 (3)因为A={x|-2<x<3},所以A∪B={x|-2<x<4}................................................5分(2)若B=∅,则a-1≥2a,解得a≤-1,满足B⊆A (7)若B≠∅,则由B⊆A,得分 (9)解得 (11)综上所述,a的取值范围为 (13)16.解:(1)由结论①正确,得分 (3)解得-6<m<2 (5)故当结论①正确时,m的取值范围为{m|-6<m<2}....................................6分(2)若m=-1,则原方程转化为-3=0,恒不成立. ... 7分 (7)若m≠-1,则由(m+1)x-3=0,得分 (8)从而解得 (10)当结论①正确,结论②不正确时, (12)当结论②正确,结论①不正确时,m≥2 (14)综上所述,当结论①,②中恰有一个正确时,m的取值范围为或m≥2}..........15 17.解分 (1)则 (4)当且仅当时,等号成立,故的最小值为₆ (6)(2)因为, (8)当且仅当a=b=c=1时,等号成立,... 9分 (9)所以分 (10) (12)当且仅当 ac+ bc=2时,等号成立,此时a=b=c=1, ... 14分 (14)所以的最小值为8………………………………………………………………………………15分18.解:(1)当a=1时,y=x²+5x+5.由题可知x₁,x₂;是方程x²+5x+5=0的两个实数根, (2)由{x21+5x1+5=0, x22+5x2+5=0,得{x 31=―5x21―5x1,x32=―5x22―5x2, 4分则x i+x32=―5(x21+x22)―5(x1+x2)=―5[(x1+x2)2―2x1x2]+25=―75+25=―50.6分(2)由y≥1,得ax²+(3a+2)x+2a+2≥0.当a=0时,不等式整理为………………………………………………………………………………………………………………………………………………………………………7分当a≠0时,令ax²+(3a+2)x+2a+2=(x+1)( ax+2a+2)=0,得x=---1或x=...............................................................................................................9分当a>0时,则原不等式的解集为或3x≥-1} (11)当--2<a<0时,―1<―2a+2a,则原不等式的解集为{x|―1≤x≤―2a+2a};当a=-2时,则原不等式的解集为{-1};...............................................................15分当a<-2时,则原不等式的解集为 (17)【高一数学·参考答案第3页(共4页)】 ·A1·…13分1,3,5或1,5,9,………………………………………………………………………… (1)故满足条件的B可能是{1,3,5},{1,5,9},{1,3,5,9}...........................................4分(2)解:由A 是“等差集”,得, ... 5 分 (5)且m≥2,则 (6)(舍去)或m=2 (8)当m=2时,A={1,2,3}是“等差集”,故m=2 (9)(3)证明:假设{x,x²,x³, (10)则存在1≤i<j<k≤n,其中i,j,k∈N*,使得 (11)即则分 (12)因为1≤i<j<k≤n,所以k-i>j-i,从而k-i≥j-i+1,... 13分 (13)则2xʲ⁻ⁱ=1+xᵏ⁻ⁱ≥1+xʲ⁻ⁱ⁺¹, ……………………14分则分 (15)因为x≥2,所以从而2-x>0,即x<2, (16)不是“等差集” (17)【高一数学·参考答案第 4 页(共4页)】。
2024-2025学年河南省开封市多校九年级上学期第一次月考化学试题

2024-2025学年河南省开封市多校九年级上学期第一次月考化学试题1.下列俗语与物质的化学性质无关的是A.玉不琢不成器B.火上浇油C.纸里包不住火D.生米煮成熟饭2.河南特产汝州汝瓷位居宋代“五大名窑”之首,其制作步骤中涉及化学变化的是A.水洗选料B.揉泥成型C.刻花印花D.装窑烧制3.“低碳节能,从我做起”,下列做法不符合“低碳生活”理念的是A.草稿纸双面使用B.出门随手关灯C.废旧书籍焚烧处理D.减少使用一次性餐具4.如图所示的图标表示A.禁止吸烟B.节约用水C.禁止烟火D.禁止燃放鞭炮5.规范的实验操作是实验成功和安全的重要保证。
下列实验操作不规范的是A.量取液体B.闻气体气味C.熄灭酒精灯D.倾倒液体6.人类的发展进步离不开科学家的贡献。
对下列科学家贡献的叙述不合理的是A.张青莲:精确测定部分元素相对原子质量B.门捷列夫:发现元素周期律并编制元素周期表C.拉瓦锡:用红磷燃烧法测得空气的组成D.汤姆孙:发现电子7.下列对科学探究认识错误的是A.化学实验是科学探究的重要途径B.科学探究应独立完成,不需要合作C.实验方案的设计是实验探究的重要环节D.科学探究的一般过程包括8个环节8.逻辑推理是一种重要的思维方法。
以下逻辑推理合理的是A.化学变化伴随有能量变化,所以有能量变化的一定是化学变化B.分子是由原子构成的,所以分子的质量和体积一定比原子大C.化合物中含有不同种元素,则由不同种元素组成的纯净物一定是化合物D.单质是由同种元素组成的物质,所以由同种元素组成的物质一定是单质9.如图是稀土元素钇在元素周期表中的相关信息,下列说法错误的是A.钇元素的原子序数为39B.钇元素属于金属元素C.钇元素的元素符号为YD.钇元素的相对原子质量为88.91g10. 5月15日是我国“防止碘缺乏病日”,防止碘缺乏病的有效措施是食盐“加碘”。
市场上销售的“加碘食盐”,是在食盐中加入了少量的碘酸钾(KIO3),下列关于“加碘食盐”的说法正确的是()A.“加碘食盐”是纯净物B.“加碘食盐”是化合物C.“加碘食盐”中有碘单质D.“加碘食盐”中有碘元素11.实验时必须严格遵守实验室安全规则。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
临颍县南街高级中学2020届高三下学期第一次月考
理科综合试卷化学部分
可能用到的相对原子质量:C 12Fe 56
7.化学与社会、生活密切相关。
对下列现象或事实的解释错误的是
选项现象或事实解释
A食盐能腐蚀铝制容器Al能与Na+发生置换反应
B用铁罐贮存浓硝酸常温下铁在浓硝酸中钝化
C用(NH4)2S2O8蚀刻铜制线路板S
的氧化性比Cu2+的强
2
D漂白粉在空气中久置变质Ca(ClO)2与CO2和H2O反应,生成的HClO分解
8.用图示装置及药品制备有关气体,其中能达到实验目的的是
9.三氯异氰尿酸(TCCA)是一种极强的氧化剂和氯化剂,可通过下列方法制备:
CO(NH2)2
CA TCCA
下列说法正确的是
A.尿素属于无机物
B.反应①为非氧化还原反应
C.反应②中n(CA)∶n(HClO)=1∶1
D.CA分子中各原子均满足8电子结构
10.元素周期表的一部分如图所示,W、X、Y、Z均为短周期主族元素,X与Z的最高正价之和与W的相等。
下列说法错误的是
A.原子半径:X>Y>Z>W
B.X2W2中含有离子键和共价键
C.Y的最高价氧化物对应的水化物难溶于水
D.将由X、Z的单质组成的混合物放入冷水中,Z的单质不发生反应
11.二茂铁[Fe(C5H5)2]可作为燃料的节能消烟剂、抗爆剂。
二茂铁的电化学制备装置与原理如图所示,下列说法正确的是
A.a为电源的正极
B.电解质溶液是NaBr水溶液和DMF溶液的混合液
C.电解池的总反应化学方程式为Fe+2C5H6Fe(C5H5)2+H2↑
D.二茂铁制备过程中阴极的电极反应为2H++2e-H2↑
12.下列实验中,对应的现象以及结论都正确的是
选项实验现象结论
A将(NH4)2SO3加热产生的气体通入BaCl2溶液中无明显现象SO2与BaCl2溶液作用不产生BaSO3沉淀B将浓硫酸滴入蔗糖中产生的气体通入品红溶液中品红褪色浓硫酸具有强氧化性
C将Fe2O3溶于足量HI溶液后,加入2滴淀粉溶液溶液颜色不变反应生成FeI3和H2O
D往漂白粉中加入浓硫酸产生黄绿色气体Cl2的氧化性比H2SO4的强
13.25 ℃时,用0.1 mol·L-1NaOH溶液滴定某二元弱酸H2A,H2A被滴定分数、pH及物种分布分数
δ[δ(X)=]如图所示:
下列说法错误的是
A.用NaOH溶液滴定0.1 mol·L-1NaHA溶液可用酚酞作指示剂
B.0.1 mol·L-1Na2A溶液中:c(Na+)<c(HA-)+2c(A2-)
C.0.1 mol·L-1NaHA溶液中:c(Na+)>c(HA-)>c(A2-)>c(H2A)
D.H2A 的K2=1×10-7
26.(14分)金属钛在航天、潜海和医疗方面应用广泛。
以钛铁矿[主要成分为钛酸亚铁(FeTiO3),含少量Fe2O3]为原料制备钛的工艺流程如图所示。
(1)步骤②、③、④中,均需进行的操作是(填操作名称)。
(2)滤液1中钛元素以TiO2+形式存在,步骤①中生成TiO2+的化学方程式为,硫酸质量分数对钛、铁浸出率的影响如图所示,据此判断,酸浸时所加硫酸的质量分数应为(填范围)。
(3)请结合离子方程式解释步骤④中加热水的原因:。
(4)电解法制备Ti的装置是以石墨为阳极,TiO2为阴极,熔融CaO为电解质。
Ti在(填“阳极”或“阴极”)生成,(填“能”或“不能”)将熔融CaO换成石灰乳。
(5)以绿矾为原料,可以制备重要工业原料氧化铁,基本流程如下:
①绿矾溶液中离子浓度由大到小的顺序为。
②FeCO3达到沉淀溶解平衡时,室温下测得溶液的pH为8,c(Fe2+)=1.0×10-5 mol·L-1。
所得FeCO3中(填“含”或“不含”)有Fe(OH)2。
(已知: K sp[Fe(OH)2] = 4.9×10-17)
27.(14分)实验室用酸性蚀刻废液(含Cu2+、H+、CuC、Cl-等)和碱性蚀刻废液[N、Cu(NH3、NH3·H2O 等]制备CuI(白色固体)的实验流程如下:
(1)步骤Ⅰ中发生了多个反应,其中Cu(NH3与盐酸反应生成Cu(OH)Cl的离子方程式为。
(2)步骤Ⅳ需控制pH为1~2,80 ℃下进行,合适的加热方式是。
(3)步骤Ⅴ的具体步骤是蒸发浓缩、、。
(4)步骤Ⅵ在下列装置(夹持及加热装置已省略)中进行。
①装置a中盛装浓硫酸的仪器的名称是,圆底烧瓶中发生反应的化学方程式为。
②装置c中反应完成的现象是。
③用装置d中的溶液洗涤制得的CuI的目的是,然后再用无水乙醇洗涤的目的是。
28.(15分)雾霾由多种污染物形成,包含颗粒物(PM2.5)、氮氧化物(NO x)、CO、SO2等。
化学在解决雾霾污染中有着重要的作用。
(1)已知:①2CO(g)+O2(g)2CO2(g)ΔH1=-566.0 kJ·mol-1
②2NO(g)+O2(g)2NO2(g)ΔH2=-116.5 kJ·mol-1
③N2(g)+O2(g)2NO(g)ΔH3=+180.5 kJ·mol-1
废气中NO2与CO 转化成无污染气体的热化学方程式为。
(2)研究发现利用NH3可除去硝酸工业尾气中的NO。
NH3与NO的物质的量之比分别为1∶2、1∶1.5、3∶1时,NO脱除率随温度变化的曲线如图所示。
①曲线a中,NO的起始浓度为6×10-4 mg·m-3,从X点到Y点经过10 s,则该时间段内NO的脱除速率为mg· m-3·s-1。
②曲线c对应的NH3与NO的物质的量之比是,其理由是。
(3)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2。
活化过程的能量变化模拟计算结果如图所示。
无水情况下,一个氧分子的活化能为,容易活化氧分子的条件是(填“有水”或“无水”)。
(4)利用反应6NO2+8NH37N2+12H2O构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。
①B极的电极反应式为。
②若反应转移1.2 mol电子,A极生成N2的体积为L(标准状况)。
35.[化学——物质结构与性质](15分)
(NH4)3[Fe(SCN)6]、[Fe(TCNE)(NCCH3)2][FeCl4] 、K4[Fe(CN)6]·3H2O等铁的配合物用途非常广泛。
回答下列问题:
(1)基态Fe原子价层电子的电子排布图(轨道表达式)为。
(2)Fe与Ca位于同一周期且最外层电子构型相同,铁的熔点和沸点均比钙的高,其原因是。
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的电负性从大到小的顺序是。
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配体为CH3CN和TCNE()。
①CH3CN中碳原子的杂化方式是和。
②TCNE中第一电离能较大的是(填元素符号),分子中所有原子(填“在”或“不在”)同一平面,分子中σ 键与π键的数目之比是。
(5)K4[Fe(CN)6]·3H2O是食盐的抗结剂,强热分解有Fe3C生成, Fe3C 的晶胞结构如图所示:
Fe3C的密度为(列出计算式)g·cm-3。
36.[化学——有机化学基础](15分)
花椒毒素(H)有抗实验性心律失常、镇痛、抗炎等作用。
由芳香族化合物A为原料合成H的一种合成路线如下:
已知:+ClCH2CH2Cl+HCl。
回答下列问题:
(1)A的化学名称是(用系统命名法)。
(2)G中所含官能团的名称是。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。
E中(填“有”或“没有”)手性碳。
(4)反应⑥的反应类型是。
(5)D的结构简式为。
(6)F与足量NaOH溶液反应的化学方程式为。
(7)芳香族化合物W是D的同分异构体,能发生银镜反应和水解反应,遇FeCl3溶液发生显色反应;W的核磁共振氢谱有5组峰,且面积比为1∶2∶2∶2∶1。
符合上述要求的W有种。
(8)有机物M()是一种重要的化工原料。
设计由邻苯二酚和氯乙酰氯(ClCH2COCl)为起始原料制备有机物M的合成路线。
(无机试剂及有机溶剂任用)。
