非化学计量和掺杂对_Na_1_2_Bi_1_省略_Ba_0_08_TiO_3陶瓷[1]
A位Bi掺杂对(Bi_(0.5)Na_(0.5))TiO_3无铅压电陶瓷性能研究

Vo .9 No2l 1 2 .
企 业 技 术 开 发
TECHNOL OGI CAL DEVEL0PMENT OF ENTERPRI E S
21 00年 1 月 1
NO .01 V2 0
A位 B 掺 杂对( iNa5 i 无铅压 电陶瓷性能研 究 i B0 QT o3 s )
rt ( n a b a io a s ts tr gfo d r eh d Wea a zdi cot eueb —a irci n aue s ae K 5 ∞) yt d in l t ei e n olw e to . n l e s rs u tr yx rydf at nadmesrdi N r t a n i  ̄ I m y t mi r f o t
A sr c: k iee t b 3 x i 3 K N—x i 3 ( = .0 00 5 00 0 0 2 crmi sm ls i iee t i o ig b ta t Wema edf rn O 一 B2 ( N f N 0 B2 ) x 00 ,. ,.1. . ) ea c a pe t df rn B pn O 0 0 wh f d
dee ti rp risa dpe o lcrcpo e is T er s l p o e h ta p o r t id pn on t h n ete sr cu eo ilcrcp o et n iz ee ti rp r e . h e ut r v st a p rp i e B o igd o a g h tu tr fKNN e t a c
在 = .0 00 5时达 到 了最 大值 , 6 . p / 为 7 1 C N。 一
关 键 词 : 电材 料 , N — B 2 介 电性 能 , 电性 能 压 K N xi , 0 压 中 图分 类 号 : Q 7 T 14 文 献标 识码 : A 文 章 编 号 :0 6 8 3 ( 0 0 2 — 0 4 O 10 — 9 7 2 1 ) 1 0 6 一 2
南京师范大学附属中学2024-2025学年高一上学期期中化学试题

南京师大附中2024-2025学年度第1学期高一年级十月段考化学试卷本试卷分选择题和非选择题两部分。
共100分。
考试用时60分钟。
相对原子质量:H1 C12 N14 O16 Na22 Mg24 Al27 S32 Br80选择题单项选择题:共17题,每题3分,共51分。
每题只有一个选项最符合题意。
1. 下列物质属于非电解质的是 A. 氨水B. 4CHC. 熔融NaOHD. 3CH COOH2. 古医典富载化学知识,下述之物见其氧化性者为 A. 石硫黄()S :“能化……银、铜、铁,奇物” B. 石灰()CaO :“以水沃之,即热蒸而解” C. 金()Au :“虽被火亦未熟”D. 石钟乳()3CaCO :“色黄,以苦酒(醋)洗刷则白”3. 用A N 代表阿伏加德罗常数的数值。
下列说法中,正确的是 A. 2.3g 金属钠由原子完全变成离子时,得到的电子数为A 0.1N B. A 0.2N 个硫酸分子与0.2mol 磷酸含有相同的氧原子数 C. 28g 氮气所含的原子数为A ND. A N 个氧气分子与A N 个氢气分子的质量比为8:1 4. 下列说法中正确的是A. 溶液与胶体的本质区别是丁达尔效应B. 反应物中失去电子的物质为氧化剂C. 书写离子方程式时电解质均要写成离子形式D. HCl 在溶于水的过程中,形成了自由移动的水合氢离子和水合氯离子5. 下列物质的分类正确的是酸碱盐酸性氧化物 碱性氧化物A24H SO NaOH 3CaCO 2H O CaOB HCl()2Ca OH4NH Cl CO MgOC HCl KOH3KNO3SO23Fe OD3HNO()Mg OH Cl 2MgCl 2COCuO6. 在4℃时,向100 mL 水中溶解了22.4 L NH 3(标准状况下测得)后形成溶液。
下列说法中正确的是( )A. 所得溶液的体积为22.5 LB. 该溶液物质的量浓度为10 mol/LC. 该溶液物质的量浓度因溶液的密度未知而无法求得D. 该溶液中溶质的质量分数因溶液的密度未知而无法求得7. 国产航母001A 等舰艇的船底都涂有含Cu 2O 的防污涂料,制备Cu 2O 的一种方法为Zn +2CuSO 4+2NaOH=Cu 2O +ZnSO 4+Na 2SO 4+H 2O 。
材料科学基础第三章答案

习题:第一章第二章第三章第四章第五章第六章第七章第八章>九章第十章第十一章答案:第一章第二章第三章第四章第五章第六堇第七章第八章第九章第十章第十一章3-2 略。
3-2试述位错的基本类型及其特点。
解:位错主要有两种:刃型位错和螺型位错。
刃型位错特点:滑移方向与位错线垂直,符号±,有多余半片原子面。
螺型位错特点:滑移方向与位错线平行,与位错线垂直的面不是平面,呈螺施状,称螺型位错。
3-3非化学计量化合物有何特点?为什么非化学计量化合物都是n型或p型半导体材料?解:非化学计量化合物的特点:非化学计量化合物产生及缺陷浓度与气氛性质、压力有关;可以看作是高价化合物与低价化合物的固溶体;缺陷浓度与温度有关,这点可以从平衡常数看出;非化学计量化合物都是半导体。
由于负离子缺位和间隙正离子使金属离子过剩产生金属离子过剩(n 型)半导体,正离子缺位和间隙负离子使负离子过剩产生负离子过剩(p型)半导体。
3-4影响置换型固溶体和间隙型固溶体形成的因素有哪些?解:影响形成置换型固溶体影响因素:(1)离子尺寸:15%规律:1. (R-R2)/R1>15%^连续。
2.<15%连续。
3.>40%不能形成固熔体。
(2)离子价:电价相同,形成连续固熔体。
(3 )晶体结构因素:基质,杂质结构相同,形成连续固熔体。
(4)场强因素。
(5)电负性:差值小,形成固熔体。
差值大形成化合物。
影响形成间隙型固溶体影响因素:(1)杂质质点大小:即添加的原子愈小,易形成固溶体,反之亦然。
(2)晶体(基质)结构:离子尺寸是与晶体结构的关系密切相关的,在一定程度上来说,结构中间隙的大小起了决定性的作用。
一般晶体中空隙愈大,结构愈疏松,易形成固溶体。
(3)电价因素:外来杂质原子进人间隙时,必然引起晶体结构中电价的不平衡,这时可以通过生成空位,产生部分取代或离子的价态变化来保持电价平衡。
3-5试分析形成固溶体后对晶体性质的影响。
TiO_2光催化剂非金属掺杂的机理研究进展

作者简介:吴雪松,男,江西九江人,硕士研究生,从事与环境功能材料的设计与研发,E -mail :fengcaihangban @ ,TEL :1376714020收稿日期:2008212210TiO 2光催化剂非金属掺杂的机理研究进展吴雪松,唐星华,张 波(南昌航空大学环境与化学工程学院,江西南昌 330036) 摘 要:根据国内外对TiO 2光催化剂改性的研究状况,将TiO 2光催化剂的改性研究分为金属离子掺杂、贵金属沉积、表面光敏化、复合半导体、非金属离子掺杂等方面。
其中,非金属掺杂较其他方式的掺杂优势明显,但其机理研究不够深入。
对TiO 2光催化剂的各种非金属掺杂的机理研究进展进行了综述。
关键词:TiO 2;非金属;改性 中图分类号:O 64411 文献标识码:A 文章编号:167129905(2009)0520033203 TiO 2在常温常压下能使水中造成污染的有机物较快地完全氧化为CO 2和H 2O 等无害物质,具有表面晶格缺陷、高比表面能、化学性质稳定、无毒、反应速度快、价格低廉等优点,是一种较为理想的光催化剂。
但是,TiO 2作为光催化剂的应用也存在不容忽视的缺点:吸光频带窄,光生空穴电子复合速度快,量子产率低,只对太阳光中的紫外光有响应。
为此,各国科研工作者积极探索TiO 2的改性方法。
TiO 2的改性大致包括金属离子掺杂、贵金属沉积、表面光敏化、复合半导体、非金属离子掺杂。
掺杂金属离子、金属氧化物,贵金属沉积、复合半导体等方法都有较好的可见光响应特性,但金属元素的掺杂使热稳定性变差,易成为电子-空穴对复合中心,降低了光催化活性,并且金属元素注入的成本也较高。
另外,金属元素掺杂还会降低紫外光活性。
表面光敏化存在受光腐蚀的现象,且可能产生二次污染。
与以上方法相比,掺杂非金属离子不但能将纳米TiO 2的光响应波长拓展至可见光区域,还能保持在紫外光区的光催化活性。
非金属元素掺杂TiO 2制取方式简单,光催化效率高,必将成为纳米TiO 2改性的主流方向。
n-dmbi掺杂机制 -回复

n-dmbi掺杂机制-回复NDMBI掺杂机制(Non-Destructive Minority Barrier Interface doping mechanism)是一种在半导体材料中引入杂质以调节材料电性的方法。
该机制主要针对磷化铟(InP)等III-V族化合物半导体材料,可以提高半导体器件的性能。
接下来,本文将从什么是NDMBI机制、NDMBI的优势、NDMBI的原理、NDMBI的应用等方面详细介绍。
一、什么是NDMBI机制NDMBI机制是通过引入大量杂质原子来增加InP半导体材料的电导率,从而改变材料的电性。
其中,NDMBI机制中的“Non-destructive”是指在材料溅射过程中不会破坏材料结构的意思。
通过引入大量的杂质原子,NDMBI可以有效地改善材料的载流子输运性能,提高器件的效率和性能。
二、NDMBI的优势1.提高载流子浓度:NDMBI机制可以有效地增加InP材料中载流子的浓度,从而提高材料的电导率。
这样一来,在半导体器件中,电流可以更加容易地通过。
2.保护材料晶格结构:NDMBI机制不会破坏InP材料的晶格结构,因此可以避免由于结构破坏导致的性能下降问题。
3.易实现与成本低廉:NDMBI机制可以通过常规的溅射方法实现,设备和工艺成熟,不需要使用昂贵的设备和复杂的制备工艺。
三、NDMBI的原理NDMBI机制的关键原理是通过溅射过程中产生的高能离子,将杂质原子嵌入到InP材料晶格中,并形成局部的氮、硫、砷等杂质原子团簇。
这些杂质原子团簇将形成少数载流子的储藏区域,增加半导体材料的载流子浓度。
具体而言,NDMBI机制利用外界电子轰击材料表面产生的高能场效应,使表面杂质原子离势能降低,提供克服屏障势垒从而引起自旋压缩。
通过这种方式,可以将杂质原子嵌入到InP材料的近表面层中,形成具有高载流子浓度的区域。
在制备过程中,通过调节溅射参数(如杂质原子的能量、剂量等),可以控制NDMBI机制的效果和杂质浓度。
N_C掺杂比例对锐钛矿TiO_2电子结构影响的第一性原理研究

DOI:10.13524/j.2095-008x.2014.01.009N、C掺杂比例对锐钛矿TiO2电子结构影响的第一性原理研究李宗宝1a,贾礼超2,王霞1b,王梁杰1a(1.铜仁学院a.物理与电子科学系;b.生物科学与化学系,贵州铜仁554300;2.华中科技大学材料科学与工程学院,材料加工与模具重点实验室,武汉430074)摘要:采用基于密度泛函理论方法,分别计算了N、C原子不同比例掺杂锐钛矿TiO2的形成能、晶体结构和电子结构等性质。
计算结果表明:原子替位掺杂后体系晶格发生畸变;C原子替位掺杂更倾向于替代Ti位,N倾向于替代O位;两种替位掺杂均使TiO2光吸收带发生明显红移;N掺杂比例为2.08%和3.13%、C掺杂比例为2.08%时,对TiO2的改性最佳。
关键词:锐钛矿TiO2;第一性原理;N掺杂;C掺杂;形成能中图分类号:O647文献标志码:A文章编号:2095-008X(2014)01-0041-06DensityfunctiontheoryontheelectronicstructurepropertyofanataseTiO2dopedbyNorCwithdifferentpercentsLIZong-Bao1a,JIALi-Chao2,WANGXia1b,WANGLiang-Jie1a(1.TongrenUniversity,a.DepartmentofPhysics&ElectronicScience;b.DepartmentofBiology&Chemistry,Guizhou554300,China;2.SchoolofMaterialsScienceandEngineering,StateKeyLabofMaterialProcessingandDie&MouldTechnology,HuazhongUniversityofScienceandTechnology,Wuhan430074,China)Abstract:Formationenergy,crystalstructureandelectronicstructureofC,NdopedanataseTiO2arecalculatedbasedonthedensityfunctionaltheoryofplane-waveultrasoftpseudoptential.Resultsindicatethat,duetodopingoftheCorNatomsinanataseTiO2,thelatticedistortsobviously.ThesubstitutionofCtendstoTisitewhileNtendstoOsite.Allthesubstitutionsleadtotheredshiftoftheopticalabsorptionandincreasingcoefficientoflightabsorption.WhenNconcentrationsare2.08%and3.13%inN-dopedTiO2,thehighestphotocatalyticactivityisobtained,whileitis2.08%forC-dopedone.Keywords:anataseTiO2;DFT;N-doped;C-doped;formationenergy0引言TiO2因在太阳光的转换和储存、温室气体光催化氧化还原及环境有机污染物降解等方面得到广泛应用,已成为最具应用潜力的光催化剂[1-4]。
非化学计量掺杂Ce纳米SiO_2复合粒子聚砜复合膜处理油田含油污水技术研究

复 合 粒 子 添 加 量 为 PS F质 量 的 1 % 时 , 合 膜 的 水 接 触 角 为 最 小试 验 值 4 . 。 以 此 添 加 量 制 得 的 0 复 17;
8 %左 右 ; 油 污水 处理 后 可达到 国 家农 田灌溉 水质 标 准 。 5 含
关 键 词 含 油 污 水 处 理 聚 砜 复 合 膜 纳 米 SO i 粒 子 C e 非 化 学 计 量 油 田 外 排 污 水 和 油 田 回 注 水 需 要 经 过 深 度 处 理 度 、 性 及 抗 压 实 性 能 的 进 一 步 提 高 。 而 非 化 学 计 韧
第2 2卷 第 3期 21 0 0年 6月
中 国 海 上 油 气
CH 1 A FFSH 0 RE I AN D A S N O OI G
V ol22 No. _ .
J n 2 1 u .0 0
非化 学 计 量 掺 杂 C e纳 米 SO2复 合粒 子 聚 砜 复合 膜 i
生 成一 层油 层 , 至会堵 塞 膜孔 , 甚 降低 渗 透功 能 。因
此, 目前 处 理含 油 污 水 常使 用 经过 改性 后 的有 机 无 机 复合 膜1 。将 无机粒 子添加 到高分 子膜 材料 中进 . 行有机一 机共混改 性 , 无 由于操 作简 便 、 制备 工艺 简单 而被广 泛采用 。张裕卿 等口 通过 向聚砜 ( S ) 中加 P F膜 入亲水 性较强 的无 机粒 子 ( Al 3 , 如 ) 大大提 高 了膜 O 的亲水 性 , 而 提 高 了膜 的抗 污染 能力 。纳 米 SO 从 i 粒子 表 面具有 丰 富 的 硅 羟 基 和 较 强 的表 面效 应 , 将 其填 充 到高 分子 材料 中可改 善材 料 的硬 度 、 性 、 韧 亲 水性 等 性 质 。A. ot o等 将 纳 米 SO B tn i i 粒 子 添 加到 聚 乙烯醇 中 , 复合 膜 的热 力 学 性 能 、 度 、 使 强 韧 性等 均有 不 同程 度 的 提 高 。T. . re 等 ] C Mek l 向聚 4 甲基一一 一 2戊炔 中加入 纳米 SO。 i 粒子 , 所得 复 合 膜 使 材料 的渗 透性 和选 择性 都 得 到 了一 定 提高 。虽 然 用
高中化学会考知识点总结

高中化学会考知识点总结一、化学基本概念。
1. 物质的组成与分类。
- 元素:具有相同核电荷数(质子数)的一类原子的总称。
- 原子:化学变化中的最小粒子。
由原子核和核外电子构成,原子核由质子和中子构成(氢原子无中子)。
- 分子:保持物质化学性质的最小粒子。
- 离子:带电荷的原子或原子团。
阳离子(如Na^+)带正电荷,阴离子(如Cl^-)带负电荷。
- 物质分类。
- 混合物:由两种或多种物质混合而成(如空气、溶液等)。
- 纯净物:由一种物质组成。
- 单质:由同种元素组成的纯净物(如O_2、Fe等)。
- 金属单质(如Cu、Al等)。
- 非金属单质(如O_2、C等)。
- 化合物:由不同种元素组成的纯净物(如H_2O、NaCl等)。
- 无机化合物。
- 氧化物:由两种元素组成,其中一种是氧元素的化合物(如CO_2、CaO等)。
- 酸:在水溶液中电离出的阳离子全部是H^+的化合物(如HCl、H_2SO_4等)。
- 碱:在水溶液中电离出的阴离子全部是OH^-的化合物(如NaOH、Ca(OH)_2等)。
- 盐:由金属离子(或铵根离子)和酸根离子组成的化合物(如NaCl、CuSO_4等)。
- 有机化合物:含有碳元素的化合物(除CO、CO_2、碳酸盐等简单含碳化合物),如CH_4、C_2H_5OH等。
2. 化学用语。
- 元素符号:表示一种元素(如H表示氢元素),还表示该元素的一个原子(如H表示一个氢原子)。
- 化学式:用元素符号和数字的组合表示物质组成的式子。
- 单质化学式的书写。
- 金属单质、固态非金属单质(如C、S、P等)、稀有气体单质(如He、Ne等)用元素符号表示。
- 气态非金属单质,如H_2、O_2、N_2、Cl_2等,在元素符号右下角写上表示分子中所含原子数的数字。
- 化合物化学式的书写:根据化合价来书写。
- 化合价:元素的原子相互化合的数目。
- 化合物中各元素化合价代数和为零。
- 化学方程式:用化学式表示化学反应的式子。
半导体材料电导

(1) 价控半导体陶瓷杂质能级的形成 例如: BaTiO3的半导化通过添加微量的稀土元素,在其禁带间形成杂质能级,实现半导化。添加 La的BaTiO3原料在空气中烧成, 用不同于晶格离子价态的杂质取代晶格离子,形成局部能级,使绝缘体实现半导化而成为导电陶瓷。 杂质离子应具有和被取代离子几乎相同的尺寸;杂质离子本身有固定的价态。 1)价控半导体陶瓷: 2)杂质离子需满足的条件
-
-
-
-
-
-
-
qVD
qVD
x
空间电荷区
空间电荷区内电势由 np区不断下降, 空间电荷区内电势能由np区不断升高, p区能带相对向上移, n区能带向下移,至费米能级相等, n-p结达平衡状态,没有净电流通过。 势垒高度:qVD = EFn—EFp
p
n
(1) 光照
n
p
p
+
_
E
n区空穴
P区电子
非平衡载流子在内建电场作用下,n区空穴向p区扩散,p区电子向n区扩散;
4
若p-n结开路,在结的两边积累电子—空穴对,产生开路电压。
5
用能量等于或大于禁带宽度的光子照射p-n结;
1
p、n区都产生电子—空穴对,产生非平衡载流子;
2
非平衡载流子破坏原来的热平衡;
Ev
EA
EA
-
价电子 2LiNi´ 2h ·
— — — — — — — —
+
+
+
Eg
Ec
Ev
ED
ED
+
LaBa · 弱束缚电子和自由电子
(2) 组分缺陷
化学计量配比的化合物分子式: MO 有阳离子空位的氧化物分子式: M 1-xO 形成非化学计量配比的化合物的原因:由温度和气氛引起。 平衡状态,缺陷反应如下: O21/2(g)=VM×+2Oo× VM× = VM´ + h · VM´ = VM´´ + h · 出现此类缺陷的阳离子往往具有正二价和正三价。
掺杂离子的改性原理是啥

掺杂离子的改性原理是啥
掺杂离子的改性原理是通过向材料中引入外部离子(通常是金属离子),改变材料的结构和性质。
掺杂离子可以替代材料的原子或占据材料的空位,形成新的化学键或改变原有化学键的性质,使材料的导电性、磁性、光学性质、力学性能等发生变化。
掺杂离子的改性原理主要有以下几个方面:
1. 替代掺杂:外部离子替代材料中的原子或占据材料的空位。
替代掺杂可以改变材料的化学成分和晶体结构,影响材料的晶格常数、晶粒尺寸和位错密度等。
2. 空位掺杂:外部离子占据材料晶格的空位,形成实质性的空位掺杂。
空位掺杂可以改变材料的原子间距和晶格缺陷,影响材料的电子传输和热传导性能。
3. 电荷掺杂:通过引入具有不同电荷的离子改变材料的电子结构和载流子浓度。
正电荷掺杂会引入更多的载流子,增加材料的导电性能;负电荷掺杂则会减少载流子浓度,降低材料的导电性能。
通过这些掺杂改性的方法,可以调控材料的各种性能,使其更适应于特定的应用需求。
例如,通过金属离子的掺杂,可以将半导体材料转变为导体材料,提高电导率;通过稀土离子的掺杂,可以改变材料的发光性质,使其应用于发光器件和显示器件等领域。
S掺杂对锐钛矿相TiO_2电子结构与光催化性能的影响_赵宗彦

S 掺杂对锐钛矿相TiO 2电子结构与光催化性能的影响*赵宗彦 柳清菊朱忠其 张 瑾(云南大学,云南省高校纳米材料与技术重点实验室,昆明 650091)(2007年10月29日收到;2007年12月3日收到修改稿)采用基于第一性原理的平面波超软赝势方法研究了掺杂不同价态S 的锐钛矿相TiO 2的晶体结构、杂质形成能、电子结构及光学性质.计算结果表明硫在掺杂体系中的存在形态与实验中的制备条件有关;掺杂后晶格发生畸变、原子间的键长及原子的电荷量也发生了变化,导致晶体中的八面体偶极矩增大;S 3p 态与O 2p 态、T i 3d 态杂化而使导带位置下移、价带位置上移及价带宽化,从而导致TiO 2的禁带宽度变窄、光吸收曲线红移到可见光区.这些结果很好地解释了S 掺杂锐钛矿相TiO 2在可见光下具有优良的光催化性能的内在原因.根据计算结果分析比较了硫以不同离子价态掺杂对锐钛矿相T i O 2电子结构和光催化性能影响的差别.关键词:锐钛矿相TiO 2,S 掺杂,第一性原理,光催化性能PACC :7115M ,7115H,7115A*教育部新世纪优秀人才支持计划(批准号:NCET 04 0915),教育部科学技术研究重点项目(批准号:205147)和云南省自然科学基金(批准号:2005E0007M)资助的课题. 通讯联系人.E mail:qjliu@1 引言自从Fujishima 等人[1]发现受紫外光照射的TiO 2具有光催化效应以来,以TiO 2为代表的光催化材料得到了广泛的研究.TiO 2本身具有良好的化学稳定性、抗磨损性、低成本和无毒等特性,因而广泛被应用于太阳能电池、污水及空气净化、自清洁涂层、抗菌、光解水制氢等领域[2 4].但是由于锐钛矿相TiO 2是一种宽禁带半导体,其禁带宽度为3 23e V,只有在紫外光( <383 8nm)的激发下才能显示出催化活性,而太阳光中紫外光能量仅占5%(可见光能量占45%),这严重限制了TiO 2应用的范围和规模.因此,如何有效地利用可见光是决定TiO 2光催化材料能否得到大规模应用的关键.近年来,为了提高纳米TiO 2的光催化性能、实现TiO 2的可见光响应,研究者发现用非金属离子掺杂来改性TiO 2的新方法,如N [5],C [6],I [7]等.非金属元素的掺杂一般是用非金属元素取代TiO 2中的部分氧,形成TiO 2-x A x (A 代表非金属元素)晶体,由于O 的2p 轨道和非金属中能级与其能量接近的p 轨道杂化后使价带宽化,禁带宽度会相应减小,从而拓宽了TiO 2的光响应范围.Asahi 等人[5]采用第一性原理计算了F,N,C,S,P 取代锐钛矿相TiO 2中的O 的掺杂,结果表明N 取代掺杂最有效,同时他们认为S 原子的掺杂可以使TiO 2带隙变窄,但由于S 离子(S 2-)半径太大,不可能在Ti O 间隙或者取代TiO 2中的O 产生掺杂.但随后的研究却表明,S 是可以掺入到TiO 2中的,其焦点问题是S 取代了O 还是取代了Ti.Umebayashi 等人[8]采用氧化退火TiS 2的方法制备了S 掺杂的锐钛矿相TiO 2,通过实验推断认为微量的S 以阴离子S 2-进入到TiO 2晶格中取代O 2-而形成TiO 2-x S x 晶体,使TiO 2的带隙变窄,从而在可见光激发下具有光催化活性.周武艺等人[9]采用酸催化溶胶 凝胶法制备了S 掺杂TiO 2粉末,发现在热处理过程中S 由S 2-被氧化为S4+并进入TiO 2晶格中取代了部分Ti 4+位,导致了晶格畸变,带隙变窄,从而导致对光的吸收发生了向可见光区移动.而Ohno 等人[10]用硫脲与异丙醇钛反应制备了掺硫TiO 2,通过XPS 测试发现S 以S4+的价态形式掺入锐钛矿相TiO 2中,在波长大于500nm 的可见光区表现出更强的光吸第57卷第6期2008年6月1000 3290 2008 57(06) 3760 09物 理 学 报AC TA PHYSIC A SINICAVol.57,No.6,June,20082008Chin.Phys.Soc.收能力和更高的光催化活性.图1 S 以不同离子价态掺杂的超晶胞模型示意图 (a)锐钛矿相Ti O 2正格矢晶胞模型;(b)S 2-掺杂;(c)S 4+掺杂;(d)S 2-+S 4+掺杂由于样品制备采用的工艺流程和实验条件各不相同,而且影响TiO 2光催化性能的因素又极其复杂,同时由于缺少S 元素对TiO 2电子结构影响的详细研究,从而导致对S 掺杂改性的机理说法不一.与实验研究相比,利用计算机模拟计算可以克服实验研究中各种不利因素的影响、突出主要矛盾,更有利于研究掺杂元素对体系电子结构和光学性质的影响,近年来一些研究者已开始了这方面的研究工作[11,12].为了进一步深入分析S 掺杂锐钛矿相TiO 2的微观机理,澄清不同离子价态的S 掺杂锐钛矿相TiO 2光催化性能影响的差别,本文采用基于第一性原理的超软赝势方法计算了S 以不同离子价态掺杂锐钛矿相TiO 2的超晶胞模型的晶体结构,然后在结构优化的基础上计算杂质形成能、电子结构和光学性质,基于这些结果比较并解释了S 的不同离子价态掺杂对锐钛矿相TiO 2光催化活性改变的差别及原因.2.计算模型与方法本文中所考虑的锐钛矿相TiO 2的正格矢晶胞及掺杂的超晶胞模型如图1所示.锐钛矿相TiO 2属四方晶系(I 41 amd ,D 194h ),一个晶胞中含有两个Ti 原子和四个O 原子,S2-(S 4+)掺杂的2 1 1超晶胞模型中分别有一个O 原子被S 2-所取代或一个Ti 原子被S 4+所取代(分别标记为S 2-掺杂、S 4+掺杂),而S 2-,S 4+共掺杂的2 1 2超晶胞模型中各有一37616期赵宗彦等:S 掺杂对锐钛矿相TiO 2电子结构与光催化性能的影响个O原子和Ti原子分别被S2-,S4+所取代(标记为S2-+S4+掺杂),离子掺杂的原子数分数大约为4 17%.本文应用Accelrys公司开发的Ma terials Studio 3 2中的C ASTEP模块进行计算.C ASTEP是一个基于密度泛函理论的从头算量子力学程序,利用总能量平面波赝势方法,将离子势用赝势代替,电子波函数通过平面波基组展开,电子 电子相互作用的交换关联能由局域密度近似或广义梯度近似进行校正,它是目前较为准确的电子结构计算的理论计算方法[13].计算中所考虑的价电子分布分别是Ti: 3s23p63d24s2,O:2s22p4,S:3s23p4.价电子平面波函数的截断能设置为380eV.交换关联能应用局域密度近似中的CA PZ函数[14,15].所有的计算均在倒易空间中进行表示,这样可以同时提高计算的效率和精度.对不可约布里渊区的积分计算采用373的Monkorst park特殊k点进行取样求和,快速傅里叶变换的网格设置为452454,迭代过程中的收敛标准设置为:原子位移不大于510-5nm,原子间作用力不大于0 1eV nm,原子间的内应力不大于0 02GPa,体系总能量的变化不大于510-6eV atom.为了得到稳定精确的计算结果,先根据能量最小化原理得到合适的晶格常数,并优化其内坐标,然后在此基础上进行电子结构和光学性质的计算.在光学性质的计算中采用非极化多晶模型,并使!剪刀算符∀对结果进行修正,以便于与实验数据进行比较.3.结果与讨论3 1 晶体结构纯锐钛矿相TiO2经过结构优化后,得到的晶格常数为a=b=0 37436nm,c=0 94779nm,d ap= 0 19695nm,d eq=0 19138nm,2 =155 917#.这与实验测量的结果[16]:a=b=0 37848nm,c= 0 95124nm,d ap=0 19799nm,d eq=0 19338nm,2 =156 230#非常接近,说明采用的计算方法是合理的.杂质形成能通常被用作分析比较不同掺杂方式的相对难易程度,杂质形成能E f的定义[17]为E f=E TiO2:S-E TiO2-k8E S8+m2E Ti2+n2E O2,(1)其中E TiO2:S是掺S后的体系总能量,E TiO2是与掺杂体系相同大小的纯TiO2的超晶胞体系总能量,E S8,E Ti2,E O2分别是单质硫分子、钛分子及氧分子的能量,k,m,n分别是掺杂体系中掺入的硫原子数及被取代的钛原子或氧原子数,得到结果如表1所示.从表1中可以看出,当硫以S2-价态取代O2-进行掺杂时E f最小,说明在制备S掺杂锐钛矿相TiO2的实验中,硫在体系中以S2-价态存在的概率最大,S2-与S4+共同存在时的E f稍大,而当S4+单独存在时的E f最大,说明在制备过程中,随着热处理温度的升高,体系中的硫元素逐渐由S2-价态氧化为S4+价态,而在这一过程中,两种价态离子在体系应当是同时存在的,文献[9]根据XPS检测得到的结果,认为在常温下硫是以S2-离子存在,没有被氧化,当样品经500∃热处理后,S2-离子被氧化而以S4+价态取代了Ti4+,本文的计算结果验证了这一实验结果.光催化反应是一个非常复杂的现象,包括光的吸收、载流子的激发和迁移、表面的氧化还原反应等过程.其中有三个关键因素:表面结构、对太阳光的吸收能力和光生载流子的量子产生效率.表面结构决定了光催化剂的吸附能力与分解速度.半导体的光学性质主要决定于其电子结构,因此研究S掺杂体系的电子结构与光学性质的关系可以发现其对TiO2光吸收能力的影响,下面将重点讨论这方面的内容.光生载流子产生后,在从内部向表面的迁移过程中,将会发生电子-空穴对的复合,复合概率的大小一方面与杂质能级有关,另一方面与晶体结构密切相关:Sato等人[18]曾报道,由偶极矩产生的局域内电场有利于光生电子 空穴对的分离,从而可提高光催化剂的光催化活性.表1中同时列出了结构优化后掺杂体系的晶格畸变、平均键长、由Mulliken布居分析得到的平均净电荷以及八面体偶极矩.由表中的晶格体积变化可知,当硫以S2-价态存在时,晶格发生膨胀,而以S4+价态存在时,晶格发生收缩,这一变化与文献[9]报道的实验结果是一致的.导致这一变化的原因主要有:一是离子半径差异所导致,S2-离子半径(0 184nm)大于O2-的离子半径(0 132nm),而S4+离子半径(0 037nm)小于Ti4+离子半径(0 068nm);二是掺入S后,由于原子间的相互作用力发生了变化而使原子间的键长也随之变化,在计算中我们发现Ti O键的平均键长都趋于增大,而3762物 理 学 报57卷Ti S键的平均键长大于Ti O键的平均键长、S O键的平均键长则小于Ti O键的平均键长.由于掺杂后晶格发生了畸变、原子间的键长及原子的电荷量都发生了变化,这就意味着掺杂后八面体中负电荷的中心不再与Ti4+离子重合,从而偶极矩不再为零.从表1中可以看到掺杂后体系中TiO6八面体的偶极矩发生一定程度的变化,其中当有两种形式的掺杂共存时的变化尤为明显;其他类型的八面体(TiO5S,SO6)由于离子形态与电荷变化突出,从而使偶极矩的变化更为明显,同样也是当有两种形式的掺杂共存时的变化尤为明显.由于S掺杂后体系的偶极矩发生的变化,使TiO2的光生电子-空穴对分离更有效,降低了其复合概率,导致S掺杂锐钛矿相TiO2的光催化性能有了明显的提高,这与近期文献[8 10]报道的实验结果是基本一致的.如果在实验能够实现硫以两种离子形态分别取代O及Ti的共掺杂,将会极大地提高锐钛矿相TiO2的光催化性能.表1 结构优化后得到的杂质形成能、平均键长、晶格畸变、平均净电荷和平均偶极矩E f eV平均键长 nmTi O Ti S S OV nm3平均净电荷 e平均偶极矩 3 3356410-30C%mTi O S TiO6TiO5S SO6TiO20 19361 280-0 6400 000S2-掺杂-2 6470 19540 22450 01131 226-0 635-0 3100 1003 531S4+掺杂0 5350 19430 1904-0 001261 299-0 6551 4000 0300 223S2-+S4+掺杂-2 3930 19540 22490 19380 006771 259-0 645-0 3201 4500 3595 6830 3393 2 电子结构为了分析S掺杂对TiO2电子结构的影响,我们在结构优化的基础上计算了掺S的TiO2的能带结构和态密度.为了进行对比,我们将纯TiO2的第一布里渊区沿对称方向的K点取样设置为与掺杂后的体系是一致的.在计算中所考虑的禁带宽度是从价带最高点(valence band maximum,简称VBM)到导带最低点(conduction band minimum,简称CB M)之间的距离,计算得到的纯锐钛矿相TiO2的禁带宽度为2 68eV,小于实验测量值3 23eV,这是由密度泛函理论本身的缺陷的造成的,即在其理论框架中没有考虑交换 关联势的不连续性,从而使半导体和绝缘体的带隙的理论计算值一般要小于实验值[19].图2是纯锐钛矿相TiO2,S2-掺杂,S4+掺杂体系211超晶胞第一布里渊区带隙附近的能带结构图,掺杂后由于晶体对称性的降低,导致能级简并度下降,从而使能级产生了分裂.当硫以S2-价态存在时,在价带顶上方产生两个杂质能级,禁带宽度减小到2 37eV,由于与价带顶的距离较小而使其成为浅受主能级,这种形式的杂质能级可以成为电子的俘获中心,对光生电子 空穴对的分离是非常有利的.当硫以S4+价态存在时,在价带顶上方产生一个分布范围很大的杂质能级,禁带宽度减小到2 54e V.为了更清楚地理解S掺杂对TiO2电子结构的影响,在图3中我们给出了带隙附近未经平滑处理的体系态密度图以及各原子的分波态密度图.当硫以S2-价态存在时,杂质能级是由O2p态、Ti3d态与S2p态杂化形成,而且杂质能级的峰强很大,即电子在其上的存在概率很大,这样杂质能级中的电子不但只需较小的光子能量便可跃迁到导带中,而且可以作为中间能级使价带中的电子先跃迁到杂质能级中,再吸收能量较小的光子便可再次跃迁到导带,这样就可以吸收波长较长的光子,使TiO2能够充分吸收可见光,这对于实现锐钛矿相TiO2的可见光化是非常有效的.而当硫以S4+价态存在时,杂质能级主要是由O2p态与Ti3d态杂化形成,S2p态对其基本没有贡献,因此可以认为杂质能级是由于晶体的对称性改变而由原来的能级分裂形成的.由于杂质能级处于禁带中间,这种形式的杂质能级在掺杂浓度较大时,极易成为电子-空穴对的复合中心,因此在实验中应当控制掺杂浓度以避免形成复合中心.当体系中两种离子同时存在时,虽然禁带宽度减小为2 25e V,但由于在导带底只有几个很小的峰,电子占据这些能量范围的概率很小,而只有到了能量大于0 75eV时,电子才有较大的占据概率,这时到价带顶的距离为2 51eV.在图4中,我们给出了各体系总态密度和禁带宽度的变化情况.从图4中可以看出各体系的导带与价带主要由O2p态与Ti3d态组成,而S2p态主要与O2p态杂化形成杂质能级.从图中可以看出掺杂后,导带及价带位置有明显的改变,而且价带宽度37636期赵宗彦等:S掺杂对锐钛矿相TiO2电子结构与光催化性能的影响图2 计算得到2 1 1超晶胞第一布里渊区带隙附近的能带结构图 (a)纯锐钛矿相TiO 2;(b)S 2-掺杂;(c)S 4+掺杂图3 计算得到S 掺杂锐钛矿相Ti O 2带隙附近的分波态密度图 (a)S 2-掺杂;(b)S 4+掺杂;(c)S 2-+S 4+掺杂3764物 理 学 报57卷有一定的增大,这些原因使掺杂体系的禁带宽度有了一定的减小.在含有S4+的体系中,S 2p 态参与形成的杂质能级位于价带下方,这对于TiO 2光催化性的改变没有很大的影响.与纯锐钛矿相TiO 2的态密度图相比,掺杂体系中价带与导带中的峰形明显平滑变宽而形成一个连续体,这说明掺杂后电子的非局域性更明显,这是由晶体对称性的降低所导致的.从图4中可以看到当体系中同时含有硫的两种价态离子时,禁带宽度减小到2 25eV,其掺杂的效果相当于两者单独掺杂效果的总和,同时具有两者的优点.图4 计算得到S 以不同价态掺杂锐钛矿相TiO 2的总态密度图对光生电子 空穴对来说,电荷迁移的速率和概率及其光催化反应的能力,取决于各个导带和价带边的位置及吸附物种的氧化还原电势.热力学允许的光催化氧化-还原反应,要求受体电势比TiO 2导带电势低(更正),给体电势比TiO 2价带电势高(更负),这样半导体被激发产生的光生电子或光生空穴才能给基态的吸附分子[20].为了进一步分析S 掺杂对TiO 2光催化性能的影响,我们采用如下的公式来计算体系的带边位置(相对于标准电极电位的氧化还原势)[21]:E CB =X -E e-0 5E g ,(2)其中,E CB 是导带边的氧化还原电势,X 是组成半导体体系各原子电负性的几何平均值,E e是自由电子以氢为标准时的电势(~4 5eV),E g 采用的是经过剪刀算符修正的体系带隙值.利用这一表达式,我们得了纯TiO 2导带带边的氧化还原电势为-0 303e V,由此可以得到其价带带边的氧化还原电势为2 927eV.这一计算结果与文献[20]中所示的带边位置是一致的.采用这一表达式,表2中给出了S 掺杂后TiO 2的带边位置的变化情况,众所周知,H 2O 2和O 3是很强的氧化剂,它们的氧化电势分别是1 77,2 07eV.因此相对而言,S 掺杂的TiO 2具有很强的氧化还原性.由于带隙的减小,掺杂后体系的导带带边位置有轻微的下移、而价带带边位置则有一定的上移,即光生电子 空穴对还原氧化能力稍有降低,其中在含有S 4+的体系,其价带带边位置有轻微的下移,也就是说S 4+有利于增强TiO 2的氧化能力.表2 S 掺杂后Ti O 2的带边位置的变化情况E g (计算值) eV E g (修正值) e V E CB eVE VB eV Ti O 22 683 23-0 3032 927S 2-掺杂2 372 92-0 1952 725S 4+掺杂2 543 09-0 0893 001S 2-+S 4+掺杂2 252 80-0 0402 7603 3 光学性质C ASTEP 中光学性质的计算是利用电偶极子近似(electric dipole approximation)进行的,从量子力学的观点看,带间跃迁光吸收过程是电子在辐射电磁场微扰作用下从低能占据态到高能未占据态之间的跃迁过程.根据费米黄金定律,可以从直接跃迁概率的定义推导出介电函数的虚部!2,即!2(q &O u ,∀#)=2e 2∃%!0∋K ,V,C|(&C K |u %r |&V K )|2 ∋(E CK -E VK -E ),(3)式中u 是入射电场的极化方向矢量,C,V 分别表示导带和价带,K 为倒格矢,(&CK |u %r |&VK )为动量跃迁矩阵.E CK ,E VK 分别为导带和价带上的本征能级.由于电子结构中无论是带间跃迁还是带内跃迁的频率都远超过声子频率,在计算中仅考虑了电子跃迁,故介电函数可以表述为线性响应函数,而介电函数的实部与虚部之间可以通过Kramers Kronig 变换相联系,即通过这一关系可以得到介电函数的实部!1.同时从介电函数的虚部出发可以推导出复折射率、吸收率、反射率等光学常数.因此介电函数的虚部!2反映了能级间电子跃迁所产生的光谱机理,从某种意义上说,介电响应函数比宏观光学常数更能表征材料的物理特性,更易于和物理过程的微观模型及固体的微观电子结构联系起来.图5是掺杂体系未经修正的介电函数虚部!237656期赵宗彦等:S 掺杂对锐钛矿相TiO 2电子结构与光催化性能的影响作为光子能量函数的谱图.介电峰位的分布与电子结构直接相关,即与电子从价带到导带的跃迁过程相关联,但不能将介电峰简单的理解为两个能级之差,因为在电子吸收光子能量而发生跃迁的过程中应考虑弛豫效应,而且多个能级之间的跃迁会对同一介电峰同时有贡献,故而二者是有一定的偏差.从图中可以看到S 掺杂后,体系的介电虚部!2值均向低能方向移动,即使体系的光波吸收阈值产生红移.由于在光子能量大于2 25e V 的介电峰是由价带电子向导带跃迁产生的,这使TiO 2在实现可见光吸收的同时保持了优异的光催化性能.因此硫以S 2-价态形式掺杂时对于提高锐钛矿相TiO 2的可见光光催化性能是有利的.在光子能量低于2 25eV 的介电峰,主要是由杂质能级上的电子向导带中跃迁产生的.在实现锐钛矿相TiO 2可见光化的实验中,由于这些杂质能级的存在,可以使价带电子可以先激发到这些杂质能级上,然后再次吸收光子能量跃迁到导带上,这样也可以拓展TiO 2光吸收的范围.但由于电子占据这些杂质能级的相对概率较小,它们所提供的贡献是很有限的.图5 计算得到S 掺杂锐钛矿相TiO 2的介电函数虚部!2与入射光子能量的关系图为了与文献报道的实验结果进行对比,图6给出了经过!剪刀算符∀修正作为光波波长函数的光吸收系数图谱.从图中可以看出纯TiO 2的光吸收曲线与文献报道的实验值相当吻合,其起始吸收带边位于390nm 附近.这说明对光学性质的计算结果进行修正是有必要和合理的.掺杂后光波吸收系数曲线有了明显红移,在波长小于440nm 的基本吸收带中,S 2-掺杂对TiO 2光吸收有较大的红移效应,这是由于禁带宽度的减小所导致的.而S4+掺杂对TiO 2光吸收的改变主要体现在波长大于400nm 附近的范围内,这是由杂质能级参与产生的.而S2-与S4+共掺杂的红移效果不如S 4+掺杂明显,这是因为电子占据导带底的概率很小所致.对照上文所分析电子结构的变化可以看出,掺杂后体系的光学性质的变化是与其电子结构的变化对应的.图6 计算得到S 掺杂锐钛矿相TiO 2的光吸收系数与入射光波长的关系图4.结 论本文采用第一性原理的平面波超软赝势方法计算了掺杂不同S 离子价态的锐钛矿相TiO 2的晶体结构、电子结构、杂质形成能和光学性质,分析了S 掺杂对锐钛矿相TiO 2的晶体结构、电子结构和光学性质的影响,在此基础上,研究了S 掺杂对锐钛矿相TiO 2在可见光下的光催化性能的影响.基于这些结果,我们得出如下结论:1 硫元素在掺杂体系中的存在形态与实验中的制备条件有关,其中以S2-掺杂的杂质形成能最小,在实验中最有可能形成,随处理温度的升高部分S 2-会被氧化为S 4+.掺杂后晶格发生畸变、原子间的键长及原子的电荷量也发生了变化,导致体系中的八面体偶极矩增大,从而有利于光生电子-空穴对的分离、提高TiO 2的光催化活性.2 硫以S2-掺杂时杂质能级位于价带上方形成浅受主能级,禁带宽度变化较大,而以S 4+掺杂时杂质能级主要位于价带下方,禁带宽度变化较小;电子结构的变化导致TiO 2光学性质的变化,掺杂后的介电函数虚部向低能方向移动,而光吸收系数则红移至可见光区.3766物 理 学 报57卷3 综合分析比较计算结果,可以认为当硫以S2-掺杂更有利于TiO2在可见光下光催化性能的提高,如果在实验能实现S2-和S4+两种价态离子的共掺杂锐钛矿相TiO2,将会极大地提高TiO2的光催化性能.感谢云南大学高性能计算中心在模拟计算方面提供的技术支持与帮助.[1]Fuji shi ma A,Honda K1972Nature23837[2]Dhananjay S B,Vishwas G P,Anthony A B2001J.Che m.Tech.Biot.77102[3]Jing L Q,Sun X J,Shang J2003Sol.Ene r.Mate r.Sol.Cells79133[4]J uan Z,Xu D Y2003Building and Environment38645[5]As ahi R,Morika wa T,Ohwakl T2001Sc ienc e293269[6]Irie H,Watanabe Y,Hashimoto K2003Chem.L e tt.32772[7]Hong X T,Wang Z P,Cai W M2005Che m.M ater.171548[8]Umebayashi T,Yamaki T,Tanaka S2003Chem.Lett.32330[9]Zhou W Y,Cao Q Y,Tang S Q2006J.Inor.Mater.21776(i nChinese)[周武艺、曹庆云、唐绍裘2006无机材料学报21776] [10]Ohno T,Akiyoshi M,Umebayashi T2004Appl.Catal.A:General265115[11]Du J,Ji Z G2007Acta Phys.Sin.562388(in Chinese)[杜娟、季振国2007物理学报562388][12]Zhao Z Y,Li u Q J,Zhang J,Zhu Z Q2007Ac ta Phys.Sin.566592(in Chinese)[赵宗彦、柳清菊、张 瑾、朱忠其2007物理学报566592][13]Segall M D,Philip J D L2002J.Phys.:Dondens.Matte r.142717[14]Ceperley D M,Alder B J1980Phys.Rev.Lett.45566[15]Perdew J P,Zunger A1981Phy.Rev.B235048[16]Burdett J K,Hughbanks T1987J.Am.Che m.Soc.1093639[17]Cui X Y,Medvedeva J E,Delley B,Freeman A J,Ne wman N,Stampfl C2005Phys.Re v.Lett.9525604[18]Sato J,Kobayas hi H,Inoue Y2003J.Phys.Chem.B1077970[19]John P P,Mel L1983Phys.Rev.Lett.511884[20]Amy L L,Guangquan L,J ohn T Y Jr1995Che m.Rev.95735[21]Junwan T,Jinhua Y2005Che m.Phys.Lett.41010437676期赵宗彦等:S掺杂对锐钛矿相TiO2电子结构与光催化性能的影响3768物 理 学 报57卷Effects of S doping on electronic structures andphotocatalytic properties of anatase TiO2*Zhao Zong Yan Liu Qing Ju Zhu Zhong Qi Zhang Jin(Y unn an K e y Laboralory o f Nan oma terials a nd Nan otechn ology,Yun nan Un ive rsity,Kun min g 650091,China)(Recei ved29October2007;re vised manu scrip t received3December2007)AbstractThe crystal structure,impurity formation ene rgy,electronic structure and optical prope rties of ana tase Ti O2doped with sulfur in diffe rent valence states were studied by using the plane wave ultra soft pse udopotential method based on first principles. The calculations shown that the e xistence form of sulfur element in ana tase T i O2was rela ted to the experimental c onditions;the oc tahedral dipole moments were increased due to the cha nges of lattice parame ters,bond length and charges on ato ms;the band gap narrowed and the curves of light absorption red shifted to visible light region due to the position of conduction band do wnward shift ing,the position of valence band upper shifting and the width of valence band broade ning re sult from hybridizing S3p state s with O2p sta tes and Ti3d sta tes.All of these results can e xplain the better photoca talytic propertie s of S doped anatase TiO2in visible light re gion.Acc ording to these results,the effects on elec tronic struc tures and photocatalytic properties of anatase TiO2 doping with different valence state s of sulfur were compared and analyzed.Keywords:anatase TiO2,S doped,first principles,photocatalytic propertiesPACC:7115M,7115H,7115A*Project supported by the Program for the Ne w Century Excellent Talents in University of Minis try of Education,China(Grant No.NCET 04 0915),the Foundati on for Key Program of Minis try of Educati on,China(Grant No.205147)and the Natural Science Foundation of Yunnan Province,Chi na(Grant No.2005E0007M).Correspondi ng author.E mail:qjliu@。
La 3+掺杂对(Sr,Ba,Ca)TiO3基压敏陶瓷结构和性能的影响

关键 词 : ( rB 。 a Ti 。 压敏 陶瓷 ; a 掺 杂 ; S 。aC ) O 基 L件 结
构 : 性 能 电
C 。和 AS 以及 不 同含 量 的 L z , 组分 均为分 析 O T aO。各
. .
氛 中 8 0 ×2 5℃ h的条 件下 进行 热处理 以实 现晶 界层 绝 缘化 。
2 2 样 品 的 测 试 .
采 用 日本 R g k / x型 X 射 线 衍 射 分 析 仪 ia u D Ma ( u ) J M一4 0 V 型 扫 描 电 子显 微 镜 对 还原 烧 C Ka 和 S 6 6 L
徐 宇兴 , 中太 , 子 龙 , 张 唐 李雄 佳
( 清华 大学 材 料 系新 型陶瓷 与精 细工艺 国家 重点 实验 室 , 京 1 0 8 ) 北 0 0 4
摘 要 : 采 用 常规 固相法制 备 ( rB , a Ti 基 压 S , a C ) O。
敏 陶 瓷 。 用 Nb叶离子 取 代 T ” 离子 , n作 受 主 掺 杂 。 i M 元 素 的 前 提 下 , 统研 究 了稀 土 离子 L 。 施 主 掺 杂 对 系 a叶 。 压敏 陶瓷 结构 和 性 能 的 影 响 。结 果 表 明 , L z 。 当 aO 一 0 4 ( 尔分 数 ) , S , a C ) O . 摩 时 ( rB , a Ti 。基 压 敏 陶 瓷 可 获 得 良好 的 电性 能 : 压 敏 电 压 V 。A 1 . 9 非 线 其 1 一 1 1 V, 性 系数 口 2 9 , 容 C= 3 . 6 F 介 电 损 耗 tn = 一 .3 电 1 1n , as
2024_2025学年新教材高中化学期末检测含解析新人教版必修第一册
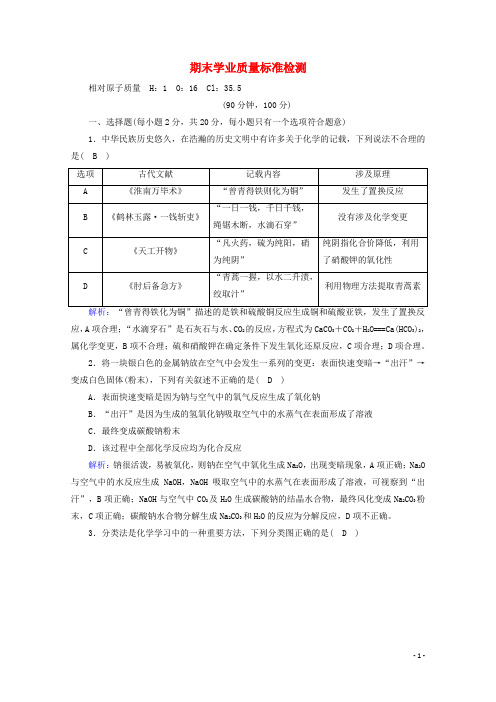
期末学业质量标准检测相对原子质量H:1 O:16 Cl:35.5(90分钟,100分)一、选择题(每小题2分,共20分,每小题只有一个选项符合题意)1.中华民族历史悠久,在浩瀚的历史文明中有许多关于化学的记载,下列说法不合理的是( B )应,A项合理;“水滴穿石”是石灰石与水、CO2的反应,方程式为CaCO3+CO2+H2O===Ca(HCO3)2,属化学变更,B项不合理;硫和硝酸钾在确定条件下发生氧化还原反应,C项合理;D项合理。
2.将一块银白色的金属钠放在空气中会发生一系列的变更:表面快速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是( D )A.表面快速变暗是因为钠与空气中的氧气反应生成了氧化钠B.“出汗”是因为生成的氢氧化钠吸取空气中的水蒸气在表面形成了溶液C.最终变成碳酸钠粉末D.该过程中全部化学反应均为化合反应解析:钠很活泼,易被氧化,则钠在空气中氧化生成Na2O,出现变暗现象,A项正确;Na2O 与空气中的水反应生成NaOH,NaOH吸取空气中的水蒸气在表面形成了溶液,可视察到“出汗”,B项正确;NaOH与空气中CO2及H2O生成碳酸钠的结晶水合物,最终风化变成Na2CO3粉末,C项正确;碳酸钠水合物分解生成Na2CO3和H2O的反应为分解反应,D项不正确。
3.分类法是化学学习中的一种重要方法,下列分类图正确的是( D )解析:氧化物包括酸性氧化物、碱性氧化物、两性氧化物(如Al2O3)、不成盐氧化物(如CO、NO)等,A项错误;少数非金属氧化物(如H2O、CO、NO等)不属于酸性氧化物,B项错误;有些离子反应是氧化还原反应,如Zn+2H+===Zn2++H2↑,C项错误;含两种或两种以上的物质是混合物,胶体由分散质和分散剂组成,胶体确定是混合物,D项正确。
4.确定温度和压强下,30 L某种气态纯净物中含有 6.02×1023个分子,这些分子由1.204×1024个原子组成。
《第一单元 化学反应速率》(同步训练)高中化学选择性必修1_苏教版_2024-2025学年

《第一单元化学反应速率》同步训练(答案在后面)一、单项选择题(本大题有16小题,每小题3分,共48分)1、在下列反应中,哪一个反应的速率最快?O2)(水解反应,较慢)A、(H2O2⇌H2O+12B、(Zn+H2SO4→ZnSO4+H2)(锌与稀硫酸反应,较快)C、(CaCO3+2HCl→CaCl2+H2O+CO2)(块状碳酸钙与稀盐酸反应,较慢)D、(Fe+CuSO4→FeSO4+Cu)(铁与硫酸铜反应,较快但可能较温和)2、在一定条件下,将二氧化氮(NO2)和水反应生成硝酸(HNO3)和一氧化氮(NO)的化学反应如下:[3NO2+H2O→2HNO3+NO]已知开始时,(container)A中NO2的浓度为0.3 mol/L,(container)B中H2O的浓度为0.4 mol/L,反应在恒容容器中进行。
下列说法正确的是:A. 该反应属于酸碱中和反应。
B. 该反应立即达到平衡状态。
C. 反应速率与NO2的浓度成正比。
D. 在反应过程中,容器A中NO2的浓度变化率与容器B中H2O的浓度变化率之比为3:4。
3、在一定条件下,将2.0 g某反应物放入一个密闭容器中,其分解反应的化学方程式为:2A → B + C。
经过一定时间后,测得容器内A的质量减少了1.0 g,此时容器内C的质量为1.2 g。
A、此时容器内B的质量为1.6 gB、此时容器内A的物质的量为0.8 molC、此时容器内C的物质的量浓度为0.6 mol/LD、若要使反应达到平衡,需增加A的浓度4、在恒温、恒容的密闭容器中进行反应:(A(g) + 2B(g) ⇌ 2C(g)),下列各项能说明该反应一定处于平衡状态的是()A. 容器内压强不再变化B. 气体A和B的浓度相等C. 正反应和逆反应速率均为零D. 气体C的生成速率是气体B的生成速率的1.5倍5、在下列化学反应中,反应速率最快的是:A. 2H₂ + O₂ → 2H₂O(在。
——温度条件下)B. CH₄ + 2O₂ → CO₂ + 2H₂O(在。
改性(Sr,Ca)TiO_(3)基储能陶瓷介电及MLCC性能研究

改性(Sr,Ca)TiO_(3)基储能陶瓷介电及MLCC性能研究陈永虹;林志盛;张子山;陈本夏;王根水【期刊名称】《无机材料学报》【年(卷),期】2022(37)9【摘要】工业级脉冲储能多层瓷介电容器(MLCC)是现阶段国内研制和生产电子启动装置的重要元器件,针对国内主要有机薄膜电容器尺寸大、寿命短、可靠性较低的不足,本研究采用传统固相反应法,制备了SrTiO_(3)和CaTiO_(3)基的脉冲储能介质陶瓷材料,研究了微量助烧剂掺杂,以及Sr^(2+)/Ca^(2+)相互掺杂对陶瓷材料的介电性能的影响,并进一步制备和研究了以(Sr,Ca)Ti O_(3)为基体MLCC性能。
实验结果表明:通过加入质量分数1.0%的助烧剂,引入微量Bi^(3+)可取代Sr^(2+),提高了SrTiO_(3)材料的介电常数,而Bi^(3+)对CaTiO_(3)基材料的介电性能无明显影响;Mn元素有效抑制高温烧结中Ti^(4+)的还原,降低介电损耗;加入助烧剂有效降低瓷粉的烧结温度,提高材料的致密性。
(Sr_(x)Ca_(1-x))TiO_(3)体系的MLCC 可保持较高的介电常数和较低的介电损耗,当x=0.4时,其介电损耗tanδ=1.8×10^(–4),击穿强度为59.38 V/μm,高低温放电电流变化率为±7%,放电稳定,在常温和高温(125℃)下经1000次循环充放电实验均未失效,是一种在不同电场强度下具有相对较优的容量稳定性以及较高可靠性的脉冲特性(Sr,Ca)TiO_(3)基电容器陶瓷介质材料。
【总页数】7页(P976-982)【作者】陈永虹;林志盛;张子山;陈本夏;王根水【作者单位】福建火炬电子科技股份有限公司;中国科学院上海硅酸盐研究所【正文语种】中文【中图分类】TQ174【相关文献】1.钴钇掺杂(Ba,Sr)TiO3基介电陶瓷的制备与性能研究2.B位(Mg1/3Ta2/3)4+置换对新型Sr基(Sr,Nd,Ca)TiO3微波陶瓷结构及介电性能的影响3.Bi2O3掺杂Sr0.92Ca0.08TiO3基陶瓷结构与介电性能的研究人工晶体中的“非主流”——有机晶体4.Sr^(2+)置换改性Ca_(0.25)(Li_(1/2)Sm_(1/2))_(0.75)TiO_3陶瓷的微波介电性能研究5.外延Ba_(0.5)Sr_(0.5)TiO_(3)薄膜铁电介电性能的厚度依赖性研究因版权原因,仅展示原文概要,查看原文内容请购买。
掺铟对(Bi0.5Na0.5)0.93Ba0.07TiO3压电陶瓷的影响

GUo i n y ng , J a 。 o 。 CHAI Liyng -i 。
( . S h o fM a e il in ea d En i e rn n y La . o r o lc rca d Pi o l c rcM a e i l n v c s o 1 c o lo t ra sSce c n g n e i g a d Ke b fFe r e e ti n e e e ti t ra s a d De ie f Hu iPr v n e he o i c ,Hu e n v r iy,W u n 4 0 6 hi U i e st ha 3 0 2,Ch n i a;2 S h o fPh sc n e t o i c n l g . c o lo y is a d El c r n c Te h o o y,Hu e n v r iy, hi U i e st
Ab ta t B o5 o ) 3 a 7 O3 pe o lc rcc r misd p d wi n r t d e .X— a i r t n p t sr c :( i o o Na 5 9 B 0 Ti iz e e t i e a c o e t I 2 we e su i h O3 d rydf ai a— f o t r ss o d t a NB c r mis d p d wih p o e mo n fI 2 x i i d a sn l p a e o e o s i tu — e n h we h tB T e a c o e t r p ra u to n e h b t i g e h s fp r v k t s r c O3 e e t r .Th a t r s as e e ld t a h mo n fr o o e r lp a e e r a e n h mo n ft t a o a ue e p t e n lo r v a e h t t e a u to h mb h d a h s s d c e s d a d t e a u to e r g n l p a e n r a e n t emo p o r pc p a eb u d r .W i o ig p o e mo n fI 2 ,t eg a n s eo h e h s s i c e s d i h r h t o i h s o n a y t d p n r p ra u to n h O3 h r i i f ec — z t r mis wa n i ie n o g nz d,a h wn b c n i g e e t o c o c p . W h n t e a u to n s a c s i h b t d a d h mo e ie ss o y s a n n l c r n mir s o y e h mo n fI z wa 03 0 1 ,t e ( i 5 o ) 3 a o7 Ti e a c rsn e p i lpeo lcrcp o ete .6 h B 0 Na 5 0 B o 9 O3c rmisp e e td o t ma iz eeti r p ris:k 一 0 5 s 一 2 5 p . ,d a 0 C/
bi离子掺杂对钙钛矿太阳能电池的应用

近年来,随着太阳能电池技术的不断发展,钙钛矿太阳能电池因其优良的光电转换性能和低成本而备受关注。
而其中一项重要的研究内容便是对钙钛矿太阳能电池进行离子掺杂,以提高其性能和稳定性。
在本文中,我们将对bi离子掺杂对钙钛矿太阳能电池的应用进行深入探讨。
一、bi离子的掺杂原理1. bi离子的特性bi(铋)离子是一种具有多种价态的稀有金属离子,常见的价态为Bi3+和Bi5+。
Bi3+被认为是一种优良的p型掺杂剂,可以有效提高钙钛矿太阳能电池的光电性能。
2. bi离子的掺杂原理通过向钙钛矿材料中引入bi离子,可以改变其晶格结构和能带结构,从而影响其光电性能。
bi离子的掺杂还可以影响钙钛矿材料的导电性和载流子传输性能,进而提高太阳能电池的性能和稳定性。
二、bi离子掺杂对钙钛矿太阳能电池的影响1. 光电性能的提高通过掺杂bi离子,可以扩展钙钛矿太阳能电池的光吸收范围,提高光电转换效率。
bi离子的掺杂还可以减小钙钛矿材料的带隙,增加光生载流子的寿命,从而提高太阳能电池的光电性能。
2. 稳定性的改善钙钛矿太阳能电池在长时间的工作过程中往往会受到环境和光热条件的影响,导致性能的逐渐下降。
而bi离子的掺杂可以提高钙钛矿材料的稳定性,减少因光热或湿气等外界条件导致的性能衰减,从而延长太阳能电池的使用寿命。
三、bi离子掺杂在钙钛矿太阳能电池中的应用前景1. 实验结果许多实验结果表明,通过掺杂bi离子,可以显著提高钙钛矿太阳能电池的光电转换效率和稳定性。
部分实验表明,在掺杂适量的bi离子后,钙钛矿太阳能电池的光电转换效率可以提高到20以上,且在高温或潮湿条件下仍能保持较高的稳定性。
2. 应用前景随着对太阳能电池性能和稳定性要求的不断提高,bi离子掺杂已经成为一种备受关注的提高钙钛矿太阳能电池性能的重要手段。
未来,通过进一步优化bi离子掺杂的方法和实验条件,钙钛矿太阳能电池有望实现更高的光电转换效率和更长的使用寿命,从而更好地满足清洁能源市场的需求。
3.3非化学计量化合物

材料科学基础第 3 章由于化学组成上偏离化学计量而产生的缺陷四种类型 非化学计量化合物阴离子缺位型 TiO 2-X阳离子填隙型 Zn 1+X O 阴离子填隙型 UO 2+X 阳离子缺位型 Fe 1-X O阴离子缺位型产生原因环境中缺氧,晶格中的氧逸出到大气中,使晶体中出现了氧空位。
阴离子缺位型(TiO 2-x )缺氧的TiO 2可以看作是四价钛和三价钛氧化物的固溶体简化式中 e´=Ti Ti ´Ti 4+获得电子降为 Ti 3+三价钛占据四价钛的位置氧空位上束缚2个自由电子有缘学习更多驾卫星ygd3076或关注桃报:奉献教育(店铺)阴离子缺位型(TiO2-x)根据质量作用定律,平衡时:由晶体电中性条件:氧空位的浓度与氧分压的1/6次方成反比阴离子缺位型F-色心TiO2-x结构缺陷示意图色心由于电子补偿而引起的一种缺陷。
研究最详细的色心是F-色心(F-Center),由一个阴离子空位和一个在此位置上的电子组成。
因陷落电子能吸收一定波长的光而使材料出现某种颜色。
TiO2 在还原气氛下 黄色→灰黑色NaCl 在蒸气中加热 呈现黄棕色产生原因过剩金属离子进入间隙位置,带正电。
等价电子被束缚在间隙位置金属离子周围,形成一种色心。
间隙阳离子+电子为保持电中性e由于间隙阳离子使金属离子过剩型结构1+xZnO在锌蒸汽中加热,颜色会逐渐加深,就是形成这种缺陷的缘故。
与上述反应同时进行的还有氧化反应 :Zn(g) + 1/2O2 = ZnO1+x 平衡时 [Zn i ·]=[e´],得:根据质量作用定律:(单电荷间隙锌)锌不完全电离时1+x实测 650℃下ZnO电导率与氧分压的关系单电荷锌间隙模型的正确性产生原因•存在间隙阴离子使阴离子过剩。
为保持电中牲,结构中引入电子空穴,相应的阳离子升价。
•电子空穴在电场作用下会运动,材料为P型半导体。
h由于存在间隙阴离子,使阴离子过剩型结构阴离子填隙型( UO 2+x )随着氧分压的提高间隙氧浓度增大等价于目前只发现UO 2+x ,可看作铀氧化物间形成的固溶体。
晶体结构缺陷(一)非化学计量缺陷

知识点050 非化学计量缺陷的定义与分类非化学计量缺陷就是指非化学计量化合物中的缺陷,或由于组成偏离定比定律而产生的缺陷Fe1-x O中的缺陷是怎样的呢?Fe2O3 3FeO2Fe Fe.+ 3O O+ V Fe,,Fe 2O 3 3FeO 2Fe Fe . + 3O O + V Fe,, 2Fe Fe 2Fe Fe .+ O O + V Fe ,, O 2 + 1 22Fe Fe 2Fe Fe . + O O + V Fe,, O 2 + 1 2 2h .+ O O + V Fe ,, O 2 1 2 2Fe Fe + 2h .p 型半导体非整比化学计量化合物都是半导体,分类如下:这类缺陷的特点是:缺陷浓度与氧分压(气氛)有关p 型半导体 2h .+ O O + V Fe ,, O 2 1 2ZnO Zn i . + + O 2 1 2e , ZnOZn i .. + + O 2 1 2 2e ,n 型半导体V O .. + + O 2 2e , O O 1 2 n 型半导体O i ,, + O 2 2h. 1 2 p 型半导体有缘学习更多+谓ygd3076考证资料或关注桃报:奉献教育(店铺)随堂练习:答:ZnOZn i..+ + O 212 2e ,知识点051 非化学计量缺陷的浓度与物质性质缺陷浓度在恒温条件下会随气氛分压的变化而变化2h .+ O O + V Fe ,,O 2 121 2= [h ][h ] = exp G-3RT.2 1 62P O 氧分压升高, 电导率增大 。
2-ZnOZn i .+ + O 2 1 2 e ,氧分压升高, 电导率降低 。
2 2[e ] = exp G-2RT,P O 2 14-V O ..+ + O 2 2e ,O O1 2 氧分压升高, 电导率降低 。
[e ] = exp G-3RT,2P O 2 1 6- 2 2= [e ]1 有缘学习更多+谓ygd3076考证资料或关注桃报:奉献教育(店铺)O i ,,+ O 2 2h.1 21 2 = [h ][h ] = exp G-3RT. 2 162P O 氧分压升高,电导率增大 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
压电陶瓷作为一类重要的功能材料 ,在机械 、 电 子、 精密控制等领域有着广泛的应用 . 然而 , 目前实 用的压电陶瓷主要是以 Pb ( Ti ,Zr) O3 ( PZT) 为基的材 料 ,其中氧化铅约占原料总量 70 %左右 , 在材料的 制备过程中 ,铅的挥发会给环境带来很大的损害 ,因 而压电陶瓷无铅化或低铅化成为此类陶瓷发展的趋 势之一 ,以适应环境保护的要求 . 目前 ,无铅压电陶瓷材料主要有铌酸盐陶瓷 ( 如 Li x Na1 - x NbO3 陶瓷 ) 、 钛酸盐陶瓷 ( 如 BaTiO3 , Na1Π 2
A 位非化学计量可以提高陶瓷的压电性能 ; B 位掺杂对材料电学性能的影响规律类似于 Pb ( Ti ,Zr) O3 系压电陶瓷
的相关规律 ; 由于非化学计量和掺杂会影响到 A 位离子对 B 位离子与氧离子形成的 B O6 八面体的耦合作用 ,影响 到畴的稳定性 ,从而影响到 (Na1Π 2 Bi1Π 2 ) 0. 92 Ba0. 08 TiO3 陶瓷的去极化温度 ; 所研究的陶瓷样品的去极化温度越低 ,压电 系数越高 .
2 2 2 2 2 2 1Πd = ( h + k ) Πa + l Π c ,
由于四方相的 a 轴和 c 轴是不相等的 , 所以实际上 第一个衍射峰是 ( 100) 面和 ( 001) 面的衍射峰叠加而 成的
[9]
,只不过其他陶瓷样品 c 和 a 相差比较小 ,因
而没有出现明显的分峰现象 . X 射线衍射的结果表 明 B 位掺杂低价的钴提高了结构的畸变程度 ,这主 要是 由 于 掺 杂 形 成 的 氧 空 位 引 起 晶 胞 的 收 缩 和 歪曲
初宝进 李国荣 殷庆瑞 张望重 陈大任
( 中国科学院上海硅酸盐研究所 ,无机功能材料开放实验室 ,上海 200050) (2001 年 4 月 23 日收到 ;2001 年 5 月 13 日收到修改稿)
研究了非化学计量和掺杂对无铅压电陶瓷 (Na1Π 2 Bi1Π 2 ) 0. 92 Ba0. 08 TiO3 的压电性能及去极化温度的影响 . 研究发现
d33 减小 ,介电系数减小 , 损耗减小 , 这个规律与 PZT
图 2 ,3 分别是所研究样品的热激电流与温度的 关系曲线和介电系数2温度的关系曲线 ,相应的去极 化温度和介电峰值温度列于表 1 中 . 对于 NBBTCo 的介电系数与温度的关系曲线 , 我们发现在高温下 还存在另一个介电峰 , 这个介电峰可能是由于其他 弛豫过程引起的 ,其机理有待于进一步的研究 . 由于 此现象与本文所讨论的内容无太多的联系 , 故本文
Bi1Π 铋层状结构的压电陶瓷 ( 如 Bi4 Ti3 O12 2 TiO3 陶瓷) 、
2 实验过程
采用传统的氧化物合成法制备所需的压电陶瓷 样 品 . 以 化 学 纯 的 Na2 CO3 , Bi2 O3 , TiO2 , BaCO3 ,
Nb2 O5 ,Co2 O3 为原料 ,根据下面的化学式进行配料 ,
10 期
初宝进等 : 非化学计量和掺杂对 (Na1Π 2 Bi1Π 2 ) 0. 92 Ba0. 08 TiO3 陶瓷电性能的影响
2013
成 . 将获得的瓷坯磨片后烧渗银电极 , 然后在 80 ℃ 的硅油中施加 3 — 4kVΠ mm 的直流电场极化 . 极化后 的样品放置一昼夜后测量电学性能和热激电流 . 利 用由电容电桥和电炉组成的装置测量未极化样品的 介电系数2温度特性 .
关键词 : 无铅压电陶瓷 , 非化学计量 , 掺杂 , 电性能
PACC : 7760 , 7780B
与 BaTiO3 固溶 , 改善了纯 Na1Π 2 Bi1Π 2 TiO3 陶瓷矫顽场
1 引
言
高不易极化和不易烧结等缺点 . 研究比较后认为 ,相 界附近的 (Na1Π 2 Bi1Π 2 ) 0. 92 Ba0. 08 TiO3 陶瓷具有各项异性 大 ,频率常数比较高 , 压电系数比较大等特点 , 矫顽 场由原来的 7. 3kVΠ mm 降为 3. 2kVΠ mm , 是此系统中 综合性能较好的组分 . 针对此组分 ,本工作研究了 A 位非化学计量和 B 位掺杂对 ( Na1Π 2 Bi1Π 2 ) 0. 92 Ba0. 08 TiO3 陶瓷压电性能及退极化温度的影响 .
NBBT ,NBBT( 1 - x ) ,NBBT( 1 + x ) ,NBBTNb 和 NBBT2 Co. 将配好的生料以无水酒精为球磨介质 ,球磨混合
,它 们 被 认 为 是 一 类 很 有 前 途 的 无 铅 压 电
材料 . 我们曾详细研究了 Na1Π BaTiO3 陶瓷系 2 Bi1Π 2 TiO3 2 统相界附近压电陶瓷的性能
图2 Na 1Π BaTiO3 陶瓷的热激电流曲线 2 Bi 1Π 2 TiO32
对压电系数的影响是不确定的 . 从我们的实验结果 2+ 看 , A 位多加 (BiNa ) 有利于 90° 畴的转向 , 这种效 应起主要作用 , 提高了压电系数 . 至于 B 位掺杂对 压电系数的影响 , NBBT 陶瓷的 B 位掺杂高价的
第 50 卷 第 10 期 2001 年 10 月 100023290Π 2001Π 50 (10) Π 2012205
物 理 学 报
ACTA PHYSICA SINICA
Vol. 50 ,No. 10 ,October ,2001 ν 2001 Chin. Phys. Soc.
非化学计量和掺杂对( Na 1Π 2 Bi1Π 2 ) 0. 92 Ba 0. 08 TiO3 陶瓷电性能的影响
Nb 相当于软性添加物 , 而掺杂低价 Co
则相当于 硬性添加物 . 硬性添加物和软性添加物对 Pb ( Zr ,Ti ) 讨论 ,本文对此不再赘述 .
Cochran 认为
[11 ]
5+
3+
O3 压电陶瓷压电性能的影响规律已有比较成熟的 ,钙钛矿结构的 AB O3 铁电体可
以看成是由 B O6 八面体形成的网络结构 ,具有铁电 活性的 B O6 八面体是通过 B O6 八面体间的 A 位阳
陶瓷) 等 . Na1Π 2 Bi 1Π 2 TiO3 是一种 A 位复合取代的钙钛 矿型结构的铁电材料 ,在室温下它的剩余极化为 Pr μ = 38 mm , 具有很强的 CΠ cm ,矫顽场为 Ec = 7. 3kVΠ
2
基础配方为 ( Na1Π 2 Bi1Π 2 ) 0. 92 Ba0. 08 TiO3 ; A 位非化学计 量 的 配 方 为 ( Na1Π 2 Bi1Π 2 ) 0. 92 x
[8 ]
均匀 后 在 刚 玉 坩 埚 中 合 成 , 合 成 温 度 为 900 — 1000 ℃,保温时间为 2h. 所得的熟料球磨后加黏结 剂 ,压成直径为 15mm , 厚度为 1mm 的圆片素坯 . 素 坯在空气气氛中 ,1140 — 1190 ℃ 的温度下保温 1h 烧
, 通过 Na1Π 2 Bi1Π 2 TiO3
从图上可看到 , Tm 大约在 245 ℃ 附近的平台处 . 从 上述图表可看到 , 这些陶瓷中都存在去极化温度远
表1 Na 1Π BaTiO3 陶瓷的性质 2 Bi 1Π 2 TiO32
NBBT
d33 / pCΠ N
T ε ε 33Π 0
NBBT(1 - x ) 140 870 0. 0281 210 125
2014
物 理 学 报
50 卷
对此现象不作讨论 . 由于高温介电峰的存在 , 使得
Tm 并不明显 ,因此表中没有给出 NBBTCo 的 Tm 值 ,
低于介电系数2温度曲线的峰值温度的现象 ,我们认 为这种现象是由于Байду номын сангаас品在远低于介电峰值温度的温 度下 发 生 宏 畴2微 畴 或 宏 畴2微 小 畴 的 转 变 引 [8 ] 起的 .
系压 电 陶 瓷 的 掺 杂 对 压 电 性 能 的 影 响 规 律 十 分 类似 .
3. 3 去极化温度与介电峰值温度的相互关系
电常数 ,这为提高 Na1Π 2 Bi1Π 2 TiO3 系陶瓷的压电性能 提供一个新的途径 . 从表 1 中还可以看到 ,与 NBBT 陶瓷相比 , B 位 掺杂五价铌的 NBBTNb 陶瓷的 d33 增大 ,介电系数增 大 ,损耗增大 ,而 B 位掺杂三价钴的 NBBTCo 陶瓷的
都有所增大 , 特别是的 B 位掺杂高价铌的 NBBTNb 陶瓷的压电常数 d33 达到 149pCΠ N , 这可能是目前
Na1Π 2 Bi1Π 2 TiO3 系 压 电 陶 瓷 的 最 大 值 . A 位 多 加 (BiNa) 2 + 和少加 (BiNa ) 2 + 都会提高 NBBT 陶瓷的压
3 实验结果
3. 1 X 射线衍射分析
图 1 是所研究的 Na1Π BaTiO3 陶瓷的 X 2 Bi1Π 2 TiO3 2 射线衍射图谱 . 从图 1 可以看到 ,所研究的陶瓷都形 成了纯的钙钛矿结构 . 我们已经知道
[8 ]
,NBBT 陶瓷
处于相界的四方相区一侧 ,为四方结构 . 从图上可看 到 ,非化学计量和掺杂的陶瓷样品没有改变基础配 方 NBBT 陶瓷的结构 , 都为四方结构 ; 值得注意的 是 B 位掺杂钴的 NBBTCo 陶瓷的衍射图谱的第一个 衍射峰发生了明显的分裂 , 根据四方相的晶面面距 公式
NBBT(1 + x ) 125 740 0. 0212 215 135
NBBTNb 149 1230 0. 0390 250 70
NBBTCo 108 450 0. 0150
112 841 0. 0204 250 140
tgδ
TmΠ℃ Td/ ℃
— — —
155
易 ,那么就会充分挖掘压电陶瓷的潜力 ,提高压电性 能 ,使压电系数增大 . 对于 A 位非化学计量的陶瓷 2+ 样品 , A 位少加 (Bi1Π 产生 A 位空位 , 晶格松 2 Na1Π 2) 弛 ,缓冲了 90° 畴转向造成的应力 , 易于 90° 畴的转 2+ 向 ,导致压电系数增大 ; 对于 A 位多加 (Bi1Π 2 Na1Π 2) 的 NBBT ( 1 + x ) 陶瓷 , 由于空气中的氧会进入晶格 2+ 补偿多加的 ( Bi1Π 的电价 , 从而产生 B 位的 2 Na1Π 2) 空位 . B 位的空位与 A 位空位相类似 , 它会使晶格 松弛 ,有利于提高压电系数 , 但同时它也会削弱 B 位对自发极化的贡献 ,不利于提高压电系数 ,因此它
