第5章 立体化学
第5章 重排反应(2)

迁移到缺电子性的碳原子上
碱性条件下的驱动力:
5.2 重排到缺电子的氧原子上
5.2.1 Hock重排——过氧化氢异丙苯的重排
ቤተ መጻሕፍቲ ባይዱ 迁移能力: H > Ar > R
5.2.2 Baeyer-Villiger氧化
立体化学——构型保持
5.3.5 Lossen 重排
5.3.6 Curtius重排
5.3.7 Schmidt重排
重排到缺电性的氮原子上——总结:
离去基团的存在,N-LG键的极化使得N变成缺电子性。。。
羰基的存在使得酰胺上的质子具有一定的酸性; 羰基容纳电子的性质使得重排反应发生。
写出下列转化的机理:
Lewis酸
离去能力: POCl3 > OH-
5.3.2 Beckmann重排
离去能力: H2O > OH-
当底物是醛肟时,消除生成腈:
Second-order Beckmann rearrangement
5.3.3 Neber重排
-氨基缩酮
-氨基酮
-氨基缩酮
5.3.4 Hoffman降解
迁移能力 :Ar > R
迁移规律与Wagner-Meerwein碳正离子的迁移规律一致
立体化学——构型保持
5.2.3 Dakin氧化
给电子基
无水条件下可得到甲酸酯
当底物为间羟基苯甲醛时,氢优于芳基先迁移: -I
总结——重排到缺电性的氧原子上
5.3 重排到缺电子的氮原子上
5.3.1 Stieglitz重排
立体化学 第5章 环烷烃
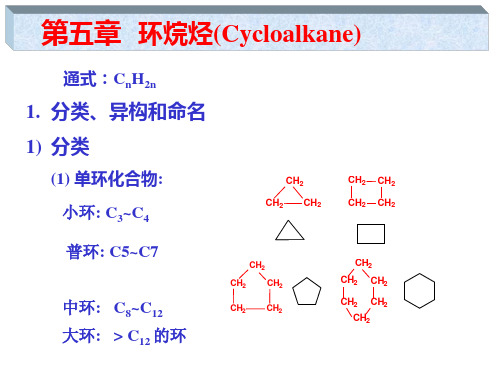
1,2,4-三甲基环己烷
C. 必要时须注明立体构型;
D. 复杂化合物也可将环的部分当作取代基。
顺-1,2-二甲基环丙烷 反-1,3-二甲基环丁烷
4-环戊基庚烷
(2) 多环化合物的命名:
(命名较为复杂, 以二环化合物为例). A. 参加成环的总碳原子数作为母体烃; 如有8个碳原子,则称为辛烷 B. 简单桥环可用“二环”、“三环”等作词头; C. 二环“连接”处的碳原子为桥头碳原子; D. 从桥头碳原子处,由大环开始编号;将各“桥”所含的碳原子 数写入方括号中(注意:桥头C原子都不可计入)。
2) 环戊烷的构象
环戊烷的结构是以拆叠的形式存在,四个C原子基本在一 平面上,另一个C则在平面之外,这种构象称为信封式构象。 环戊烷由于以“信封式”构象存在,使分子张力较小,化学性 质较稳定。
3) 环己烷的构象及构象分析
i) 椅式和船式构象
椅式
船式
船式构象相对能量较高, 不稳定,通过C-C键扭曲, 使其成为扭曲式(或称为扭 船型)。这种构象相对于船 式能量低。
角张力---由于键角偏离正常键角 而产生的张力。
环丙烷的三个C在同一平而上,相邻两个C上的C-H键都是重叠式构象, 相互拥挤,产生排斥,也具有较高的能量。
扭转张力---由于重叠式构象而产生的张力。
4. 环烷烃的构象和构象分析
1) 环丁烷的构象
环丁烷的四个C不在同一平面上,形如蝴蝶。即通过C-C键的扭转而以 一个拆叠的碳环存在。 环丁烷的三个C原子分布在同一平面,另一个C取于平面之外。 环丁烷的这种存在形式可使环的张力降低,但仍然是一个不稳定分子。
(1)分子中有两个平行的平面,C1、C3、C5和C2、C4、C6;
(2)12个氢原子分成两类:一类与分子对称轴平行,即垂直于环平面,称为
5 第5章 立体化学 3
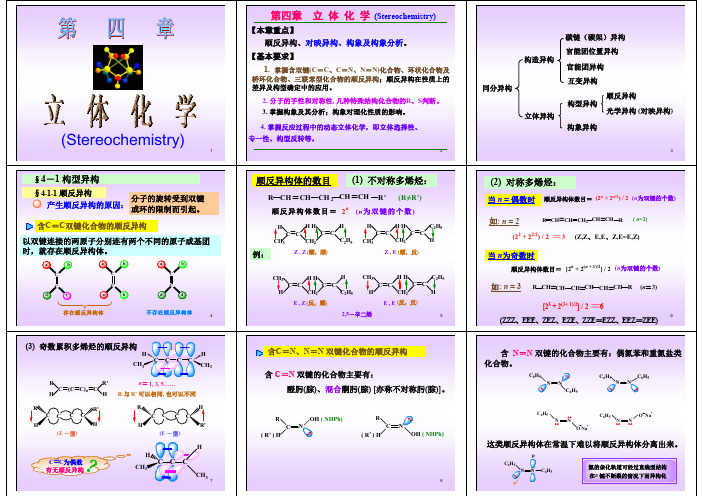
构成手性分子的必要和充分条件是: 分子中既没有对称面也没有对称中心, 一般就可以断定它是手性分子。
26
2. 化学转变法
通过化学转变,将未知构型的化合物与已知构型化 合物联系起来,可以确定顺反异构体的构型。如邻硝基 肉桂酸:
H
C CH
[H]
重氮化
水解
NO2 HO C O
H H
OO
21
对称因素 对称面:
S 构型
Cl HO2C
CO2H Cl B
R 构型
CO2H
CO2H
Cl
CO2H HO2C
Cl
Cl
Cl
A
B
37
这种数字代替基团的简易构型标记法也可用于其它手性轴化合物, 例:
丙二烯 类型:
H
H
2
CC C
H3C
CH3
1
4
R3
螺环类型:
H3C
H
CH3
1
3
4
2
H
2
4
3
S1
简易构型标记法也适合亚烷基环烃类和联苯型。
3个光学异构体
30 30
R/S 标记方法:手性轴标记法(四面体法)
手性轴
H
H
H
H
P
CCC
CCC
Q
CH3
CH3
CH3
CH3
P 方向投影
Q方向投影
H
H
CH3
CH3 R - 2, 3 -戊二烯
靠眼睛近的原子 或基团比远离眼 睛的原子或基团 优先。
H
CH3
H
CH3 R - 2, 3 -戊二烯
结论: R/S 构型的确定与从手性轴的哪一端观察无关。33
有机化学理论课 第五章 旋光异构

第五章旋光异构(Optical Isomerism)一、教学目的和要求同分异构是有机化合物的普遍现象,因此同分异构化学即立体化学的一个重要部分,它是研究组成分子的各个原子在空间的不同排布方式所引起的异构现象,以及因这些异构现象而引起的分子的物理和化学性质的差异的影响.所以讨论立体化学时,总是先从立体异构现象谈起.前面我们已在第二章、第三章、第四章讨论了某些立体异构现象,例如,烷烃构像、脂环烃构像、含双键和脂环化合物顺反异构。
本章在对上述内容作简要小结后,重点讨论立体异构现象中最重要,也是不易掌握的对映异构现象,为进一步学习碳水化合物、蛋白质,以及各类反应中的立体化学现象打好基础本章学习的具体要求1、掌握有机化合物异构的分类2、掌握对映异构、手性、手性分子、非手性分子、旋光活性、旋光活性物质、旋光度和比旋光度等有关概念3、掌握对映异构体数目的计算方法和对映、非对映、外消旋体和内消旋体的概念。
4、掌握费歇尔投影式和投影规则5、了解外消旋化。
二、教学重点与难点重点是旋光异构,旋光与分子结构的关系;含不对称碳原子化合物的旋光异构;难点是旋光异构的表示方法;R、S命名法。
三、教学内容1、偏振光和旋光性2、分子的对称性,手性,旋光活性3、构型表示方法D/L,R/S4、含有多于一个手性碳原子的立体异构5、取代丙二烯类和取代联苯类的旋光异构6、立体专一反应和立体有择反应7、外消旋体的拆分四、教学方法和教学学时(1)教学方法:以讲授为主;教具、多媒体为辅助手段,配合适量的课外作业(2)教学学时:4学时五、总结、布置作业5.1 各种异构现象的归纳旋光异构又称对映异构或光学异构,是指两个分子或多个分子间,由于构型的差异而表现出不同的旋光性能的现象,这些分子互为旋光异构体。
5.2 物质的旋光性Optical Activities of Substances偏振光(plane-polarized light )使偏振光的振动平面发生偏转的特性叫旋光性。
第五章 立体化学

四、判断对映体的方法
有三种方法可以用来判断一个分子是否 存在对映体: 1.建造一个分子和它的镜像的模型,如果 两者不能重合,就存在对映体。 2. 如果分子有对称面,那么它和其镜像 就能重合,就不存在对映体。 3.如果一个分子有一个手性碳原子,它就 具有对映异构现象,有一对对映体。
第二节 费歇尔(Fischer)投影式
D-(-)-甘油酸
D-(-)-乳酸
D.L命名法的使用有一定的局限性,它只适用与甘油醛结构 类似的化合物.目前,仍用于糖类和氨基酸的构型命名
二、 R.S构型命名法
R/S 构型标记法分为两步:
(1) 按次序规则确定与手性碳相连的四个原子 或基团的优先次序(或称为“大小” 次序)
3
CH3 C H4 Br1
对称面
内消旋酒石酸分子
问题:内消旋体是否显旋光性?为什么? 答案:不显旋光性。因为内消旋体有一对 称面,互为对称的两部分对偏振光的影响 相互抵消,使整个分子不表现旋光性。
第六节 构型命名
一、D.L命名法 规则:以甘油醛为标准,Fischer投影式中C* 上羟基处于右侧的为D-构型;反之为L-构型
CH3 H C6H5
S构型
CH3
Br
HO H
S构型
C6H5
COOH HO H
R构型
COOH H3C Cl C6H5
R构型
CH2OH
问题:判断下列手性碳的R、S构型。
R
HO COOH C H
R
H H
CO2H OH OH CH3
CH3
R
R-乳酸
2R,3R-2,3-二羟基丁酸
实物与镜像不重合
不含 对称中心 对称面
CO2H H HO C C OH H HO H
第五章 立体化学基础

第五章立体化学基础:手性分子1.将1.5g的旋光物质溶解在乙醇中,配成50ml溶液:(1)假如该溶液在10 cm 旋光仪管中观察旋光度为+2.79°时,求出20℃时的钠光(D线)下的比旋光度;(2)假如上述溶液在5 cm 旋光管中测定,那么测得的旋光度是多少?(3)若将此溶液由50ml稀释到150ml 且在10cm管中进行测定,旋光度又是多少?2.比旋光度是+40°的某物质,在1分米的旋光管中测得的旋光值为+10°。
试问此物质溶液的百分浓度为多少?3.判断下列分子是否具有对称中心、对称轴或对称面?(1)反1,2-二甲基环丙烷(2)环己烷的船式构象(3)乙烷的交叉式构象(4)丁烷的对位交叉式构象(5)乙烷的重叠式构象4.(S)-(-)-1-氯-2-甲基丁烷二氯代后所得产物的分子式为C5H10Cl12 。
试预测能有几种馏分,画出各馏分化合物的结构,各馏分有无旋光性?5.分别列举一对互为构造异构体,构象异构体和顺反异构体的实例(用结构式表示)。
构象异构体通常能分离吗?6.下列分子哪些是手性分子?7.将(—)、(+)和内消旋酒石酸三者等量的混合物进行分步结晶,可得到两部分均无旋光性的结晶。
哪两部分?8.解释下列概念⑴手性分子;⑵手性碳原子;⑶对映体;⑷非对映体;⑸内消旋化合物;⑹外消旋体;⑺旋光性;⑻旋光性化合物。
9.化合物(+)-丙氨酸和(-)-丙氨酸在下述性质方面有哪些异同?⑴熔点;⑵密度;⑶折光率;⑷旋光性能;⑸水中溶解度。
10.若测得一蔗糖溶液,旋光度为+90°,怎么能确知它的旋光度不是-270°?11.下列化合物,各有几个手性碳原子?12.下列化合物中,哪些存在内消旋化合物?⑵,3-二溴戊烷 2⑶,4-二溴戊烷⑴,3-二溴丁烷 2213.用R/S构型命名法标记下列分子构型14.用R/S构型命名法命名下列各个化合物的构型;并说明哪对是互为对映体?哪对互为非对映体?15.指出下列各组中两个化合物的关系(相同化合物?对映体?非对映体?)16.(S)-2-甲基-1-氯丁烷在光的作用下,与控制量的氯气发生取代反应,生成二氯代产物的混合物,分离得到A:2-甲基-1,4-二氯丁烷和B:2-甲基-1,2-二氯丁烷。
高等有机化学 第5章 消除和加成反应

5.1.3 β-消除反应的方向
对于无环体系中的消除反应已经提出了两种不同的解释。 (1)休斯和英格尔德观点 霍夫曼取向是由于离去基和β-碳原子上烷基的电子效应
使得两个β-碳上氢的酸性不同所引起的。酸性较高的氢优先 被碱移去。
据此理论可知,一个带正电的不良离去基,例如N+Me3 和S+Me3导致E2历程移向E1cB一端。在似E1c B的过渡态 中,β-C-H键具有更多的破裂程度,酸性较大的β-H更易被 碱夺去,而发生霍夫曼消除。
R CH CH2R' H+ RCH CHR' + H2O OH
5.1 消除反应
亲核取代反应常常伴随有消除反应,例:
CH3 CH3 C L
CH3
H2O CH3COCH3
CH3 CH3
CH3 C OH + CH2 C CH3 + HL
CH3
取代产物
消除产物
L代表卤原子X,OTs等等。
醇类在无机酸催化下的脱水反应,例:
应使过渡态中初期的双键和烯烃中的双键稳定之故。
H
HCH
HH
H
HCC
H H
CCH δH δB
Ⅰ
H
HCH H
HC C CH3 δ
CH2 H Bδ
Ⅱ
5.1.3 β-消除反应的方向
5.1.3 β-消除反应的方向
在E2 反应中,双键可能有两种不同的取向,至于按那种
取向进行消除反应取决于作用物的结构和离去基的性质及碱 的强度。
对于消除反应,根据共价键破裂和生成的次序可分为三 种历程。
H
CC L
C C +H + L
除了与SN1和SN2相对应的E1和E2外.还有一种极端的 E1cB历程。
第五章对映异构

[教学目的] 通过本章的学习,掌握对映异构的概念 使学生掌握有机化学中立体化学的知识 [教学重点] 含有一个、两个手性碳原子的对映异构 [教学难点] 亲电加成反应的立体化学
第五章 对映异构—教学要求
[教学基本要求] 1、对映异构现象与分子结构的关系 2、手性及对称因素 3、含一个手性碳原子化合物的对映异构 4、构型的表示方法——Fischer投影式 5、含两个手性碳原子化合物的对映异构 6、构型的R/S命名规则 7、环状化合物的立体异构 8、不含手性碳原子化合物的对映异构
第五章 对映异构—旋光性(偏振光)
2、偏振光的振动方向
第五章 对映异构—旋光性
3、旋光性、旋光度α、左旋体、右旋体
第五章 对映异构—旋光性(旋光仪)
二、旋光仪和比旋光度 1、旋光仪
第五章 对映异构—旋光性(旋光仪)
偏振光和起偏镜、检偏镜的关系:
第五章 对映异构—旋光性(旋光度)
2、旋光度 每一种旋光性物质,在一定条件下, 都有一定的旋光度。但因测定旋光度 时,溶液的浓度、盛液管的长度、温 度及所用光的波长等对旋光度都有影 响,因此,为了能比较物质的旋光性 能,通常规定:
但有些含对称轴的化合物,却不含对称面和 对称中心,也具有手性。例如,反一 1 , 2 一 二氯环丙烷分子中有二重对称轴,但没有对 称面和对称中心,具有旋光性,是手性分子。
第五章 对映异构—对称因素(对称轴)
因有无对称轴不能作为判断分子有
无手性的标准。在手性分子结构中,往
往允许有象对称轴的对称因素存在。
第五章 对映异构—对称因素(对称中心)
2、对称中心: 若分子中有一点P,通过P点画任何直线, 如果在离 P 等距离的直线两端有相同的 原子或基团,则点 P 称为分子的对称中 心(用 i 表示)。例如, 2 , 4 一二氟一 1 , 3一二氯环丁烷,即具有对称中心i。
第五章立体化学基础(手性分子)

第五章 立体化学基础(手性分子) 一、选择题1.下列化合物具有旋光性的是( )。
CH 2OHHO HCH 2OH3HA .B .C .D .33COOHH2.3-氯-2,5-二溴己烷可能有的对映体的个数是( )。
A .3对 B .1对 C .4对 D .2对3.下列羧酸最稳定的构象是( )。
COOHCH 3H 3C H 3CCOOHCH 3A .B .C .D .4.下列化合物构型为S 型的是( )。
A .B .C .D .CH 3BrHNH 2CH 3HOH CH 2CH 3CH 2OHClH OHCOOHHOH CH 2OH5.具有手性碳原子,但无旋光活性的是( )。
A.E-1,2-二甲基环丁烷B.Z-1,2-二甲基环丁烷C.1,2-二氯丁烷D.1,3-二氯丁烷E.1,4-二氯丁烷 6.下列化合物的绝对构型为( )。
COOH H OHCH 2CH 3A .B .C .D .D-L-R-S-型型型型7.下列化合物构型为S 型的是( )。
A .B .C .D .CH 3BrHNH 2CH 3HOH CH 2CH 3CH 2OHClH OHCOOHHOH CH 2OH8.下列互为对映体的是( )。
H HO COOH H OH COOHH OHOH H COOH HHOOCOH H HO COOH OHH COOH HHOCOOH (1)(3)(4)(2)(1)(3)(4)(2)(1)(3)(2)和和和和(3)A .B .C .D .9.3R ,4R-3,4-二苯基戊酸的最稳定构象是( )。
A .B .C .D .3C 6H 56H 5HOOCH 23C 6H6H 53C 6H H C 6H65H 3H C 6H10.下列分子没有手性的是( )。
A .顺-1-甲基-3-乙基环戊烷B .反-1-甲基-3-乙基环戊烷C .顺-1-甲基-2-乙基环丙烷D .反-1-甲基-3-乙基环丁烷 11.下列化合物的Newman 式对应的费歇尔投影式为( )。
第5章立体化学基础

CH3
CH3
H
OH
异丙醇
H
OH
H CH3
OH
2,32,3-丁二醇
CH3
H
CH3
H
CH3
CH3
H
1,11,1-二氯乙烷
H
顺-1,2-二甲基环丙烷 二甲基环丙烷
四、判断对映体的方法
1. 最直接的方法是建造一个分子及其镜像的模型。 最直接的方法是建造一个分子及其镜像的模型。 如果两者能重合,说明分子无手性, 如果两者能重合,说明分子无手性,没有对映异构现 象;如果两者不能重合,则为手性分子,有对映异构 如果两者不能重合,则为手性分子, 现象,存在对映体。 现象,存在对映体。 2. 考察分子有无对称面。如果分子有对称面, 考察分子有无对称面 如果分子有对称面, 对称面。 则该分子与其镜像就能重合,没有对映异构现象。 则该分子与其镜像就能重合,没有对映异构现象。 3. 大多数情况下,可根据分子中是否存在手性碳 大多数情况下,可根据分子中是否存在手性碳 原子(或手性中心 来判断分子是否有手性。 原子 或手性中心) 来判断分子是否有手性。 或手性中心
COOH COO H
CO OH H HO C CH 3
H OH CH 3 CH 3 OH H
COO H C H3 C H OH
-
二者的关系:互为镜象(实物与镜象关系, 二者的关系:互为镜象(实物与镜象关系,或 者说左、右手关系)。二者无论如何也不能完全重 者说左、右手关系)。二者无论如何也不能完全重 )。 叠。这种呈物体与镜像关系,彼此又不能重叠的性 这种呈物体与镜像关系, 呈物体与镜像关系 质称为手性。 质称为手性。
COOH COOH
H OH CH3 CH3 OH
H
第5章 立体化学基础

configurational ~ 对映异构
立体化学是指研究分子立体结构的化学。
构造异构:指分子式相同,分子中原子 或基团间的相互连接方式或连接顺序不 同而产生的异构现象。
立体异构:指分子的构造式相同而原子 或基团在空间的取向不同产生的异构现 象,即分子的立体形象不同而产生的异 构现象。
构型异构属于立体异构,它包括顺反异构 和对映异构。
本章学习要点:
1、掌握立体化学中的基本概念,学会用 Fischer投影式表示对映异构体的构型;
2、掌握对映异构体的系统命名、“次序规则” 及D/L和R/S构型标记法;
3、理解取代环烷烃的顺反异构和构象异构; 4、了解与立体异构现象相关的知识。
Chapter 5 主要内容
一、平面偏振光及比旋光度 二、对映异构 三、对映体的构型标记 四、取代烷烃的立体化学 五、旋光异构体的性质
看:乳酸分子的两种构型
肌肉运动产生右旋乳酸; 乳酸杆菌使葡萄糖
发酵得到左旋乳酸;
*O
CH3-CH-C-OH OH
• 从酸牛奶中分离得 到的乳酸无旋光性, 称为外消旋乳酸。
乳酸分子模型
三种来源不同的乳酸物理性质不同:
名称 右旋乳酸 左旋乳酸 外消旋乳酸
m.p.(℃) 28 28 18
[α]D20 +3.80 -3.80 00
一对对映体的物理性质相同, 旋光度大小相等, 方向相反。
三种乳酸是不同化合物, 消旋乳酸实际上是右 旋乳酸和左旋乳酸的等量混合物。外消旋体 (用“±”表示)熔点降低, 没有旋光性。
4. Introducti(1822-1895)
外消旋酒石酸钠铵
O or S
C
P
N
大学有机化学第五章 旋光异构(GAI)

(2S,3R)-2-羟基-3-氯丁醛
3)R/S和D/L构型标记法和旋光方向没有必然联系 构型只表示原子或原子团的空间排列方式,旋 光方向与基团空间排列方式、性质、结构有关,可用 旋光仪测定。命名时不用写出“+、-”的符号。
C 2H 5 H CH3
3R-3-甲基-1-戊烯
CH3
CH CH2
C HO C 2H 5
• HOOC—*CH—*CH—COOH • OH OH • CH3 - *CH- *CH-CH3 • Br Br
HOOC H OH HOOC HO COOH H H OH
HO H HOOC
H HOOC
OH
H
OH COOH
mirror
Ⅰ(2R,3R)-酒石酸
Ⅱ(2S,3S)-酒石酸
Ⅲ(2R,3S) )-酒石酸
COOH HO HO
2 3
OH H
H H
CH3
CH3
Ⅰ(2R,3S)-2,3-二羟基丁酸 Ⅲ (2S,3S)-2,3-二羟基丁酸 * C2 OH>COOH>CH(CH3) >H OH
C3*
OH>CH COOH>CH3>H OH
Ⅰ 和Ⅲ互为非对映体
HO
2
CHO
1
HO 2 H HO CH3 4 H
CHO 1
b a d
R
b
b c d
c
b
c
a
C
a d
S
c
C a
d
当最小基团d放在横线上时, 情况相反, 顺时针S -构型,逆时针构型为R -构型。(横 反竖不反)
a
a
d
c b
S
生物化学第5章-蛋白质的三维结构(共41张PPT)

亮氨酸拉链结构,Leucin zipper;
EF手型钙结合性模序
(EF-hand Ca2+-binding motif)
肌钙蛋白的两个结构域。
七、球状蛋白与三级结构
1、定义:蛋白质的三级结构是指多肽链中全部氨基酸残基的相对空间位置,即整 条肽链的三维构象。蛋白质的三级结构是在多种二级结构的基础上进一步
早在20世纪30年代,科学家就开始有X-射线衍射方法研究了肽的结构。 1、酰胺平面:参与肽键形成的两个原子及相邻的四个原子处于同一平面
,形成了酰胺平面,也称肽键平面,又称一个肽单位;多肽链的主链 由许多酰胺平面组成,平面之间以α碳原子相隔。
肽键的键长介于C-N单键和双键之间,具有部分双键的性质,不能自由旋 转;(肽键中C-N键长0.132nm, C-N单键0.148nm,C=N键)
基酸,某些氨基酸如脯氨酸和甘氨酸经常存在其中,由于甘氨酸缺少侧链(只有一个H),在β-转
角中能很好的调整其他残基的空间阻碍,因此使立体化学上最合适的氨基酸;而脯氨酸残
基的R与其α氨基己形成吡咯环,不能形成α-螺旋,因此在一定程度上迫使β-转角形成 。
四、Protein的二级结构——无规则卷曲
random coil
侧链与介质水,主链肽基与侧链或主链肽基与水之间形成。
②稳定蛋白质三维结构的作用力——盐键
盐键又称盐桥或离子键,它是正电荷与负电荷之间的一种静电相互作用。 在近中性环境中,蛋白质分子中的酸性氨基酸残基侧链电离后带负 电荷,而碱性氨基酸残基侧链电离后带正电荷,二者之间可形成离 子键。多数情况下,可解离侧链基团分布在球状蛋白的表面,与介 质水形成水化层,稳定蛋白构象。
酰胺平面中的键长、键角是一定的;
有机化学PPT第五章 立体化学基础课件

南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
含有一个手性碳原子的化合物,在空间有2种不同构
型, 它们彼此构成一对对映体。
CH3C* HCOOH
COOH
OH
乳酸
HO C H
CH3
COOH H C OH
CH3
有一个手性碳的化合物必定 是手性化合物,只有一对对映体。
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
问题:下列化合物哪些含手性碳原子?
1. CH2Cl2
2. CHCl3 3.CH3CHClCH2CH3
4. CH3-CH-CH2CH3 CH2CH3
H
6.
CH3 7.
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
第一节 手性分子和对映体
一、手 性
观察自己的双手, 左手与右手有什么联系和区别?
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
左右手互为镜像与实物关系(称为对映关 系),彼此又不能重合的现象称为手性。
H
2 COOH
H3C3 1Cl
H 1OH
2 CH2CH3
3CH3
竖,顺,R南-京型医科大学康达学院化学教横研室,有逆机化,学 R-型
南京医科大学康达学院 博学至精 明德至善
课堂练习:根据Fischer投影式命名。
2
CO2H
H
OH 1
3 CH3 R-(-)-乳酸
HOCH2 3
有机化学第五章脂环烃

或
5
1-甲基-3-乙基环戊烷 甲基-
CH2 CH2 CH2 CH-CH3 CH2 CH CH(CH3)2 或
4 5
6 1 2 3
1-甲基-3-异丙基环己烷 甲基③ 若环烃中有双键时,编号应从双键开始,且使编号的数 若环烃中有双键时,编号应从双键开始, 值最小。 值最小。
1 6 5 4 2
结论: 结论: ● e键取代基最多的构象稳定 ● 大取代基(体积)在e键的构象稳定 大取代基(体积)
§5-5 脂环烃的制备
一、芳烃化合物还原法
Ni 180~ 180~250℃
+ 3 H2
+ H2
催化剂
H2 催化剂 四氢化萘 十氢化萘
二、分子内偶联法
1.武慈合成法——主要适合于制备三 主要适合于制备三、 1.武慈合成法——主要适合于制备三、四元环
1,31,3-环己二烯
3
若环中有双键也有支链时,编号从双键起, ④ 若环中有双键也有支链时,编号从双键起,且要使支链 编号尽可能最小。 编号尽可能最小。
1 5 2
3-甲基环戊烯 CH3
4 3
1 6 5 4 2
1,61,6-二甲基环己烯
3
2. 螺环烃的命名
螺环烃编号方法----- 从邻接于螺原子的一个碳原子开始, ① 螺环烃编号方法----- 从邻接于螺原子的一个碳原子开始, 由小环到大环。 由小环到大环。 螺环烃命名方法---------用 做词头, ② 螺环烃命名方法-----用螺做词头,然后在方括号中写出 每 个环的碳原子数(不包括螺碳) 个环的碳原子数(不包括螺碳)从 小 7 8 1 2 10 1 9 环到大环。 环到大环。 CH2 CH2 CH2 2 C CH2 8 4 5 CH2 CH CH2 5 6 3 3 7 6 4 CH3 5-甲基螺[3 .4] 辛烷 甲基螺 甲基 螺[4.5]癸-1,6-二烯 [4.5]癸 1,6-
立体化学

化 学 结 构
化 学 反 应
第一章 立体化学
(Steric Chemistry)
静态立体化学 测定分子所具有结 构的立体形象的方法和应用; 构的立体形象的方法和应用;结构 的立体形象和物理性质的关系 态立体化学 分子的立体形象 化学 应性 应方 和 的
立 体 化 学
内容提要
§1-1 静态立体化学 一、含有刚性结构化合物的构型异构 二、光学异构 (一)分子的对称性 (二)含一个手性中心的分子 (三)含两个或多个手性中心的分子 (四)环状化合物的光学异构 (五)含手性轴的分子
C6H5
C N
N N
OH
C6H5
(三)脂环化合物的顺反异构
二、光学异构 (一)分子的对称性 1.对称要素 1.对称要素 (1)简单对称轴 (1)简单对称轴 符号: 符号:Cn
Cl H C C
H Cl
180°
Cl H
C C
H Cl
分子围绕通过分子中心、 分子围绕通过分子中心、并且垂直于分 子所在平面的直线旋转一定的角度后, 子所在平面的直线旋转一定的角度后,同原 简单对称轴。 来的分子重合,此直线为简单对称轴 来的分子重合,此直线为简单对称轴。
(2S, 3R) L-赤藓糖 赤藓糖
(2R, 3R) L-苏阿糖 苏阿糖
(2S, 3S) D-苏阿糖 苏阿糖
赤(藓) 型 (ery-):相同原子或基团在碳链同侧 藓 : 苏(阿) 型 (threo-):相同原子或基团在碳链异侧 阿 :
(五)含手性轴的手性分子 如果分子的手性是由于原子或原子团围绕 某一直线的非对称排列而产生的, 某一直线的非对称排列而产生的,该点就称为 手性轴。相当于把手性中心拉长成一条直线。 手性轴。相当于把手性中心拉长成一条直线。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
COOH COOH 两个基团 两个基团 HO H OH H HO 再对调一次 对调一次 CH3 CH3
CH3
COOH
COOH 在纸平面上 H OH H o 旋转180 CH3
如果固定某一个基团,而依次改变另三个基团的位置,则构型不变。
H H3C CH2CH3 COOH CH3CH2
H
COOH CH3
Constitution
Configuration
对映异构 旋光异构 Conformation
异构体间 的互变须 经过化学 键的断裂 和重新生 成才能实 现!
2
构造异构:指具有相同的分子式而分子中原子间键合的顺序或/
和方式不同而产生的不同的分子结构。
构造异构类型
碳架异构 位置异构 构造异构 官能团异构 CH3 OCH3 CH3 CH2 CH2 CH3 CH3 CH2 CH2 Cl
绕对称轴旋转 180°之后
16
有些具有对称轴的分子中不含有对称面或对称中心, 是手性分子 。
有二重对称轴,但没有对称面和对称中心, 和它的镜像不能重合,是手性分子。
结论
有无对称轴不能作为判断分子有无手性的依据。
17
(4) 更替对称轴(旋转反映轴)
穿过分子画一直线,分子以它为轴旋转360/n后,再用一个与此
个键伸向前方,而竖向的两个键伸向后方,交叉点为手性碳原子。
Fischer 投影式的操作:
(1) 不能离开纸面翻转。可以沿纸面旋转180,但不能旋转90或270;
(2) 基团两两交换次数不能为奇数次,但可以是偶数次。
COOH H OH C H3 HO COOH H C H3
翻转
翻转
24
CO O H H OH C H3
6
旋光仪、旋光度、比旋光度
旋光性物质:能使偏振光偏振面偏转的物质。 旋光度:使偏振光偏振面旋转的角度,用表示。 旋光方向:右旋(+); 左旋(-) 旋光性:使偏振光偏振面旋转的能力,用比旋光度表示。
[a ]l =
t
a
c× l
t 温度,l 光源的波长; 旋光度,
l 盛液管的长度,c 溶液浓度
7
光学(旋光、对映)异构的发现
绝 能真实代表某一 对 光活性化合物的 构 型 构型(R、S)
注意:
无论是D,L还是R,S标记方法,都不能通过其标记的构型来判断旋光方向; 旋光方向是化合物的固有性质,而对化合物的构型标记只是人为的规定; 仅从化合物的构型还无法确定其旋光方向,必须通过实验来确定; R/S标记用来表示手性中心原子的构型比较明确,符合系统命名的要求,缺 点是不能反映异构体之间的联系,同时在许多情况下,即使保持手性中心构 型不变的情况下进行反应,其产物的R和S构型也可能发生了改变。
22
构型的表示法 Fischer 投影式
COOH H C CH3 OH
COOH H C CH3 OH
COOH H OH CH3
立体结构
锲形式
投影式
Fischer投影式
[约定 ]将含有碳原子的基团 (主链)写在竖线上,把命名时编号最小 的碳原子写在竖线上端。在投影时,与手性碳原子横向相连的两
23
8
2、手性中心与手征性
若分子中的某一原子(通常是碳)上连接有四个不同基团时,该 四个基团在空间可有两种不同的相对排列位置,构成一对异构体 ,两个异构体互成不能重合的实物与镜像的对映关系。
OH CH3CHCOOH
乳酸
这样的对映异构好似人的左手和右手的关系,互为镜像但不能重合,故把这 种实物和镜像对映却又不能重合的现象称为手征性,简称手性;具有手(征) 性的分子叫手(征)性分子;连有四个不同基团的中心原子称为手性中心,手 性中心是碳原子称为手性碳。手性分子具有旋光性。 注意:任一化合物都有镜像,但多数化合物的实物和它的镜像结构都是能 够重合的。如果结构上的这种实物和它的镜像能够重合,则它们就是同一 物质,因而是非手性的,没有对映异构,也不是对映异构体。 9
CH3 CH3 CHCH3 CH3 CHCH3
Cl
CH3 CH2 OH CH3 CHO
3
互变异构 CH2 =CHOH
立体异构 A. 构象异构
分子中的原子或原子团互相键连的方式和连接的次序 相同,但在空间的相对位置不同而引起的异构。根据
引起的异构的方式不同分为构象异构和构型异构。
定义:由于单键旋转而引起的原子在空间的相对位置不同。
热H2SO4
pka1 pka2 2.93 4.23 2.93 4.23
139 139 烯 溴烷
(+)-2-甲基-1-丁醇
(- )-2-甲基-1-丁醇
HBr CH3COOH
D
酯
旋光异构体在手性环境下(如手性试剂、手性催化剂等) 其反应 速率不同。生物体内的酶和各种底物具有手性,构成手性环境, 手性分子进入生物体内手性环境后, 引起不同的分子识别,不同 的对映体在生理活性上相差很大。
直线垂直的平面进行反映,如果得到的镜像与原来的分子能够
重合,这条直线就是更替对称轴,用Sn表示。
具有更替对称轴的化合物 和镜像能够重合,因此没 有手性,不具旋光性。
18
结 论:
A、有对称面、对称中心、交替对称轴的分子均可与其镜象重 叠,是非手性分子;反之,为手性分子; B、对称轴并不能作为分子是否具有手性的判据; C、大多数非手性分子都有对称轴或对称中心,只有更替对称 轴而无对称面或对称中心的化合物是少数; D、手性分子具有光学活性。 所以,对于那些既无对称面也没有对称中心的分子,一般可 判定为是手性分子。
旋 转180
C H3 。 HO H CO O H
旋
转
旋转180o则构型保持不变
旋转180 。
CO O H H OH C H3
旋 转90 。
H C H3 CO O H OH
旋转90o则构型改变
旋 转90 。
25
将投影式中与手性碳相连的任意两个基团对调, 对调一次或奇数次则转变 成它的对映体;对调二次或偶数次则构型保持不变。
部分的镜像,则这个平面就是分子的对称面。
对称面
14
(2) 对称中心
若分子中有一点,通过该点画任何直线,如果在离此点等距 离的两端有相同的原子,则该点称为分子的对称中心。
对称中心
15
(3) 对称轴
以设想直线为轴旋转360o/ n,得到与原分子相同的分子,该直
线称为n重对称轴(又称n阶对称轴),用Cn表示 对称轴 对称轴
pKa=3.79(25oC)
(R)-()-乳酸 mp 53oC []15 D=-3[]15 D=0
pKa=3.86(25oC)
乳酸含有一个手性碳原子,有手性,具有旋光性,有一对对映体; 发酵得到的乳酸是左旋的,其比旋光度为–3.8o; 肌肉运动产生的乳酸是右旋的,其比旋光度为 + 3.8o; 从酸奶中得到的乳酸无旋光性,它是等量的左旋乳酸和右旋乳酸的 混合物,称外消旋体(常用±或dl表示)。外消旋体是混合物。
一个可使平面偏振光向右旋,称为右旋体;另一个可使平面偏 振光向左旋,称为左旋体。二者使平面偏振光旋转角度相同。 因此叫做对映异构、旋光异构或光学异构。
呈现实物与镜像的不重合性是产生对映异构现象的充分必要条件!
10
旋光异构体的性质 在非手性环境下,旋光异构体的物理性质与化学性质相同。 名称 (+)-酒石酸 (-)-酒石酸 熔点/oC 170 170 []25(20%水) 溶解度 +12o - 12o
第五章
同分异构现象 具有相同的分
立体化学
立体化学
研究分子在三维 空间的结构以及 与三维结构相联
子式而拥有不
同的分子结构, 因而也拥有不 同物理、化学 性质。
系的特殊物理性
质和化学性质的 科学。
一、同分异构体的分类
具有相同的分子式,但具有不同结构的化合物互称为异构体。
异构体主要分为两大类:构造异构和立体异构
优先顺序
OH > C2H5 > CH3 > H 28
基于Fisher投影式判断R、S构型:
顺序最小的原子(或基团)在竖线上, 顺时针排列为R构型,
逆时针排列为S构型。 顺序最小的原子(或基团)在横线上, 顺时针排列为S构型, 逆时针排列为R构型。
29
D,L标记的是相对构型,R,S标记的是绝对构型
CH3 H
C C
CH3 H
CH3 H
C C
H CH3
CH35
二、旋光异构、手征性与分子对称性 1、旋光异构 平面偏振光
光是一种电磁波,朝各个方向振动且光波的振动方向与光的传播 方向垂直。只在一个平面上振动的光,称为平面偏振光,简称偏 振光或偏光。
光波前进方向
光源
普通光
平面偏振光
普通光经过Nicol棱镜,可产生仅在一个平面上振动的光— ——— 平面偏振光
H
COOH OH CH 3
D-(-)-乳酸 27
R / S标记法
a c d
a
R
b
b
S
c
d
R/S标记分为两步
1. 将与手性碳原子相连的四个原子或原子团按优先顺序规则排序, 如a > b > c > d; 2. 把最小的基团d放在最远离观察者的位置,其余三个基团指向观察者,沿 着C*d的方向、按从大到小的优先顺序观察 a、b、 c三个基团的排列方式 ,顺时针排列则构型为R(rectus),逆时针排列构型为S(sinister)。
11
对映异构体的作用差异——匹配性
12
药理活性差异
多巴
治疗帕金森综合症的首选药物 造成粒状白细胞减少症(极度危险)
普萘洛尔
用于治疗心脏病 男性避孕药
