醇的性质和应用PPT下载1
合集下载
醇的性质和应用上课ppt课件
饱和一元醇通式:
CnH2n+1OH或 CnH2n+2O
阅读教材第71页有关甲醇、乙二醇 和丙三醇的介绍,总结三种醇的 物理性质和常见用途。
认识到了贫困户贫困的根本原因,才 能开始 对症下 药,然 后药到 病除。 近年来 国家对 扶贫工 作高度 重视, 已经展 开了“ 精准扶 贫”项 目
新
知
可上网查看相 关危害新闻哦!
思考
⑴如何区分乙醇溶液和无水乙醇?
取少量酒精,加入无水硫酸铜, 若出现蓝色,则证明是工业酒精.
⑵如何实现由乙醇溶液向无水乙醇转化?
乙醇溶液 加CaO生成Ca(OH)2 无水乙醇
(96%)
蒸馏
(99.5%)
认识到了贫困户贫困的根本原因,才 能开始 对症下 药,然 后药到 病除。 近年来 国家对 扶贫工 作高度 重视, 已经展 开了“ 精准扶 贫”项 目
3CH3CH2OH+2K2Cr2O7+8H2SO4→
(橙红色)
3CH3COOH+2Cr2(SO4)3+2K2SO4+11H2O
(绿色)
= =
认识到了贫困户贫困的根本原因,才 能开始 对症下 药,然 后药到 病除。 近年来 国家对 扶贫工 作高度 重视, 已经展 开了“ 精准扶 贫”项 目
知识拓展
(1). 2R—CH2—OH + O2
认识乙醇与氢卤酸的反应。
1.组装如图所示装置。在试管I中依 次加入2 mL蒸馏水、4 mL浓硫酸、 2 mL 95%的乙醇和3 g 溴化钠粉末, 在试管II中注入蒸馏水,烧杯中注入 自来水。加热试管I至微沸状态数分 钟后,冷却,观察并描述实验现象。
2.在该反应中,采用蒸馏水、浓硫 酸和溴化钠固体的目的是获得与乙 醇作用的氢溴酸。根据上述实验现 象,你能判断出乙醇与氢溴酸反应 的产物吗?请设计实验证明试管II中 收集到的是卤代烃吗?
醇的性质与应用 PPT课件

[问题4]下图为乙醇和氢溴酸反应的实验装置,该实验 过程中并没有直接加入氢溴酸,氢溴酸是如何获得的? 实验中可观察到试管I中的溶液由无色变橙黄色、试管II 中溶液分层,下层为无色油状液体。推测可能的原因?
[问题5]实验时为什么需要往试管I、试管II中加入少量 蒸馏水?及烧杯中注入的自来水有何作用?设计实验证 明该实验过程中有溴乙烷生成?
有机化学基础
专题4、烃的衍生物
第二单元 醇 酚 第一部分、醇的性质和应用
[问题1]分别写出胆固醇、维生素A、丁香油酚三种有 机化合物的分子式以及结构中具有的官能团名称?
[问题2]三只烧杯中分别加入乙醚、无水乙醇、水,从 煤油中取出一块金属钠,切去表层后分成三等份,分别 放入三只烧杯中,观察现象?推测乙醚、乙醇、水中氢 原子的活泼性强弱?实验中产生的气体成分?如何证明?
反应物
反应条件
Na
不需要
与O2催化氧化 Cu或Ag、加热 CH3COOH 浓硫酸、加热
HX
加热
脱水
浓硫酸、1400C
反应
浓硫酸、1700C
反应类型
断键方式
[问题11]饱和一元醇的通式?写出最简单的饱和一元 醇的分子式?阅读教材第70页了解这种物质性质?
[问题12]阅读教材第71页了解根据醇羟基的分类方式, 并了解几种常见的多元醇的物理性质。
[问题6]在下列试管中将乙醇和浓硫酸混合后,加热至 1400C可生成乙醚,试写出反应的化学方程式,判断 该反应的反应类型,分析反应中可能的断键方式?
[问题7]若将乙醇与浓硫酸混合液加热至1700C,可观 察到KMnO4溶液最终完全褪色,若证实使溶液褪色的 是乙烯气体,写出反应的方程式,反应类型?分析反 应中可能的断键方式?
部分专题4第二单元第一课时醇的性质和应用PPT课件

返回
1.下列说法不. 正确的是
()
A.乙醇分子中有1/6的氢原子与其他氢原子不一样
B.乙醇分子可认为是乙烷分子中的一个氢原子被一
个羟基取代产生的
C.乙醇分子中的每个碳原子都形成了四个键,但显
示的化合价不是+4价
D.乙醇的相对分子质量为46,相对分子质量为46的
就是乙醇
返回
解析:A.羟基上的一个氢原子与氧原子相连,其他氢原子 与碳原子相连;B.CH3—CH3去掉一个氢原子,换上—OH 便是CH3—CH2—OH;C.化合价与共用电子对的偏向有关, 乙醇分子中的二个碳原子都不是有四对共用电子对偏向的 原子;D.CH3—O—CH3的相对分子质量也是46。 答案:D
2.醇与钠反应生成醇钠与氢气,醇与卤化氢(HX)反 应生成卤代烃,醇可发生消去反应,一些醇可氧化生成相 应的醛或酮。乙醇在浓硫酸、170℃时生成乙烯,在140℃ 时生成乙醚。
返回
3.甲醇有剧毒,饮用少量可使眼睛失明,大量 使人死亡。
4.乙二醇可作为汽车发动机的抗冻剂,丙三醇具 有吸湿性,有护肤作用,是重要的化工原料。
返回
1.乙醇与钠反应生成H2 化学方程式为: 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑ 。 2.乙醇与氢卤酸发生取代反应 化学方程式为: CH3CH2OH+HBr―△―→CH3CH2Br+H2O 。
返回
3.乙醇的脱水反应 (1)分子内脱水(消去反应),化学方程式为: CH3CH2OH―浓―1H7―02S℃―O→4 CH2===CH2↑+H2O 。 (2)分子间脱水(取代反应),化学方程式为: 2CH3CH2O―浓―1H4―02S℃―O→4 CH3CH2—O—CH2CH3+H2O 。
返回
(3)丙三醇(甘油)结构简式: CH2OHCHOHCH2OH , 无色黏稠有 甜 味的液体,吸湿性强,它跟水、乙醇以任意比 例互溶,甘油水溶液的凝固点很低,用于制造硝化甘油。
1.下列说法不. 正确的是
()
A.乙醇分子中有1/6的氢原子与其他氢原子不一样
B.乙醇分子可认为是乙烷分子中的一个氢原子被一
个羟基取代产生的
C.乙醇分子中的每个碳原子都形成了四个键,但显
示的化合价不是+4价
D.乙醇的相对分子质量为46,相对分子质量为46的
就是乙醇
返回
解析:A.羟基上的一个氢原子与氧原子相连,其他氢原子 与碳原子相连;B.CH3—CH3去掉一个氢原子,换上—OH 便是CH3—CH2—OH;C.化合价与共用电子对的偏向有关, 乙醇分子中的二个碳原子都不是有四对共用电子对偏向的 原子;D.CH3—O—CH3的相对分子质量也是46。 答案:D
2.醇与钠反应生成醇钠与氢气,醇与卤化氢(HX)反 应生成卤代烃,醇可发生消去反应,一些醇可氧化生成相 应的醛或酮。乙醇在浓硫酸、170℃时生成乙烯,在140℃ 时生成乙醚。
返回
3.甲醇有剧毒,饮用少量可使眼睛失明,大量 使人死亡。
4.乙二醇可作为汽车发动机的抗冻剂,丙三醇具 有吸湿性,有护肤作用,是重要的化工原料。
返回
1.乙醇与钠反应生成H2 化学方程式为: 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑ 。 2.乙醇与氢卤酸发生取代反应 化学方程式为: CH3CH2OH+HBr―△―→CH3CH2Br+H2O 。
返回
3.乙醇的脱水反应 (1)分子内脱水(消去反应),化学方程式为: CH3CH2OH―浓―1H7―02S℃―O→4 CH2===CH2↑+H2O 。 (2)分子间脱水(取代反应),化学方程式为: 2CH3CH2O―浓―1H4―02S℃―O→4 CH3CH2—O—CH2CH3+H2O 。
返回
(3)丙三醇(甘油)结构简式: CH2OHCHOHCH2OH , 无色黏稠有 甜 味的液体,吸湿性强,它跟水、乙醇以任意比 例互溶,甘油水溶液的凝固点很低,用于制造硝化甘油。
高中化学课件《醇的性质和应用》

3.组成
一元醇的分子通式为 □ R—OH,饱和一元醇的分子通式为 02 CnH2n+1OH。
学生自主学习
师生课堂互动
学习效果检测
课时作业
4.化学性质与乙醇相似
(1)与活泼金属发生 □03 置换 反应。
(2)氧化反应(燃烧、催化氧化、被酸性 KMnO4 溶液氧化等)。
(3)消去反应。
(4)与 HX、羧酸等的 □04 取代 反应等。
的凝固点很低,用于制造硝化甘油。
学生自主学习
师生课堂互动
学习效果检测
课时作业
1.醇和卤代烃发生消去反应时有什么异同?
提示:相同点:①醇和卤代烃发生消去反应的规律类似,对有机物结构 的要求均为:醇(或卤代烃)分子所含碳原子数必须大于 1;与—OH(或—X) 相连的碳原子的邻位碳原子上有氢原子。②醇和卤代烃的消去反应均有烯烃 生成。
学生自主学习
师生课堂互动
学习效果检测
课时作业
[对点练习] 1.乙醇分子中不同的化学键如图所示,关于乙醇在各种不同反应中断裂 的键说明不正确的是( )
A.和金属钠反应时键①断裂
B.和浓 H2SO4 共热到 170 ℃时断键②和④ C.在银催化条件下与 O2 反应时断键①和③
D.和浓 H2SO4 共热到 140 ℃时断键②,其他键不变化
醇的性质和应用
[明确学习目标] 1.了解醇类的分类。2.掌握醇类的化学性质。3.理解醇 类催化氧化反应、消去反应机理与规律。
学生自主学习
师生课堂互动
学习效果检测
课时作业
23
学生自主学习
一、乙醇的结构和化学性质 1.分子结构
学生自主学习
师生课堂互动
学习效果检测
课时作业
一元醇的分子通式为 □ R—OH,饱和一元醇的分子通式为 02 CnH2n+1OH。
学生自主学习
师生课堂互动
学习效果检测
课时作业
4.化学性质与乙醇相似
(1)与活泼金属发生 □03 置换 反应。
(2)氧化反应(燃烧、催化氧化、被酸性 KMnO4 溶液氧化等)。
(3)消去反应。
(4)与 HX、羧酸等的 □04 取代 反应等。
的凝固点很低,用于制造硝化甘油。
学生自主学习
师生课堂互动
学习效果检测
课时作业
1.醇和卤代烃发生消去反应时有什么异同?
提示:相同点:①醇和卤代烃发生消去反应的规律类似,对有机物结构 的要求均为:醇(或卤代烃)分子所含碳原子数必须大于 1;与—OH(或—X) 相连的碳原子的邻位碳原子上有氢原子。②醇和卤代烃的消去反应均有烯烃 生成。
学生自主学习
师生课堂互动
学习效果检测
课时作业
[对点练习] 1.乙醇分子中不同的化学键如图所示,关于乙醇在各种不同反应中断裂 的键说明不正确的是( )
A.和金属钠反应时键①断裂
B.和浓 H2SO4 共热到 170 ℃时断键②和④ C.在银催化条件下与 O2 反应时断键①和③
D.和浓 H2SO4 共热到 140 ℃时断键②,其他键不变化
醇的性质和应用
[明确学习目标] 1.了解醇类的分类。2.掌握醇类的化学性质。3.理解醇 类催化氧化反应、消去反应机理与规律。
学生自主学习
师生课堂互动
学习效果检测
课时作业
23
学生自主学习
一、乙醇的结构和化学性质 1.分子结构
学生自主学习
师生课堂互动
学习效果检测
课时作业
醇酚之醇性质和应用李淑仙.pptx
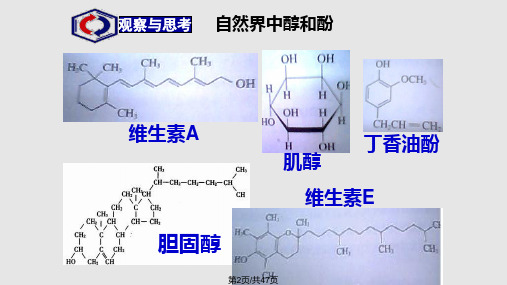
已知:—C=C—CH—+Br2 400℃ —C=C—C—Br
试写出由丙烯制硝化甘油的化学方程式。
第38页/共47页
1、-OH 与OH- 有何区别?
电子式 电荷数 存在形式
羟基(-OH )
. O ··H
不显电性 不能独立存在
﹕﹕ ﹕﹕
氢氧根(OH- )
[
..
O
··H
-
]
带一个单位的负电荷 能独立存在
反应条件
NaOH的乙醇溶液、 浓硫酸、加热到
加热
170℃
化学键的断裂 C—Br、C—H
C—O、C—H
化学键的生成
反应产物
CH2=CH2、HBr
第24页/共47页
CH2=CH2、H2O
学与问 能发生消去反应的醇,分子结构特点是什 么?是不是所有的醇都能发生消去反应?
下列各种醇与浓硫酸共热到一定温度不能产生 烯烃的是(BD )
乙醇与氢卤酸的反应
HH
学生表演H H
H―C―C―OH + H―Br
H―C―C―Br + H―OH
HH
HH
第19页/共47页
醇的性质和应用
②①
HH R—C —C—O—H
HH
若②处C—O键断
开,又会如何?
CH3CH2OH + HBr △ CH3CH2Br + H2O (可逆程度较大)
第20页/共47页
观察与思考 自然界中醇和酚
维生素A
肌醇
丁香油酚
维生素E
胆固醇
第2页/共47页
醇、酚的区别
烃分子中饱和碳原子上的氢原子被羟基(—OH) 取代形成的化合物称为醇。
分子中 羟基(—OH)与苯环(或其他芳环)碳原子
试写出由丙烯制硝化甘油的化学方程式。
第38页/共47页
1、-OH 与OH- 有何区别?
电子式 电荷数 存在形式
羟基(-OH )
. O ··H
不显电性 不能独立存在
﹕﹕ ﹕﹕
氢氧根(OH- )
[
..
O
··H
-
]
带一个单位的负电荷 能独立存在
反应条件
NaOH的乙醇溶液、 浓硫酸、加热到
加热
170℃
化学键的断裂 C—Br、C—H
C—O、C—H
化学键的生成
反应产物
CH2=CH2、HBr
第24页/共47页
CH2=CH2、H2O
学与问 能发生消去反应的醇,分子结构特点是什 么?是不是所有的醇都能发生消去反应?
下列各种醇与浓硫酸共热到一定温度不能产生 烯烃的是(BD )
乙醇与氢卤酸的反应
HH
学生表演H H
H―C―C―OH + H―Br
H―C―C―Br + H―OH
HH
HH
第19页/共47页
醇的性质和应用
②①
HH R—C —C—O—H
HH
若②处C—O键断
开,又会如何?
CH3CH2OH + HBr △ CH3CH2Br + H2O (可逆程度较大)
第20页/共47页
观察与思考 自然界中醇和酚
维生素A
肌醇
丁香油酚
维生素E
胆固醇
第2页/共47页
醇、酚的区别
烃分子中饱和碳原子上的氢原子被羟基(—OH) 取代形成的化合物称为醇。
分子中 羟基(—OH)与苯环(或其他芳环)碳原子
《醇的性质和应用》课件

储存醇类物质时应远离火源和热 源,使用防爆电气设备,并配备 灭火器材。
个人防护措施
1 2
佩戴防护服
在处理醇类物质时,应穿戴化学防护眼镜、化学 防护服和化学防护手套。
通风
保持良好的通风条件,以降低醇蒸汽在空气中的 浓度。
3
使用个人防护器材
根据需要选择合适的个人防护器材,如呼吸器、 护目镜等。
THANK YOU
溶剂
醇可用作有机合成中的溶剂,用于溶解和提取各种物质。
化学原料
醇可用于合成多种化学品,如酯类、醚类、醛类等。
食品和饮料
01
02
03
调味料
某些醇具有特殊的风味, 可作为食品和饮料的调味 料。
香料
醇是许多香精和香料的主 要成分,用于增加食品和 饮料的香气。
防腐剂
某些醇具有抗菌和防腐作 用,可用于延长食品的保 质期。
03
醇的化学性质
氧化反应
叔醇可以被氧化生成羧酸 。
氧化生成羧酸
仲醇可以被氧化生成醛。
在催化剂的作用下,伯醇 可以被氧化生成酮。
氧化生成醛 氧化生成酮
酯化反应
与羧酸反应
醇可以与羧酸反应生成酯和 水。
与羧酸酐反应
醇可以与羧酸酐反应生成酯 和水。
与酰氯反应
醇可以与酰氯反应生成酯和 氯化氢。
取代反应
醇的毒性主要与其代谢产物和干 扰细胞代谢有关,长期接触高浓 度醇可能导致肝肾损伤、神经元 死亡等。
毒性症状
接触醇后可能出现头痛、恶心、 呕吐、腹痛、乏力等症状,严重 时可能导致昏迷或死亡。
防火和防爆
01
燃烧特性
醇类物质是易燃的,其闪点较低 ,一般在21℃以下。
爆炸条件
《醇的化学性质》PPT课件

•性质
——带有甜味的有毒粘稠液体,氢键使沸点高(197 ℃ )
——缩合:在微量H+或OH-存在下,乙二醇与环氧乙烷作用生成 一缩二乙二醇,和三缩三乙二醇,进一步作用,可得聚乙二醇
OHCH2CH2OHOHCH2CH2OCH2CH2OH(二甘醇)
OHCH2CH2OCH2CH2OCH2CH2OH (三甘醇)
• 性质
无色液体,易燃,爆炸极限:6.0%~36.5% ,有毒性,蒸气与眼接 触或饮用可致盲。
•用途
2020/11/8
13
——制备甲醛;有机合成中的甲基化试剂;溶剂;燃料
2、乙醇
•制法
——发酵
——工业上:由以乙烯为原料生产
CH2=CH 2 + H 2SO4(95 %) △
CH3CH2OSO2OH H3O+ CH3CH2OH (硫酸氢乙酯)
•说明
2020/11/8
8
醇分子内脱水,主要按E1机理进行,由于碳正离子的生成,易发
生分子重排;用Al2O3脱水,不发生重排
4. 酯的生成
醇与含氧无机酸或有机酸反应,生成酯。
•醇与含氧无机酸(硫酸、硝酸、磷酸)反应生成无机酸酯:
CH3OH + HO SO 2 OH
CH3OSO2OH + H 2O 硫酸氢甲酯(酸性硫酸甲酯)
CH2=CH 2 + H 2O
H3P O4 300℃, 7MPa~8MPa
CH3CH2OH
CH3CH=CH 2
+
H 2O
H3P O4 195℃, 2MPa
(CH 3)2CHOH
——乙醇精馏可得95.6%的工业酒精,可用生石灰共热蒸馏得99.
55%的乙醇,再用镁处理可得99.95%的乙醇;或用苯与之共沸得
最新《醇》课件幻灯片

2.甲醇、乙醇、丙醇均可与水以任意比例混溶, 这是因为甲醇、乙醇、丙醇与水形成了氢键。
二、乙醇
(一)乙醇的结构
分子式 结构式
结构简式 官能团
C2H6O
HH
CH3CH2OH
H—C—C—O—H HH
或C2H5OH
—OH (羟基)
(二)乙醇的物理性质:
让我 想一想?
颜 色 : 无色透明 气 味 : 特殊香味 状 态: 液体 挥发性: 易挥发 密 度: 比水小
乙醇
O
乙醛
氧化
CH3COOH
乙酸
乙醇 K2Cr2O7 (橙红色)
驾 驶 员 正 在 接 受 酒 精 检 Cr2(SO4)3 查
(绿色)
三、消去反应
HH
HC
C
H
浓H2SO4 1700C
CH2=CH2
+H2O
H OH
羟基和氢脱去结合成水
反应 与金属反应
催化氧化 消去反应 分子间脱水 与HX反应
⑤
H H② ①
+2H2O
启迪思考:
当--C上没有氢或只有 一个氢的情况又如何氧 化呢?
思考:
CH3
CH3
CH3-C-OH、 CH3-CH-OH、 CH3
都属于与乙醇同类的烃的衍生物,它们能否发生象乙 醇那样的催化氧化反应?如能,得到什么产物?
结论:羟基碳上有2个氢原子的醇被催化氧化成醛。
羟基碳上有1个氢原子的醇被催化氧化成酮。 羟基碳上没有氢原子的醇不能被催化氧化。
CH3CHO+Cu+H2O 乙醛
现象:Cu丝黑色又变为红色,产生特殊 气味(乙醛的气味)液体。
催ቤተ መጻሕፍቲ ባይዱ剂
2CH3CH2OH + O2 2CH3CHO + 2H2O 由此可见,实际起氧化作用的是CuO而
二、乙醇
(一)乙醇的结构
分子式 结构式
结构简式 官能团
C2H6O
HH
CH3CH2OH
H—C—C—O—H HH
或C2H5OH
—OH (羟基)
(二)乙醇的物理性质:
让我 想一想?
颜 色 : 无色透明 气 味 : 特殊香味 状 态: 液体 挥发性: 易挥发 密 度: 比水小
乙醇
O
乙醛
氧化
CH3COOH
乙酸
乙醇 K2Cr2O7 (橙红色)
驾 驶 员 正 在 接 受 酒 精 检 Cr2(SO4)3 查
(绿色)
三、消去反应
HH
HC
C
H
浓H2SO4 1700C
CH2=CH2
+H2O
H OH
羟基和氢脱去结合成水
反应 与金属反应
催化氧化 消去反应 分子间脱水 与HX反应
⑤
H H② ①
+2H2O
启迪思考:
当--C上没有氢或只有 一个氢的情况又如何氧 化呢?
思考:
CH3
CH3
CH3-C-OH、 CH3-CH-OH、 CH3
都属于与乙醇同类的烃的衍生物,它们能否发生象乙 醇那样的催化氧化反应?如能,得到什么产物?
结论:羟基碳上有2个氢原子的醇被催化氧化成醛。
羟基碳上有1个氢原子的醇被催化氧化成酮。 羟基碳上没有氢原子的醇不能被催化氧化。
CH3CHO+Cu+H2O 乙醛
现象:Cu丝黑色又变为红色,产生特殊 气味(乙醛的气味)液体。
催ቤተ መጻሕፍቲ ባይዱ剂
2CH3CH2OH + O2 2CH3CHO + 2H2O 由此可见,实际起氧化作用的是CuO而
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
3.在施工全过程中,严格按照经招标 人及监 理工程 师批准 的“施 工组织 设计” 进行工 程的质 量管理 。在分 包单位 “自检 ”和总 承包专 检的基 础上, 接受监 理工程 师的验 收和检 查,并 按照监 理工程 师的要 求,予 以整改 。
、4.贯彻总包单位已建立的质量控制 、检查 、管理 制度, 并据此 对各分 包施工 单位予 以检控 ,确保 产品达 到优良 。总承 包对整 个工程 产品质 量负有 最终责 任,任 何分包 单位工 作的失 职、失 误造成 的严重 后果, 招标人 只认总 承包方 ,因而 总承包 方必须 杜绝现 场施工 分包单 位不服 从总承 包方和 监理工 程师监 理的不 正常现 象。
溶剂
消毒剂(75% 的乙醇溶液)
饮料 燃料
专有名词:
医用酒精 75%(体积分数)
工业酒精 无水酒精
>96%(质量分数) >99.5%(质量分数)
饮用酒
视度数而定体积分数
思考 ⑴如何区分工业酒精和无水酒精?
取少量酒精,加入无水硫酸铜, 若出现蓝色,则证明是工业酒精.
⑵如何实现由工业酒精向无水酒精转化?
石油资源紧张制约着中国汽车事业的发展。 2001年中国宣布推广“车用乙醇汽油”。所谓 “乙醇汽油”就是在汽油里加入适量的乙醇混
合而成的一种燃料。下列有关叙述错误的是A
()
A.乙醇汽油是一种新型的化合物 B.汽车使用乙醇汽油能减少有害气体的排放 C.工业上常用裂化的方法提高汽油的产量 Dห้องสมุดไป่ตู้用玉米、高梁发酵可以制得乙醇
② 分子间脱水
CH3CH2OH+CH3CH2OH
浓硫酸 140℃
CH3CH2OCH2CH3+H2O
(4) 酯化反应 ——酸跟醇作用生成酯跟水的反应
羧酸 或无机含氧酸
五、乙醇的制法
⑴发酵法
⑵乙烯水化法
CH2=CH2
+
H2O
催化剂 加热、加压
CH3CH2OH
1.我公司将积极配合监理工程师及现 场监理 工程师 代表履 行他们 的职责 和权力 。
5.所有进入现场使用的成品、半成品 、设备 、材料 、器具 ,均主 动向监 理工程 师提交 产品合 格证或 质保书 ,应按 规定使 用前需 进行物 理化学 试验检 测的材 料,主 动递交 检测结 果报告 ,使所 使用的 材料、 设备不 给工程 造成浪 费。
谢谢观看
1.我公司将积极配合监理工程师及现 场监理 工程师 代表履 行他们 的职责 和权力 。
②
α CH3—CH—CH3
OH CH3
③ CH3—αC—CH3
OH ④
α CH3OH
OH
[思考]:
将铜丝在酒精灯外焰上灼烧,然后浸入无水乙
醇中,铜丝发生的变化:
.
往灼热的CuO粉末中通入乙醇蒸气,有何现象? 室温下往CuO粉末中通入乙醇蒸气,有何现象?
(4) 乙醇的脱水反应
① 分子内脱水
HH H―C―C―H
(2)与氢卤酸(HX)反应
C2H5 OH+H Br
C2H5Br+H2O
——取代反应
NaBr + H2SO4 = NaHSO4 + HBr
课本
(3)乙醇的氧化反应
氧化反应:有机物得“O”或去“H”的反应 还原反应:有机物去“O”或加“H”的反应
写出乙醇发生氧化反应的方程式 ① 乙醇的燃烧
②乙醇的催化氧化
2CH3CH2OH+O2
Cu △
O 2CH3C H + 2H2O
HH α
H C—C—H
两个H脱去与O结合成水
H O—H
***催化氧化基本原理: 脱去-OH上的H和αC上的H,形成C=O
***催化氧化基本原理: 脱去-OH上的H和αC上的H,形成C=O
下列醇能发生催化氧化吗?氧化后的产物是醛吗?
① CH3—CH2—αCH2
明
月
几 时 有 ?
把 酒 问 青
天
!
醇的性质和应用
1、定义
——烃分子中饱和碳原子上的H被羟 基取代而形成的化合物
1、定义
——烃分子中饱和碳原子上的H被羟 基取代而形成的化合物
2、存在及其作用
3、饱和一元醇的通式:
CnH2n+1OH 或 CnH2n+2O
乙醇俗称酒精,是人类最早制 备的有机物之一,也是大家相 当熟悉的一种醇!
2.我公司在开工前,将根据合同中明 确规定 的永久 性工程 图纸, 施工进 度计划 ,施工 组织设 计等文 件及时 提交给 监理工 程师批 准。以 使监理 工程师 对该项 设计的 适用性 和完备 性进行 审查并 满意所 必需的 图纸、 规范、 计算书 及其他 资料; 也使招 标人能 操作、 维修、 拆除、 组装及 调整所 设计的 永久性 工程。
3.在施工全过程中,严格按照经招标 人及监 理工程 师批准 的“施 工组织 设计” 进行工 程的质 量管理 。在分 包单位 “自检 ”和总 承包专 检的基 础上, 接受监 理工程 师的验 收和检 查,并 按照监 理工程 师的要 求,予 以整改 。
、4.贯彻总包单位已建立的质量控制 、检查 、管理 制度, 并据此 对各分 包施工 单位予 以检控 ,确保 产品达 到优良 。总承 包对整 个工程 产品质 量负有 最终责 任,任 何分包 单位工 作的失 职、失 误造成 的严重 后果, 招标人 只认总 承包方 ,因而 总承包 方必须 杜绝现 场施工 分包单 位不服 从总承 包方和 监理工 程师监 理的不 正常现 象。
重要应用:
确定乙醇的结构
思考:
乙醇的分子式为C2H6O,按C四价的原则结构可 能为:
H
H
H — C—O — C—H
H
H
×
HH H — C—C—O—H
√
HH
某校化学兴趣小组预备利用乙醇与金属钠的反 应来验证乙醇的分子结构,请选出实验所需仪器 和连接顺序:
问题:多余的钠如何处理?
再加入过量乙醇反应掉
5.所有进入现场使用的成品、半成品 、设备 、材料 、器具 ,均主 动向监 理工程 师提交 产品合 格证或 质保书 ,应按 规定使 用前需 进行物 理化学 试验检 测的材 料,主 动递交 检测结 果报告 ,使所 使用的 材料、 设备不 给工程 造成浪 费。
谢谢观看
H OH
浓硫酸 170 ℃
CH2=CH2 + H2O
思考:
是不是所有的醇都能发生消去反应?
下列物质与浓硫酸共热可得到烯烃的是 ( BD )
A. C6H5CH2OH C. (CH3)3CCH2OH
B. (CH3)3COH D. (CH3)2CHOH
上题选项中,不能发生催化氧化的是 ( B ) 能被氧化成为醛的是 ( A C )
2.我公司在开工前,将根据合同中明 确规定 的永久 性工程 图纸, 施工进 度计划 ,施工 组织设 计等文 件及时 提交给 监理工 程师批 准。以 使监理 工程师 对该项 设计的 适用性 和完备 性进行 审查并 满意所 必需的 图纸、 规范、 计算书 及其他 资料; 也使招 标人能 操作、 维修、 拆除、 组装及 调整所 设计的 永久性 工程。
2CH3CH2ONa+H2↑
回忆:
H-OH中羟基上的H比乙醇中羟基上的H活泼
钠的现象 声的现象
实验结论
钠与乙醇
沉在底部
无
Na的密度大于 乙醇。钠与乙 醇缓慢反应, 放出氢气。
钠与水
浮、熔
有“嘶嘶”声
Na的密度小于水, 熔点低。钠与水剧 烈反应,放出大量 热,生成氢气
课本
练习: 写出Mg与乙醇、钠与丙三醇反应的化学方程式
工业酒精 加CaO生成Ca(OH)2 无水酒精
(96%)
蒸馏
(99.5%)
二、乙醇的物理性质
学案P1
三、乙醇的结构
❖分子式 : C2H6O
❖结构式:
HH H — C—C—O—H
HH
❖结构简式: CH3CH2OH或C2H5OH
学案P1
四、乙醇的化学性质
(1)与活泼金属反应
2CH3CH2OH+2Na
