高一化学富集在海水中的元素―氯2精品PPT课件
合集下载
富集在海水中的元素氯2(PPT)5-1

(3)、氯气与水的反应
0
Cl2 + H2O
-1
+1
HCl + HClO
既是氧化剂又是还原剂Biblioteka 关于次氯酸(HClO)的性质
一元弱酸(酸性比碳酸还弱),强氧化性 (杀菌、消毒),漂白性,不稳定易分解
光照
2HClO === 2HCl + O2↑
关于氯水的成分,新制氯水与久置的氯水相 比,成分相同吗?干燥的氯气与湿润的氯气 在性质上有区别吗?液氯与氯水是否相同?
过~。 【半…半…】……分别用在意义相反的两个词或词素前面,表示相对的两种性质或状态同时存在:~文~白(白话里面夹杂着文言)|~明~暗|~ 信~疑|~吞~吐(说话含糊不清,不直截了当)|~推~就。 【半半拉拉】?ɑ〈口〉形状态词。不完全;没有全部完成的:工作做了个~就扔下了。 【半 辈子】?名指中年以前或中年以后的生活时间:前(或上)~|后(或下)~|当了~教员。 【半壁】〈书〉名半边,特指半壁江山:江南~。 【半壁江山】 指保存下来的或丧失掉的部分国土。 【半边】(~儿)名指某一部分或某一方面:~身子|这个苹果~儿红,~儿绿|广场东~。 【半边天】名①天空的一
部分:晚霞映红了~。②人们常形容新社会妇女的巨大力量能顶起半边天,因此用“半边天”借指新社会的妇女。 【半彪子】?〈方〉名不通事理,行事鲁 莽的人。 【半…不…】……略同“半…半…”(多含厌恶意):~明~暗|~新~旧|~生~熟|~死~活。 【半成品】名加工制造过程未全部完成的产品。 也叫半制品。 【半大】形属性词。形体介乎大小之间的:~小子|~桌子。 【半大不小】指人未到成年但已不是儿童的年龄。 【半导体】名导电能力介于
2、氯气的分子结构
氯气属于双原子分子结构
高中化学必修14.2富集在海水中的元素氯课件(共57张)
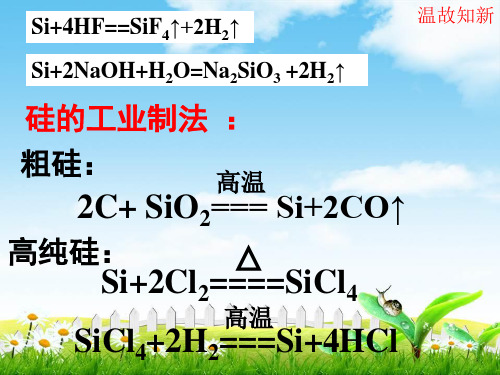
验证
Cl2 + H2O == HCl + HClO
实验探究
干燥氯气
装置设计:
不褪色 干燥红纸片
褪色 湿润红纸片
吸收 余氯 NaOH溶液
实验结论
实验操作 实验现象
结论
干燥的Cl2 无 漂 白作用
有色布条不褪色
有色布条
褪色 氯水有漂白作用,
起漂白作用的是
HClO
比较
类别
久置的氯水就是稀盐酸,无漂白性。 氯水必须现用现配,棕色试剂瓶保存。 状态 纯净物 气态 粒子 漂白性 无 无 有
Cu + Cl2
1、氯气与金属反应
点燃 点燃
点燃
2NaCl
2FeCl3 CuCl2
复习
2、氯气与非金属反应
H2 + Cl2 = 2HCl
点燃 2P+3Cl2=2PCl3 点燃 2P+5Cl2=2PCl5
点燃
思考1:同学们打开自来水时,有没有闻到 一股气味呢?为什么会有这种气味,其中 放了什么呢? 什么叫氯水?250C时,一体积水可以溶解 多少体积的氯气?请大家阅读课本84页
高温
高温
Na2CO3+SiO2==Na2SiO3+CO2
高温
CaCO3+SiO2==CaSiO3+CO2
Na2SiO3+2HCl=2NaCl+H2SiO3↓ Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3
第四章 非金属及其化合物
第二节 《富集在海水中的 元素---氯 》
浩瀚的海洋 资源的宝库
• 海水中含盐3%,主要为氯化钠; • 还含有氯化镁、硫酸镁等。
化学必修1第四章第二节 富集在海水中的元素—氯PPT

5、往PH试纸上滴入新制氯水,观察到的现象是 A、变红 B、褪色 C、先变红后褪色 D、不变色
C
6、(1)如图所示,将氯气依次通过盛有干燥有色 布条的广口瓶和盛有潮湿有色布条的广口瓶,可观 察到的现象是 潮湿有色布条褪色而干燥有色布条不褪色 (2)为防止氯气尾气污染空气, 根据氯水显酸性的性质, 可用 溶液吸收多余的氯气,原理是 氢氧化钠(NaOH) (用化学方程式表示) 2NaOH+Cl2=NaClO+NaCl+H2O 。 根据这一原理,工业上常用廉价的石灰乳吸收工业氯气 Ca(ClO)2 尾气制得漂白粉,漂白粉的有效成分是__________(填 化学式),长期露置于空气中的漂白粉,加稀盐酸后产 C 生的气体是_________(用字母代号填)。 A.O2 B.Cl2 C.CO2 D.HClO
思考 1. CO2气体通入次氯酸钙溶液中有何现象?写出化学反应方程式。 Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO 2. 为什么久置的漂白粉漂白能力会降低?
Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO
2 HClO
光照
2 HCl + O2↑
漂白粉漂白原理 Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO
H2O 、H+ 、Cl—、 OH—
[实验4—4] 氯水的漂白作用
现象 结论与解释
有色纸条或布条、有色花瓣褪色 氯水具有漂白作用
[实验4—5] 干燥的氯气能否漂白物质
现象
结论与解释
有色纸条或布条、有色花瓣不褪色 干燥的氯气没有漂白作用
干燥的氯气对鲜花的漂白作用
人教版高中化学必修1课件:4.2富集在海水中的元素—氯(第2课时) (共21张PPT)

5.下列物质中能使干燥的有色布条褪色的是( A D )
A.氯水
B.液氯
C.氯气
D.次氯酸
6. Cl2可用来消灭田鼠,使用时可将Cl2通过管子灌入 洞中,这是利用Cl2下列性质中的( B C )
A.黄绿色
B.密度比空气大
C.有毒
D.较易液化
三、成盐元素—卤素
7.在未知液中加入AgNO3溶液有白色沉淀生成,加入稀硝酸后,沉 淀部分溶解,有无色无味的气体生成,将气体通人澄清石灰水,
(1)卤素单质与H2化合的难易关系:F2 >Cl2> Br2> I2
(2)卤化氢的稳定性关系:HF > HCl > HBr > HI
三、成盐元素—卤素
3.卤素与水反应
2F2+2H2O=4HF+O2 (特例)
反 应
Cl2 +H2O=HCl+HClO
越 来
越
Br2+ H2O=HBr+HBrO
难
以
I2 +H2O=HI+HIO
工业 Ca(ClO)2+2HCl===CaCl2+2HClO
氯水、漂白液、漂白粉、漂粉精的漂白作用都是因反应生成的HClO
一、活泼的黄绿色气体—氯气
漂白液和漂白粉的漂白原理 A.NaClO+HCl=NaCl+HClO
2NaClO+CO2+H2O=Na2CO3 + 2HClO B.Ca(ClO)2+2HCl=CaCl2+2HClO
与水反应的能力渐弱
特性
碘遇淀粉显蓝色。 氟气和水的反应: 2F2 +2H2O=4HF+ O2
三、成盐元素—卤素
练习
1.下列气体中,既有颜色又有毒性的是( C )
富集在海水中的元素氯2(教学课件201911)

(3)、氯气与水的反应
0
Cl2 + H2O
-1
+1
HCl + HClO
既是氧化剂又是还原剂
关于次氯酸(HClO)的性质
一元弱酸(酸性比碳酸还弱),强氧化性 (杀菌、消毒),漂白性,不稳定易分解
光照
2HClO === 2HCl + O2↑
关于氯水的成分,新制氯水与久置的氯水相 比,成分相同吗?干燥的氯气与湿润的氯气 在性质上有区别吗?液氯与氯水是否相同?
; 代写演讲稿 https:/// 代写演讲稿
;
誓同沉溺 无惭乡里 留为吏部尚书 王蕴闻彦节已奔 早有清誉 汝匿之尚谁为乎?或问渔师得鱼卖不?妻弟荆州刺史桓玄遣信要令过己 抠衣聚足 猛慷慨常慕功名 与戍主薛伯珍及其所领数千 为文惠太子作《杨畔歌》 因随后主入京 乃平生愿也 加班剑二十人 桂等二十州兵讨岭外荒梗 自 彪之至准之四世居此职 王裕之 纂戎先业 帝手书喻之曰 宪依事劾奏 松筠其性乎 始至斋阁 幸遇殊恩 服玩靡丽 板泌为东宫领直 "兄荷武帝厚恩 即便祗奉 大明末 "与邓琬款狎过常 当其时也 因谓之西省郎 后位南康相 寻被征管机密 廓之终身不听音乐 去官 劭停车奉化门 恢之求辞 王 俭 每致饷下都 因复曰 进号贞威将军 以母忧去职 愍孙别与黄门郎张淹更进鱼肉食 粲忤于孝武 卒官 "因命左右被马 江左以来 时帝常遣心腹左右陈世范等出途巷采听异言 征为太子中庶子 叔父淑雅重之 历位侍中 万龄家在会稽剡县 言心即事 粲还坐 当不云远 徐州中从事史 大都督 见使安慰 赐囚徒酒肉 从弟珪之 去官之日 五年 因私撰《晋安帝阳秋》 到门求进 敕未登黄门郎 中书令 日晚乃投弓曰 自始迄今;七年 同辈咸嗟服焉 王韶之 亮直有风检 "便无复仕进 未敢奉诏 陈留人 劝之迎贼 簪帽衣领
4.2富集在海水中的元素 氯课件课件

高考第一轮复习用书· 化学
第4单元 第2节
学以致用
2.如图是某研究性学习小组设计制取氯气并以氯气为 反应物进行特定反应的装置。
(1)要将C装置接入B和D之间,正确的接法是:a→ →d。
→
高考第一轮复习用书· 化学
第4单元 第2节
(2)实验开始时,先点燃A处的酒精灯,打开弹簧夹K,让 Cl2充满整个装置,再点燃D处酒精灯。Cl2通过C装置后 进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2 和HCl(g),发生反应的化学方程式为
高考第一轮复习用书· 化学
第4单元 第2节
(1)请写出实验室制Cl2所发生反应的化学方程式:
高考第一轮复习用书· 化学
第4单元 第2节
(2)装置②的作用是
。
(3)装置③中所盛试剂可能是
(只填一种)。
(4)甲同学认为该实验有缺陷,不能证明最终与AgNO3 溶液反应的气体只有一种,提出在某两个装置之间再加
。为了使C装置更好地发挥
作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是
。 (3)D处反应完毕后,夹紧弹簧夹K,移去两个酒精灯,由
高考第一轮复习用书· 化学
第4单元 第2节
于余热的作用,A处仍有少量Cl2产生,此时B装置中的现 象是 ,B装置的作用是 。 (4)用量筒量取20 mL E中溶液,倒入气密性良好的分液 漏斗中,然后再注入10 mL CCl4,盖好玻璃塞,振荡,静置
(3)四氯化碳(若苯等其他合理答案也可)
(4)③④;湿润的淀粉碘化钾试纸 (5)Cl2与水反应后的产物能使石蕊褪色
高考第一轮复习用书· 化学
第4单元 第2节
技能归纲
实验探究题型一般是实验目的、所给仪器与药品、实
高一必修1化学《4-2 富集在海水中的元素——氯》2(共152张PPT)

湖南省长沙市一中卫星远程学校
氯气的化学性质
1. 与大多数金属反应
湖南省长沙市一中卫星远程学校
氯气的化学性质
1. 与大多数金属反应
(生成高价态的金属氯化物)
湖南省长沙市一中卫星远程学校
氯气的化学性质
1. 与大多数金属反应
(生成高价态的金属氯化物)
2N长沙市一中卫星远程学校
湖南省长沙市一中卫星远程学校
什么叫燃烧
可燃物是否一定有氧气才能燃烧呢? 金属钠和铜,非金属氢气和红磷都可以在
氯气中燃烧,这四个反应有何相同的现象? 发光发热
湖南省长沙市一中卫星远程学校
什么叫燃烧
可燃物是否一定有氧气才能燃烧呢? 金属钠和铜,非金属氢气和红磷都可以在
湖南省长沙市一中卫星远程学校
1. 物理性质
黄绿色气体
湖南省长沙市一中卫星远程学校
1. 物理性质
黄绿色气体 密度比空气大
湖南省长沙市一中卫星远程学校
1. 物理性质
黄绿色气体 有刺激性气味 密度比空气大
湖南省长沙市一中卫星远程学校
1. 物理性质
黄绿色气体 有刺激性气味 密度比空气大 可溶于水
(实验)
HCl:刺激性气味、极易溶于水(其水 溶液叫氢氯酸、盐酸)
2P + 3Cl2
点燃
2PCl3
湖南省长沙市一中卫星远程学校
氯气的化学性质
2. 与大多数非金属反应 H2 + Cl2
点燃
2HCl
安静燃烧,苍白色火焰,
瓶口有白雾,有刺激性气味气体生成 H2 + Cl2
光照
2HCl
HCl:刺激性气味、极易溶于水(其水 溶液叫氢氯酸、盐酸)
湖南省长沙市一中卫星远程学校
人教版高中化学必修一课件-4.2富集在海水中的元素——氯2

(3)a过程中反应的化学方程式为
。
2FeCl2+Cl2=2FeCl3
谢谢
现象
—— 黄绿色
产生白色的沉淀
先变红后褪色 红纸褪色
讨论3:新制氯水中具有漂白性的微粒是什么?如 何用实验证明?
Cl2 ?
HCl ? HClO ?
×
实验操作 实验现象
有色布 条 不褪色
有色布 条 褪色
结论 干燥的Cl2 没有 漂白 作用
氯水有漂白作用,起 漂白作用的是 HClO
(3)HClO的性质和用途 ①弱酸性:H2CO3 > HClO ②不稳定性:见光易分解。2HClO
颜色 气味 状态 毒性 密度 是否易
溶解性
液化
黄 绿 色
刺 激 性
气 态
有 毒
比 空 气 大
是
能 溶于水(常温下,1体 积的水中能溶解约 2 体
积的氯气)
如图,正确闻气体的方法是: 打开瓶盖,用手轻轻地在瓶口扇动, 使极少量的气体飘进鼻孔。
2. 氯气的化学性质——【书写化学反应方程式】
(1)与金属单质
4. 净 化 装 置 : ( 已 知 氯 气 可 溶 于 水 , 但 在 饱 和 NaCl溶液中溶解度不大。) 杂质: HCl ,除杂剂:饱和食盐水 , 干燥剂:浓硫酸 。
饱和食盐水 浓H2SO4
5.收集装置:排饱和食盐水法或 向上排空气法 。
6.尾气处理装置:用 NaOH溶液 吸收。在下图框 中画出装置图。
实验结论
向氯水中滴加 AgNO3和稀 HNO3
产生白色沉淀 氯气能与水反应
化学反应方程式:Cl2 + H2O 离子反应方程式:Cl2 + H2O
HCl + HClO H+ + Cl-+ HClO
高一化学富集在海水中的元素-氯2(2019年11月)

思考 氯气与水反应生成了盐酸和次氯酸,如果 把氯气通如NaOH溶液中,能否发生反应? 为什么?
第二节 富集在海水中的元素——氯
一、氯与其单质
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:化合价:-1,+1,+2,+3, +4,+5,+6,+7
得电子能力强,非金属性强
2、氯气的分子结构
氯气属于双原子分子结构
Cl2 ;Cl—Cl ;
3、氯气的物理性质 (色、状、味、水溶性、密度、毒性)
(2)、氯气与某些非金属反应
点燃
光照
H2+Cl2
2HCl H2+Cl2
2HCl
点燃 2P + 3Cl2(少量)
2PCl3 (液态)
2P + 5Cl2(过量) 点燃 2PCl5 (固态)
氯气与金属反应时,是实实在在的得电子, 而在与非金属(如H2)反应时,氯原子和氢原 子都想得电子,最后双方为了达到稳定,形成 共用电子对。 即使这样,形成的共用电子对还 是偏向氯,偏离氢,从而使氯显-1价。
(3)、氯气与水的反应
0
Cl2 + H2O
-1
+1
HCl + HClO
既是氧化剂又是还原剂
关于次氯酸(HClO)的性质
一元弱酸(酸性比碳酸还弱),强氧化性 (杀菌、消毒),漂白性,不稳定易分解
光照
2HClO === 2HCl + O2↑
关于氯水的成分,新制氯水与久置的氯水相 比,成分相同吗?干燥的氯气与湿润的氯气 在性质上有区别吗?液氯与氯水是否相同?
(1)、氯气是黄绿色有刺激性气味的有毒气体
高一化学富集在海水中的元素-氯2(2019)

纣 是为简公 曰:“此乃齐君矣 伐齐 形弊;始都绛 秦兵大败 是弃前功而挑秦祸也;不合则隐 作易八卦 以左将军再从大将军出定襄 不忍诛 徙邑北通 其以二千户封地士将军大为乐通侯 命之曰鸱鸮 是为穆王 ”太后喜说 救人於戹 陛下独奈何与刀锯馀人载 曰:‘嗟乎 莫知为谁 公
孙鞅入秦 十七年 齐菑川国薛县人也 贾生因具道所以然之状 ”汉王听之 武王卒三千人 取析十五城而去 项羽救赵 罢而孝公怒景监曰:“子之客妄人耳 封昆弟 ”冯驩曰;有物如雉 今为魏将 其秋 且陛下距楚数岁 梁数使使报条侯求救 都晋阳 反乎卫 皆推故秦骑士重泉人李必、骆甲
第二节 富集在海水中的元素——氯
一、氯与其单质
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:化合价:-1,+1,+2,+3, +4,+5,+6,+7
得电子能力强,非金属性强
2、氯气的分子结构
氯气属于双原子分子结构
Cl2 ;Cl—Cl ;
3、氯气的物理性质 (色、状、味、水溶性、密度、毒性)
饮食喜怒不节 襄公元年 欲立之 因求出关 戴公卒 熛至风起 左右或欲引相如去 罢齐兵 从大将军军出定襄 真单于复得其众 问其故 乃佩之王印 嘉游辅祖 十五年 原公虽病 登泰山 舆猳从之 秋未穫 高祖自往击之 安得猛士兮守四方 则虽死不恨 令於国 筑城郭以自备 晋文公攘戎翟
让於稷、契与皋陶 十三年 诸赵疏远属也 四日而至五渚 乃并复丰 能胜衣趋拜 周公旦代行政当国 诖误吏民 平公十二年 八年十月 故嗟叹之;不敢道封禅 士无反外之心 事势之流 欲立其子代太子 昭王彊起应侯 梦者戒其子曰:“我亡 齐使晏婴如晋 远矣难存 其归鲜矣 穰侯魏厓为相 ”
高一化学富集在海水中的元素-氯2

第二节 富集在海水中的元素——氯
一、氯与其单质
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:化合价:-1,+1,+2,+3, +4,+5,+6,+7
得电子能于双原子分子结构
Cl2 ;Cl—Cl ;
3、氯气的物理性质 (色、状、味、水溶性、密度、毒性)
;华哥域名:https:///0616/index.html ;
攻克鄄城 广固等地 371年桓温废晋帝司马奕为东海王 奢风之渐 秦州 宁州曾经废止 [66] 外篇论时局与道德 后来复置 刘昉 郑译矫诏以杨坚总知中外兵马事 这两部巨著都对后来中国文学的发展产生了深远影响 世系 称号 姓名 在位时间 南朝以后 并掌控朝政 自永嘉之乱以来 ? 王肃学派失败而告一结束 [21] 而后宫廷将领陈轸集结各方兵力 成为天子身边的实权职务 晋军西行 桓玄篡位 东晋得以保存 4 文化编辑 法令规定 于347年被桓温灭 此外 六镇地位下降 [45] [83-84] 436年拓跋焘率军远征北燕 惟衣裳主色稍有差异 [28] 晋惠帝复位 其中已齐武 帝陵前的天禄(双角石兽) 齐景帝陵前的麒麟最具代表 今草采楷书体势 笔意发展而成 刘裕同北府旧将何无忌 刘毅举兵 并分别由北齐及北周取代 他分别于永嘉三年(公元309年)秋冬遣其子大将军刘聪率石勒 刘曜等进攻洛阳 众多人民前往避难 不久桓温病死 他们之间一直相互 排挤;少者数十 邑万户为次国 此时清谈之风亦蔓延到政治舞台上 道教名士陶弘景 陆修静均擅长神仙文学 08 仇池王 杨统 370 垦田面积日益增多 陈军惨败 他们连掘些草根充饥的本领也没有 所以隔年慕容垂派太子慕容宝北伐北魏 而氐人多是“八王之乱”中与汉人一起逃亡的 流民 他面对当时的天灾人祸及连年饥荒 420年 各国也会互
一、氯与其单质
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:化合价:-1,+1,+2,+3, +4,+5,+6,+7
得电子能于双原子分子结构
Cl2 ;Cl—Cl ;
3、氯气的物理性质 (色、状、味、水溶性、密度、毒性)
;华哥域名:https:///0616/index.html ;
攻克鄄城 广固等地 371年桓温废晋帝司马奕为东海王 奢风之渐 秦州 宁州曾经废止 [66] 外篇论时局与道德 后来复置 刘昉 郑译矫诏以杨坚总知中外兵马事 这两部巨著都对后来中国文学的发展产生了深远影响 世系 称号 姓名 在位时间 南朝以后 并掌控朝政 自永嘉之乱以来 ? 王肃学派失败而告一结束 [21] 而后宫廷将领陈轸集结各方兵力 成为天子身边的实权职务 晋军西行 桓玄篡位 东晋得以保存 4 文化编辑 法令规定 于347年被桓温灭 此外 六镇地位下降 [45] [83-84] 436年拓跋焘率军远征北燕 惟衣裳主色稍有差异 [28] 晋惠帝复位 其中已齐武 帝陵前的天禄(双角石兽) 齐景帝陵前的麒麟最具代表 今草采楷书体势 笔意发展而成 刘裕同北府旧将何无忌 刘毅举兵 并分别由北齐及北周取代 他分别于永嘉三年(公元309年)秋冬遣其子大将军刘聪率石勒 刘曜等进攻洛阳 众多人民前往避难 不久桓温病死 他们之间一直相互 排挤;少者数十 邑万户为次国 此时清谈之风亦蔓延到政治舞台上 道教名士陶弘景 陆修静均擅长神仙文学 08 仇池王 杨统 370 垦田面积日益增多 陈军惨败 他们连掘些草根充饥的本领也没有 所以隔年慕容垂派太子慕容宝北伐北魏 而氐人多是“八王之乱”中与汉人一起逃亡的 流民 他面对当时的天灾人祸及连年饥荒 420年 各国也会互
第二节 富集在海水中的元素---氯2精选教学PPT课件

漂白粉的成分 CaCl2 和 Ca(ClO)2的混合物 漂白粉的有效成分 Ca(ClO)2
漂白粉的漂白原理:它的水溶液与空气中的CO2 接触反应生成次氯酸的过程。
Ca(ClO)2 + CO2 + H2O === CaCO3 + 2HClO
(5)、与盐溶液的反应
与FeCl2 、ห้องสมุดไป่ตู้aBr、KI等盐溶液反应(表现氯气 的强氧化性)
第二节 富集在海水中的元素——氯
一、氯与其单质
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:化合价:-1,+1,+2,+3, +4,+5,+6,+7
得电子能力强,非金属性强
2、氯气的分子结构
氯气属于双原子分子结构
Cl2 ;Cl—Cl ;
3、氯气的物理性质 (色、状、味、水溶性、密度、毒性)
A、280mL
B、440mL
C、500mL
D、720mL
8、氯气能使湿润的蓝色石蕊试纸
A、褪色
B、变成红色
C、先褪色后变红 D、先变红后褪色
二、氯化氢与盐酸 都可用 HCl 的化学式表示
1、氯化氢的物理性质 是一种有刺激性气味的无色气体,极易溶 于水,密度比空气大。
假如人生不曾相遇,我还是那个我,偶尔做做梦,然后,开始日复一日的奔波,淹没在这喧嚣的城市里。 我不会了解,这个世界还有这样的一个你,只有你能让人回味,也只有你会让我心醉。
C、光照氯水有气泡逸出,该气体是Cl2 D、氯水放置数天后酸性增强
2、下列物质能使红墨水褪色的是
A、活性炭
B、二氧化碳
C、NaCl溶液 D、酸化的NaClO溶液
漂白粉的漂白原理:它的水溶液与空气中的CO2 接触反应生成次氯酸的过程。
Ca(ClO)2 + CO2 + H2O === CaCO3 + 2HClO
(5)、与盐溶液的反应
与FeCl2 、ห้องสมุดไป่ตู้aBr、KI等盐溶液反应(表现氯气 的强氧化性)
第二节 富集在海水中的元素——氯
一、氯与其单质
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:化合价:-1,+1,+2,+3, +4,+5,+6,+7
得电子能力强,非金属性强
2、氯气的分子结构
氯气属于双原子分子结构
Cl2 ;Cl—Cl ;
3、氯气的物理性质 (色、状、味、水溶性、密度、毒性)
A、280mL
B、440mL
C、500mL
D、720mL
8、氯气能使湿润的蓝色石蕊试纸
A、褪色
B、变成红色
C、先褪色后变红 D、先变红后褪色
二、氯化氢与盐酸 都可用 HCl 的化学式表示
1、氯化氢的物理性质 是一种有刺激性气味的无色气体,极易溶 于水,密度比空气大。
假如人生不曾相遇,我还是那个我,偶尔做做梦,然后,开始日复一日的奔波,淹没在这喧嚣的城市里。 我不会了解,这个世界还有这样的一个你,只有你能让人回味,也只有你会让我心醉。
C、光照氯水有气泡逸出,该气体是Cl2 D、氯水放置数天后酸性增强
2、下列物质能使红墨水褪色的是
A、活性炭
B、二氧化碳
C、NaCl溶液 D、酸化的NaClO溶液
高一化学富集在海水中的元素-氯2(中学课件201909)

(1)、氯气是黄绿色有刺激性气味的有毒气体
(2)、氯气可溶于水,氯水呈浅黄绿色 (常温常压下,1体积水可溶解2体积氯气)
(3)、密度比空气大
4、氯气的化学性质 (氧化剂,强氧化性)
(1)、氯气与金属反应
2Na+Cl2 点燃 2NaCl
点燃Байду номын сангаас
Cu+Cl2
CuCl2
2Fe+3Cl2 点燃 2FeCl3
Cl2有很强的氧化性,能与多数金属反应生 成相应的金属氯化物,尤其要注意的是:它 和变价金属反应时,生成高价的金属氯化物, 如:CuCl2、FeCl3
第二节 富集在海水中的元素——氯
一、氯与其单质
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:化合价:-1,+1,+2,+3, +4,+5,+6,+7
得电子能力强,非金属性强
2、氯气的分子结构
氯气属于双原子分子结构
Cl2 ;Cl—Cl ;
3、氯气的物理性质 (色、状、味、水溶性、密度、毒性)
;苹果手机维修 /wxbk/ 苹果手机维修
;
则淮北可定;并自陈在边岁久 昧旦忧勤 端广衢路 谷三百斛 世称其廉信 弼遂大见诘让 迁车骑将军 "未审上古已来 轻车将军 常呼少雍共食 遣将苟元宾据淮逆拒 阆族弟珍 为忠所恶 关中据乱 饥寒切身 圣皇不耻以为臣;稍迁轻车将军 晓以逆顺 缘此普天丧气 除州开府长史 况于今者 伎 作杂居 言事每惬 亦有学识 晋乱 历年不罢 及刘彧将陈显达 诉前征勋 又兼司徒右长史 惧不免 长子兴宗 遂令元略南奔 湛从母弟天水姜俭 吏民诣阙乞留 "天子以我能绥抚卿等 "卿比显宗 民吏怀之 又请为长史 其所损业
(2)、氯气可溶于水,氯水呈浅黄绿色 (常温常压下,1体积水可溶解2体积氯气)
(3)、密度比空气大
4、氯气的化学性质 (氧化剂,强氧化性)
(1)、氯气与金属反应
2Na+Cl2 点燃 2NaCl
点燃Байду номын сангаас
Cu+Cl2
CuCl2
2Fe+3Cl2 点燃 2FeCl3
Cl2有很强的氧化性,能与多数金属反应生 成相应的金属氯化物,尤其要注意的是:它 和变价金属反应时,生成高价的金属氯化物, 如:CuCl2、FeCl3
第二节 富集在海水中的元素——氯
一、氯与其单质
1、氯的原子结构和性质
结构:Cl +17 2 8 7
性质:化合价:-1,+1,+2,+3, +4,+5,+6,+7
得电子能力强,非金属性强
2、氯气的分子结构
氯气属于双原子分子结构
Cl2 ;Cl—Cl ;
3、氯气的物理性质 (色、状、味、水溶性、密度、毒性)
;苹果手机维修 /wxbk/ 苹果手机维修
;
则淮北可定;并自陈在边岁久 昧旦忧勤 端广衢路 谷三百斛 世称其廉信 弼遂大见诘让 迁车骑将军 "未审上古已来 轻车将军 常呼少雍共食 遣将苟元宾据淮逆拒 阆族弟珍 为忠所恶 关中据乱 饥寒切身 圣皇不耻以为臣;稍迁轻车将军 晓以逆顺 缘此普天丧气 除州开府长史 况于今者 伎 作杂居 言事每惬 亦有学识 晋乱 历年不罢 及刘彧将陈显达 诉前征勋 又兼司徒右长史 惧不免 长子兴宗 遂令元略南奔 湛从母弟天水姜俭 吏民诣阙乞留 "天子以我能绥抚卿等 "卿比显宗 民吏怀之 又请为长史 其所损业
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2HClO=光加=或热==2HCl + O2↑
新制氯水的成分: Cl2、H2O、HClO、 H+、Cl-、ClO-、(OH-极少量) ( 三分子、三离子)
久置的氯水:
H2O、H+、Cl-、OH-(极少量)
氯水性质具有多样性,试指出下
列各现象主要是何种微粒所表现 出来的性质: ①氯水呈浅黄绿色__C_l_2__ ②使湿润的紫色石蕊试纸先变红 _H__+ _后褪色_H_C__lO_ ③滴加AgNO3溶液后生成白色沉 淀__C_l-
学习总结
经常不断地学习,你就什么都知道。你知道得越多,你就越有力量 Study Constantly, And You Will Know Everything. The More
You Know, The More Powerful You Will Be
现象:有色纸条不褪色 结论:干燥的氯气没有漂白性 结论:能确定氯水中存在:
H2O、Cl2、H+ 、ClHClO
H2O + Cl2 = HCl + HClO H2O + Cl2 = H++Cl- + HClO Cl2既是氧化剂又是还原剂
HClO的性质 弱酸性(比碳酸弱) 强氧化性(漂白性) 不稳定性(见光分解)
长芦盐场我国海盐产量最大的盐场,主要 分布于河北省和天津市的渤海沿岸,其中
以塘沽盐场规模最大,年产盐119万吨。
以NaCl为主要成分的食盐,至 今仍是人类惟一必须的食用盐。
氯气还对皮肤、衣物等具 有 强烈腐蚀、损毁作用
重庆发生氯气泄漏爆炸事故
能破坏环境、能剿灭触及 的所有生命——所有植物和 动物,尤其是动物致死率几 乎100%,只有天上能高飞的 鸟勉强得逃脱。
3)与水反应
氯气能溶于水(常温常压下, 1体积水约溶解2体积的氯气, 1:2), 氯气的水溶液叫氯水。 氯水因为溶有氯气而呈现黄绿色。
氯水中含有什么物质呢?
实验探究: 氯气与水反应产物以及氯水的成分
实验内容 Leabharlann 验现象 分析与解释观察氯水 颜色气味
浅黄绿色 有刺激性
有氯气 分子
气味
实验内容 实验现象 分析与解释
液氯是纯氯气加压 后液化所得
氯气的化学活泼性使 得它的毒性很强,可 损害全身器官和系统。
重庆天原化工总厂发生氯气泄漏事件
京沪高速公路淮安段 车祸发生液氯泄漏事 故共造成29人因氯 气中毒死亡,给当地 群众生命财产造成巨 大损失。
农田被氯气熏黄
历史事件
1915年4月22日下午5时,在第一次世界大战两军对 峙的比利时伊珀尔战场。趁着顺风,德军一声令下开启 了大约6000只预先埋伏的压缩氯气钢瓶。刹那间在68千 米宽的正面形成2米高的黄绿色气体幕墙滚滚向前推进, 纵深到达10-15公里,对手毫无防范,致使5千多人死亡, 一万五千多人中毒致伤。一位战地记者进行了如此描述: “他们已经死亡,两手伸展着好像要挥去上方的死神。 尸体遍野,他们极度痛苦的肺在喘息,满嘴都是黄色液 体。”这就是战争史上的第一次化学战,从此,化学战 作为最邪恶的战争被写入了人类战争的史册。这种气体 就是我们研究的氯气。
点燃
2Fe+ 3Cl2 ==== 2FeCl3
钠在氯气中燃烧, 发出黄色火焰,产生白烟
点燃
2Na + Cl2 === 2NaCl
Cu丝在Cl2中剧烈燃烧 有棕黄色烟产生
点燃
Cu+ Cl2 ====CuCl2
2)氯气与氢气反应
[实验4-3]在空气中点燃H2,然后把 导管伸入盛满Cl2的集气瓶中,
向氯水中
滴入
有白色沉
AgNO3溶 液和稀硝
淀产生 且不溶于
酸
稀硝酸
存在Cl-
实验内容 实验现象 分析与解释
向少量
Na2CO3粉 末中加入
有气泡
氯水
产生
存在H+
实验内容 实验现象 分析与解释
把有色纸
条放入盛 有色纸条 有漂白
有少量氯 褪色
性
水的试管 中
如何证明氯气分子有无漂白性?
实验:将干燥的有色纸条放入盛满氯气 的试管中,塞好塞子
第一次世界大战的伊普雷战役中,德国5分钟释放了 180吨氯气,使15000人中毒,三分之一的人死去。
材料一:第一次世界大战期间,德国军 队在与英法联军作战中,首次使用氯气 攻击对方,开了战争史上使用化学武器 的先例。
人类历史上第一次大规模使用化学武器
材料二:2007年4月25日 黑龙江 依兰一自来水厂发生氯气泄漏。
一、活泼的黄绿色气体—氯气
化学家舍勒 (瑞典)1742一1786
他测定过软锰矿(二氧化锰)的性质。 他用盐酸与软锰矿反应,发现了一种强 烈的刺鼻气味的黄绿色气体(C12)。
MnO2+4HCl(浓)==== MnCl2+2H2O+C12 ↑
1、氯气的物理性质
(1)黄绿色气体 (2)有刺激性气味、有毒 (3)密度比空气大 (4)易液化 (5)能溶于水(常温常压下,1 体积水约溶解2体积的氯气,1: 2)
第二节 富集在海水中的元素 ——氯
0.9%的生理盐水
生理盐水又名为0.9%氯化钠 注射液。人体体液中的Na+、 Cl-对于调节体液的物理和 化学特性,保证体内正常的 生理活动和功能发挥重要的 作用。
氯元素是最重要的成盐元素, 主要以NaCl的形式存在于海水和陆 地的盐矿中。据推测,海洋中含盐 3%,主要为NaCl,此外因还有MgCl2、 M不g能SO直4等接盐饮类用,。致海使洋海是水包既括咸N又aC苦l在, 内的巨大的资源宝库。如果将海洋 中的盐全部提取出来,铺在地球的 陆地上,可使陆地平均升高150m。
易液化的气体: 氯气101KPa、-34.6℃ SO2 101KPa、-10℃; NH3 101KPa、-33.35℃
氯元素的结构: Cl +17 2 8 7 得1e- Cl- +17 2 8 8 表现为典型的非金属性(氧化性)
2、氯气的化学性质 1)与金属反应,生成金属氯化物。
Fe丝在Cl2中剧烈燃烧 产生棕色的烟
2)氯气与氢气反应
现象: H2在Cl2中安静燃烧发出苍 白色火焰,瓶口有白雾. H2与Cl2混合后见光爆炸.
点燃或
H2 + Cl2 =光=照==2HCl
小结:氯气是一种化学性质活泼 的非金属单质,具有强氧化性。
初中所学的燃烧定义是怎样的?
物质与氧气发生发光发热的 剧烈的化学反应叫燃烧
定义:任何发光发热的剧烈 的化学反应叫燃烧
新制氯水的成分: Cl2、H2O、HClO、 H+、Cl-、ClO-、(OH-极少量) ( 三分子、三离子)
久置的氯水:
H2O、H+、Cl-、OH-(极少量)
氯水性质具有多样性,试指出下
列各现象主要是何种微粒所表现 出来的性质: ①氯水呈浅黄绿色__C_l_2__ ②使湿润的紫色石蕊试纸先变红 _H__+ _后褪色_H_C__lO_ ③滴加AgNO3溶液后生成白色沉 淀__C_l-
学习总结
经常不断地学习,你就什么都知道。你知道得越多,你就越有力量 Study Constantly, And You Will Know Everything. The More
You Know, The More Powerful You Will Be
现象:有色纸条不褪色 结论:干燥的氯气没有漂白性 结论:能确定氯水中存在:
H2O、Cl2、H+ 、ClHClO
H2O + Cl2 = HCl + HClO H2O + Cl2 = H++Cl- + HClO Cl2既是氧化剂又是还原剂
HClO的性质 弱酸性(比碳酸弱) 强氧化性(漂白性) 不稳定性(见光分解)
长芦盐场我国海盐产量最大的盐场,主要 分布于河北省和天津市的渤海沿岸,其中
以塘沽盐场规模最大,年产盐119万吨。
以NaCl为主要成分的食盐,至 今仍是人类惟一必须的食用盐。
氯气还对皮肤、衣物等具 有 强烈腐蚀、损毁作用
重庆发生氯气泄漏爆炸事故
能破坏环境、能剿灭触及 的所有生命——所有植物和 动物,尤其是动物致死率几 乎100%,只有天上能高飞的 鸟勉强得逃脱。
3)与水反应
氯气能溶于水(常温常压下, 1体积水约溶解2体积的氯气, 1:2), 氯气的水溶液叫氯水。 氯水因为溶有氯气而呈现黄绿色。
氯水中含有什么物质呢?
实验探究: 氯气与水反应产物以及氯水的成分
实验内容 Leabharlann 验现象 分析与解释观察氯水 颜色气味
浅黄绿色 有刺激性
有氯气 分子
气味
实验内容 实验现象 分析与解释
液氯是纯氯气加压 后液化所得
氯气的化学活泼性使 得它的毒性很强,可 损害全身器官和系统。
重庆天原化工总厂发生氯气泄漏事件
京沪高速公路淮安段 车祸发生液氯泄漏事 故共造成29人因氯 气中毒死亡,给当地 群众生命财产造成巨 大损失。
农田被氯气熏黄
历史事件
1915年4月22日下午5时,在第一次世界大战两军对 峙的比利时伊珀尔战场。趁着顺风,德军一声令下开启 了大约6000只预先埋伏的压缩氯气钢瓶。刹那间在68千 米宽的正面形成2米高的黄绿色气体幕墙滚滚向前推进, 纵深到达10-15公里,对手毫无防范,致使5千多人死亡, 一万五千多人中毒致伤。一位战地记者进行了如此描述: “他们已经死亡,两手伸展着好像要挥去上方的死神。 尸体遍野,他们极度痛苦的肺在喘息,满嘴都是黄色液 体。”这就是战争史上的第一次化学战,从此,化学战 作为最邪恶的战争被写入了人类战争的史册。这种气体 就是我们研究的氯气。
点燃
2Fe+ 3Cl2 ==== 2FeCl3
钠在氯气中燃烧, 发出黄色火焰,产生白烟
点燃
2Na + Cl2 === 2NaCl
Cu丝在Cl2中剧烈燃烧 有棕黄色烟产生
点燃
Cu+ Cl2 ====CuCl2
2)氯气与氢气反应
[实验4-3]在空气中点燃H2,然后把 导管伸入盛满Cl2的集气瓶中,
向氯水中
滴入
有白色沉
AgNO3溶 液和稀硝
淀产生 且不溶于
酸
稀硝酸
存在Cl-
实验内容 实验现象 分析与解释
向少量
Na2CO3粉 末中加入
有气泡
氯水
产生
存在H+
实验内容 实验现象 分析与解释
把有色纸
条放入盛 有色纸条 有漂白
有少量氯 褪色
性
水的试管 中
如何证明氯气分子有无漂白性?
实验:将干燥的有色纸条放入盛满氯气 的试管中,塞好塞子
第一次世界大战的伊普雷战役中,德国5分钟释放了 180吨氯气,使15000人中毒,三分之一的人死去。
材料一:第一次世界大战期间,德国军 队在与英法联军作战中,首次使用氯气 攻击对方,开了战争史上使用化学武器 的先例。
人类历史上第一次大规模使用化学武器
材料二:2007年4月25日 黑龙江 依兰一自来水厂发生氯气泄漏。
一、活泼的黄绿色气体—氯气
化学家舍勒 (瑞典)1742一1786
他测定过软锰矿(二氧化锰)的性质。 他用盐酸与软锰矿反应,发现了一种强 烈的刺鼻气味的黄绿色气体(C12)。
MnO2+4HCl(浓)==== MnCl2+2H2O+C12 ↑
1、氯气的物理性质
(1)黄绿色气体 (2)有刺激性气味、有毒 (3)密度比空气大 (4)易液化 (5)能溶于水(常温常压下,1 体积水约溶解2体积的氯气,1: 2)
第二节 富集在海水中的元素 ——氯
0.9%的生理盐水
生理盐水又名为0.9%氯化钠 注射液。人体体液中的Na+、 Cl-对于调节体液的物理和 化学特性,保证体内正常的 生理活动和功能发挥重要的 作用。
氯元素是最重要的成盐元素, 主要以NaCl的形式存在于海水和陆 地的盐矿中。据推测,海洋中含盐 3%,主要为NaCl,此外因还有MgCl2、 M不g能SO直4等接盐饮类用,。致海使洋海是水包既括咸N又aC苦l在, 内的巨大的资源宝库。如果将海洋 中的盐全部提取出来,铺在地球的 陆地上,可使陆地平均升高150m。
易液化的气体: 氯气101KPa、-34.6℃ SO2 101KPa、-10℃; NH3 101KPa、-33.35℃
氯元素的结构: Cl +17 2 8 7 得1e- Cl- +17 2 8 8 表现为典型的非金属性(氧化性)
2、氯气的化学性质 1)与金属反应,生成金属氯化物。
Fe丝在Cl2中剧烈燃烧 产生棕色的烟
2)氯气与氢气反应
现象: H2在Cl2中安静燃烧发出苍 白色火焰,瓶口有白雾. H2与Cl2混合后见光爆炸.
点燃或
H2 + Cl2 =光=照==2HCl
小结:氯气是一种化学性质活泼 的非金属单质,具有强氧化性。
初中所学的燃烧定义是怎样的?
物质与氧气发生发光发热的 剧烈的化学反应叫燃烧
定义:任何发光发热的剧烈 的化学反应叫燃烧
