第4章 旋光异构
有机化学练习题大全
绪论章节习题1.指出下列化合物中带“*"号碳原子的杂化类型:(1) (2)(3)(4)(5)(6)2.写出下列化合物的结构式:(1)(2)CH 3 CH 2 ―O―CH 2 CH 2 CH 3 (3)CH 3 CH 2 CH 2 CH 2 CH 3 (4)(5)CH 3 CH 2 ―O―CH(CH 3 ) 2 (6)(7) (8)3。
下列化合物各属于哪一类化合物? (1)(2)(3)(4)(5) (6)CH 3 ―NH 24.π键是怎样构成的?它有哪些特点?5。
下列化合物哪些易溶于水?哪些难溶于水? (1)CH 3 OH (2)CH 3 COOH (3)CCl 4 (4)(5)(6)CH 3 (CH 2)16 CH 36。
某化合物的实验式为CH,其相对分子质量为78,试推算出它的分子式.7.某化合物的相对分子量为80,其元素组成为:C45%,H7.5%,F47.5%.试推算出它的分子式。
8.下列化合物是否有偶极矩?如果有,请指出方向.(1)CH 2 Cl 2 (2)CH 3 Br (3)CH 3 ―0―CH 3(4)CH 3 CH 2 NH 2 (5)HCO 2 H (6)CH 3 CHO第二章开链烃章节习题1. 用系统命名法命名下列化合物,若是顺反异构体应在名称中标明构型。
(1)(C 2 H 5 ) 2 CHCH(C 2 H 5 )CH 2 CH(CH 3 ) 2 (2)(CH 3 CH 2 ) 2 CHCH 3 (3)(4)(5) (6)(7) (8)(9)(10)(11)(12)2。
写出下列化合物的结构式:(1)3-甲基—4—乙基壬烷(2)异己烷(3)2,3,4-三甲基—3-乙基戊烷(4)4-甲基-3-辛烯(5)2-甲基—3-乙基—3—辛烯(6)(E)—2-己烯(7)(Z)-3—甲基—2-戊烯(8)2,7—二甲基—3,5—辛二炔(9)(3顺,5反)-5-甲基-1,3,5-庚三烯(10)顺-3,4-二甲基-3—己烯3. 写出C 5 H 12 烷烃的所有一氯代衍生物。
5旋光异构
C2H5 C H CH3
C2H5
OH 异丙醇 CH3–CH–CH3 不是手性碳 OH CH3–CH–COOH
?
HO
OH H CH3
C
乳酸
[]25=+13.52 []25=-13.52 D D COOH COOH HO C H CH3 OH H CH3 []25=+2.6 D C
*
[]25=-2.6 D
第二节 物质的旋光性与分子结构的关系
一、分子的手性与旋光性 (一)手性与手性分子 1.手性——具有实物与镜像的关系,但不能完 全重叠的性质。 2.手性分子——当一个分子不存在对称因素时, 该分子的实物和镜象不能重合, 称为不对称分子,又称手性分子。 (二)物质的旋光性:凡是手性分子都有旋光性 旋光性 手性分子(不对称分子)
等量的左旋体和右旋体的混合物称为外消旋体,一 般用(±)或dl来表示。 m.p. []25 D 外消旋体与对映体的 比较(以乳酸为例):
( – )乳酸 53℃
(+)乳酸 (±)乳酸
-2.6
53℃ +2.6 18℃ 0
二 、旋光异构体构型的表示方法 ——费歇尔(Fisher)投影式 1.投影规则: (1)用“十”字交叉表示手性碳原子 (2) 碳链直立,命名中编号较小的基团放在上端 (3) ―十”字交叉中横键表示指向前方,竖键表示 指 向后方 常称为“横前竖后”:即横键朝前,竖键朝后 要求:1. 立体结构能用费歇尔投影式表示其构型 2.给出费歇尔投影式能想象出立体结构。
第三节 含一个手性碳原子化合物的旋光异构
一、对映体与外消旋体 1.对映体——互为实物体与镜象关系但不能完全重叠的 一对立体异构体。 含有一个手性碳原子的化合物一定是手性分子,有 两种不同的构型,是互为物体与镜象关系的立体异构 体,称为对映异构体(简称对映体)。 对映异构体都有旋光性,其中一个是左旋的,一个 是右旋的。所以对映异构体又称为旋光异构体。
有机化学答案

第1章 饱和烃(一)思考题部分思考题1-1写出分子式为C 6H 14烷烃的所有构造异构体。
CH 3CH 2CH 2CH 2CH 2CH 3CH 3CHCH 2CH 2CH 3CH 3CH 3CH 2CHCH 2CH 3CH 3CH 3CHCHCH 3CH 3CH 3CH 3CCH 2CH 3CH 3CH 3思考题1-2下列化合物哪些是同一化合物?哪些是构造异构体?同一化合物:(2)和(6);(3)、(4)和(5) 构造异构体:(1)、(2)和(3)思考题1-3用系统命名法命名下列化合物。
(1)2,2,4-三甲基戊烷 (2) 3,6-二甲基-4-乙基-5-丙基辛烷 (3)2,3,4-三甲基-5-乙基辛烷 思考题1-4写出下列化合物的构造式(1) CH 3CH 2CCH 2CH 3CH 3CH 3 (2) CH 3CCH 3CH 3CH CH 3CH 3(3) CH 3CHCH 2CH 2CH 3CH 3思考题1-5写出下列每一个构象式所对应的烷烃的构造式。
(1) CH 3CHCH 3CH 3(2)CH 3CHCH 2CH 3CH 3(3) CH 3CH 2CHCHCH 2CH 3CH 3CH 3思考题1-6写出下列化合物最稳定的构象式,分别用伞形式和Newman 投影式表示。
(1)C HCH 12 (2)C HCH 12思考题1-7比较下列各组化合物的沸点高低,并说明理由。
(1)正丁烷>异丁烷 (2) 正辛烷>2,2,3,3-四甲基丁烷(3) 庚烷>2-甲基己烷>3,3-二甲基戊烷理由:烷烃异构体中,直链烷烃的沸点比支链烷烃沸点高。
思考题1-8已知烷烃分子式为C 5H 12,根据氯代反应产物的不同,试推测各烷烃的结构并写出结构式。
(1)和(4):C CH 3H 3C CH 3CH 3(2) CH 3CH 2CH 2CH 2CH 3 (3)CH 3CH CH 2CH 3CH 3思考题1-9试写出分子式为C 6H 12的环烷烃的所有构造异构体并命名。
4第四章 旋光异构
H
H3C
C2H5
OH
Ⅲ
(4)若将其中一个费歇尔投影式的手性碳原子 上的任意两个原子或基团交换奇数次后,得到的投影 式和另一投影式相同,则这两个投影式表示两种不同 构型,二者是一对对映体。如下述化合物Ⅰ和Ⅳ表示 一对对映体:
CH3 H OH
C2H5
Ⅰ
-H和-CH3交换 第一次交换
H
H3C
OH在空间的两种排列
结论:如果分子在结构上是相同的,但旋 光活性不同,那么这种差别就只可能是原子或 基团在空间的排布不同,而且这两种空间排列 都是非对称的。也就是说,其分子具有手性。 如果这两种不同的排布互为实物和镜像不能重 叠,那么所对应的两种物质彼此间比旋光度大 小相等、方向相反。
C3 NH3
第二节 含手性碳原子化合物的旋光异构
一、含一个手性碳原子化合物的旋光异构 (一)对映体和外消旋体
2-氯丁烷分子中含一个手性碳原子,手 性碳原子上的四个基团在空间有两种不同的排 列方式,即有两种不同的构型 。
CH3
CH2CH3
CH Cl
CH3
H Cl
C
CH2CH3
这两种构型互为实物和镜像的关系,它们不 能完全重合,代表两个不同的异构体。这种互为 实物和镜像关系的异构体叫做对映异构体,简称 对映体。由于对映体的构造相同,因此其物理性 质、化学性质一般都相同。它们的区别在于光学 活性不同,其比旋光度大小相等,方向相反。一 对对映体中,一个是左旋体,另一个是右旋体。 但不能从构型上确定哪一个是左旋体或右旋体, 只能用旋光仪测得。
如果把两个对映体等量混合后,则左旋体和右旋 体的旋光能力相互抵消,不显示出旋光性。这种由等 量对映体组成的混合物叫做外消旋体,用(±)或 “dl”表示,如外消旋2-氯丁烷可记作(±)-2-氯丁 烷或dl-2-氯丁烷。
医本有机化学第4章旋光异构

3
OH COOH H CH3 R OH HO CH3 S COOH H
有21=2个旋光异构体,1对对映体 等量的对映体的混合物构成外消旋体。
六 手性碳与旋光异构体数目的关系
(二)含二个不同手性碳原子的化合物 * * CH3-CH-CH-CH3 Cl Br CH3 CH3 CH3 CH3 H H Cl Cl H H Cl Cl H Br H H Br H Br Br CH3 CH3 CH3 CH3 2R,3S 2R,3R 2S,3R 2S,3S IV II III I 对映体 对映体 非对映体 有22=4个旋光异构体,2对对映体,2个外消旋体
同一物
对映体
五
CHO H OH CH2OH
旋光异构体的命名
[O]
COOH H OH CH2OH
HNO2
1. D/L命名法(相对构型命名法)
COOH H OH CH2NH2
D-(+)甘油醛
NaNO2 + 2HBr
D-(-)甘油酸
COOH H OH Zn + HCl CH2Br
D-(+)异丝氨酸
COOH H OH CH3
(1)对称面(σ)
Cl C H C
H
Cl
具有对称面的分子无手性。
二 分子中常见的对称因素
(2)对称中心(i) 若分子中有一点P,通过P点画任何直线, 如果在离P等距离直线两端有相同的原子或基 团,则点P称为分子的对称中心。例如:
H H Br P Br COOH H H Br COOH H CH3 H H Br H H CH3
P
H H
H
有对称中心的分子没有手性。
旋光异构
。
纸面上转动90
。
=
对映体
(3)固定一个基团,另外三个基团按顺时针或逆时 针方向依次调换位置,构型保持不变。
COOH
固定羧基
COOH
其它依次调换位置
H CH3
OH
CH3 OH
H
(4)任意两个基团对调奇数次,构型变为其对映体。 任意两个基团对调偶数次,构型不变。
对映体间的区别
旋光方向相反,生理功能不一样。 例如: 1. 右旋葡萄糖具有营养价值,而左旋葡萄糖无营养。 2. 左旋氯霉素为抗菌消炎药,右旋氯霉素为无药效等。 3. 芬必得中的有效成分布洛芬,只是S-异构体有镇痛 作用。
CH3 (CH3)2CHCH2
* CHCOOH
布洛芬
4. 许多香料,对映异构体的气味很不相同。R-香芹酮 有清凉的留兰香气味,而S-香芹酮则有药草的气息。
IV
内消旋体:含有手性碳原子,但分子具有对称面而不 具有旋光性的化合物,用meso表示。
乳酸:一个手性碳原子----2个旋光异构体
氯代苹果酸:二个不相同手性碳原子---4个旋光异构体
酒石酸:二个相同手性碳原子----3个旋光异构体
旋光异构体数目跟手性碳原子数目有关。若含n个 不同的手性碳原子,则该化合物最多可以有2n个旋光 异构体,且有2n-1个外消旋体。
表6-2 氯代苹果酸的物理性质
二、含两个相同手性碳原子化合物的旋光异构
* * 例:酒石酸 HOOC-CH-CH-COOH的立体异构 OH OH
I
II
III
IV
(2R,3R)
(2S,3S)
(2R,3S)
(2S,3R)
旋光异构
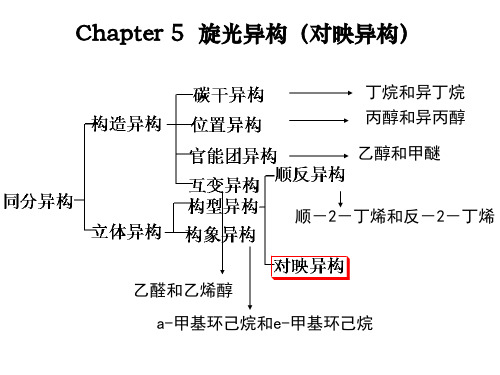
镜子 H H3C C Cl CH3 H3C H C Cl CH3
如果实物和它的镜像能够重合,则实物和镜像为同一物质, 并且没有对映异构体。为非手性分子。
手性和对映异构的关系
对映异构体的每一个都具有手性 手性分子肯定有对映异构体 手性(镜像的不重合性) 手性(镜像的不重合性)是产生对映异构现 象的充分必要条件! 象的充分必要条件!
镜子 COOH H C CH3 OH HO COOH C H
CH3
用费歇尔投影式表示为:
COOH H OH CH3
COOH HO H CH3
在费歇尔投影式中,规定横向的两个原子团在纸平面的前 面,竖向的两个原子团在纸平面的后面,横线和竖线的交 点代表手性碳原子。
朝纸面外
朝纸面内
根据费歇尔投影式判断手性碳原子的构型时,需要记住它的立 根据费歇尔投影式判断手性碳原子的构型时, 体形象。 体形象。 当最小的基团在竖线上,即在纸平面的后面时,直接根据另外 三个基团判断; 如果最小的基团在横线上,即在纸平面的前面,观察者应从纸 平面的后面往前看。若从纸平面的前面观察,根据另外三个基 团判断,观察到的构型与实际构型相反。 如果观察到为R,应改为S;如果观察到为S, 应改为R。
O H N O * O N O O H H N * O H N O O
R-型(不致畸)
S-型(致畸)
原因:生物体是手性环境
反应停” 被“反应停”夺去胳膊的孩子们
香芹酮 (香料)
O
O
S-Carvone caraway
R-Carvone spearmint
Dopa (药物)
HO H HO
COOH NH2
Cl F H H
H
.HF
Cl
第四章 立体异构
Cl
C CH3
C Br
CH3
C
C H
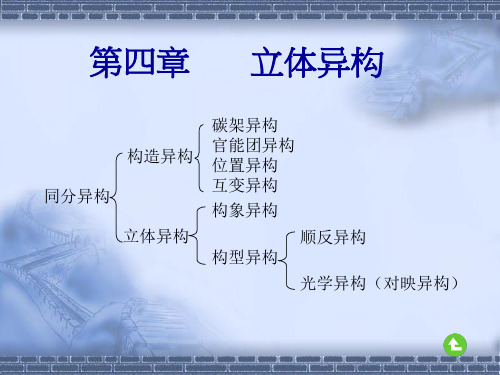
(E)- 2-氯-1-溴丙烯
(Z)- 2-氯-1-溴丙烯
2. 次序规则
(1)将与双键碳原子直接相连的原子按原 子序数大小排列,原子ቤተ መጻሕፍቲ ባይዱ数大者为“较优”基 团;若为同位素,则质量高者为“较优”基团。
I > Br > Cl > S > P > F > O > N > C > D > H
H C CH3
这种在有双键或环状结构的分子中,由于旋转受阻 使与双键或环相连接的原子或原子团在空间的排布方式不 同所引起的立体异构现象叫做顺反异构现象。各种异构 体互称为顺反异构,又称几何异构。
2.产生顺反异构的原因和条件
产生的原因:由于双键中的π键限制了σ键 的自由旋转,使得两个甲基和两个氢原子在空间 有两种不同的排列方式。
三、含一个手性碳原子的化合物的旋光异构
1.对映体和外消旋体 H3C
C
CH3 H HO
C
HOOC
H OH
COOH
乳酸的一对对映体(透视式) 对映体:互为实物和镜像关系的异构体叫做对 映异构体,简称对映体。
外消旋体;它们的等量混合物可组成一个外消 旋体,用(±)表示 。外消旋体无旋光性。
2.构型的表示方法
构象的两种表示方法
透视式
H
H H C H H C H H
H C H H H
C H
交叉式
重叠式
纽曼投影式:
H H H H
H H
H H
HH
H H
交叉式
重叠式
交叉式构象为优势构象
乙烷处于交叉式构象时,两个碳 上的氢原子相距最远,相互排斥力最 小,因而内能最低。重叠式构象内能 最高。但二者内能相差仅12.5kJ/mol, 室温时,分子热运动所提供的能量就 能使各个构象相互转化,因而不能分 离出乙烷的某一构象异构体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
OH Eye
OH Eye
C C 2H 5 H CH3
H
C CH3 C 2H5
(R)-2-丁醇
(S)-2-丁醇
R、S标记
直接根据Fischer投影式命名的简便方法介绍:
The end!
般用(±)来表示。 外消旋体与对映体的比较(以乳酸为例):
旋光性 物理性质 化学性质 生理作用
外消旋体 不旋光
对映体 旋光
mp 18℃
mp 53℃
基本相同
基本相同
各自发挥其左右
旋体的生理功能
4、 旋光异构体构型的表示方法
可用立体结构(楔形式和透视式)和费歇尔 (E· Fischer)投影式表示。
(1)立体结构式
平面偏振光:只在一个平面上振动的光,简 称偏振光。
1.2 旋光仪、旋光度、比旋光度
A B C D
A' B' A' 旋光性物质 D'
A
旋光仪示意图
乳酸
α
目镜(亮)
起偏镜
盛液管
检偏镜
旋光性:使偏振光偏振面旋转的能力。 旋光度:使偏振光偏振面旋转的角度。用表示。 旋光方向:右旋(+); 左旋(-). 有旋光性的物质叫旋光性物质或光活性物质。 手性化合物都具有旋光性。
一对立体异构体,互为对映异构体(简称对映体)。 对映异构体都有旋光性,其中一个是左旋的,一 个是右旋的。所以对映异构体又称为旋光异构体。
HO C H3C H COOH
OH HOOC C CH3 H
乳酸
判断对映体的方法有三种
(1)建造一个分子和它的镜像的模型, 如果两者不能重合,就存在对映体。 (2)如果分子有对称面或对称中心,那 么它和其镜像就能重合,就不存在对映体。
大
特点:R、S构型法,能表示分子的绝对的空间
关系,即:看见一个光活异构体的名字,就可写 出它的空间构型表达式。
COOH H C OH HO HOOC C H HOOC H HO C H H C H CH3 CH3 HO H H H HCOOH
R
S
R
R
注意:R、S构型不代表旋光性中的左旋。
比旋光度:在一定条件下,用一分米长的旋光管,待
测物质的浓度为1g· -1时测得的旋光度。 ml .
测定温度
旋光度( 旋光仪上的读数)
[ ]t = λ
比旋光度 波长 ( 钠光D)
L • C
溶液的浓度(g/ml)
盛液长度( 分米dm)
例如:在胆固醇的氯仿溶液中,浓度为260mg/5ml, 放入5cm长的盛液管中在室温(20℃)下测定其 旋光度为-2.5o,求它的比旋光度? [α]Dt=[α]D20=α/(L*c) =-2.5/(0.5dm*0.26g/5ml)=-96o
对称中心
Cl
H
有对称面和/或对称中 心的分子无手性,无 旋光性。
F
H H
F
H
Cl
一个分子不能与它的镜像重合的条件:一般是这 分子没有对称面,也没有对称中心。
2-溴丁烷
HO C H3C H COOH
OH HOOC C CH3 H
乳酸
手性碳原子:连有四个各不相同基团的碳原子。
(或称为手性中心)用C*表示。
3.2 构型标记
CH2OH
L-(-)- 甘油醛
注意事项:要用标准的Fischer投影式。 D/L命名法的使用有一定的局限性,它只适用与甘油 醛结构类似的化合物。目前,仍用于糖类和氨基酸 的构型命名 。D/L构型和旋光方向没有必然的联系。
2)R,S-命名法:
1. 与手性碳原子相连的四个原子或基的优先排列次序;
对映体
非对映体
对映体
3.4 含两个相同手性碳原子的化合物
2,3-二羟基丁二酸
COOH H HO OH H COOH (2R, 3R)-(+)酒石酸 HO H COOH H OH COOH (2R, 3S)-(-)酒石酸 H H COOH OH OH COOH (2R, 3S) meso-酒石酸 HO HO COOH H H COOH (2S, 3R)
子中有两个以上手性中心时,就有非对映异构现象。
两个非对映异构体:比旋光度不同,物理性质不
同,化学性质基本相同,但同一反应中,速率不同。
内消旋体与外消旋体的异同
相同点:都不旋光
不同点:内消旋体是一种纯物质,外消旋 体是两个对映体的等量混合物,可拆分开来。
酒石酸立体异构体的物理性质
熔点(℃) (—)酒石酸 (+)酒石酸 内消旋酒石酸 (±)酒石酸 170 170 140 206 溶解度(g) 139.0 139.0 125.0 20.0 旋光度() -12 +12 0 0
第4章
旋光异构
一、偏振光和比旋光度 二、物质旋光性与分子结构的关系 三、旋光异构体及其构型标记 四、外消旋体的拆分
碳链异构 位置异构 构造异构 官能团异构 异构现象 互变异构
.
立体异构
顺反异构 构型异构 旋光异构 构象异构
有机化合物质(生物分子)中存在着旋光异构现象。 生物体内的酶和各种底物具手性。
对映体
内消旋体 (不是手性分子)
非对映体
对映异构体之间性质比较:
1.旋光方向相反,其他物理性质(熔点、沸点等)相同
2.化学性质:在非手性环境下相同,在手性环境下, 反应速率不同,有时相差比较大。
3.生物生理性质:生物体立体选择性高。对于生物 体,一对对映异构体的作用可能正好相反。
非对映体:不呈物体与镜象关系的立体异构体。分
H OH CH2OH HO
CH2OH
H COOH
1 COOH HO H
CH2OH
2 OH HOCH2
H
COOH
3
4
以甘油醛为标准,人为规定: 1) D、L构型标记 羟基在碳链右边的为D型, 它的对映体为L型。
CHO H OH CH2OH D-(+)-甘油醛 HO CHO H COOH H2N H R L-氨基酸
掌握旋光异构现象的基本概念对生物学科尤为重要。
如:(1R,2R)-(-)-氯霉素有效,而其他对映体几乎无 效,它们的抗菌活性为100:0.4
1 偏振光和比旋光度
1.1 偏振光
光波是一种电磁波,振动方向垂直于光的传播方向。
晶轴 A B C D A' 普通光 Nicol棱镜 B' A' 平面偏振光 D' C' A
H C2H5 Cl CH3
旋转90°
C H3 H C2H5
旋转180°
C2H5 Cl Cl C H3 H
对映异构体
同一化合物
COOH COOH CH3 COOH 再对调一次 旋转180o HO H H OH HO H H OH 对调一次 在纸平面上 CH3 COOH CH3 CH3
R S R R
下列Fischer式是否表示同一化合物? COOH
•所有手性分子都有非对映体。
•所有具有手性碳的化合物都是手性分子。 具有R构型的手性化合物必定有右旋的旋 光方向。
•手性化合物必定含有手性碳原子。 •如果一个化合物没有对称面,它必然是手 性的。
•内消旋体和外消旋体都无旋光性,都是非 手性分子。 •构象异构体都没有光学活性。 •对映异构体可通过单键旋转相互重合。 •某光学异构体经化学反应后得到构型符号 相同的产物,因此反应过程中没有改变原 构型。 •每个对映异构体的构象只有一种。 •由一种异构体转变成其对映体时,必须断 裂与手性碳所连的键。
(3)如果一个分子有一个手性碳原子, 它就具有对映异构现象,有一对对映体。
2、对映体之间的异同点
(1)物理性质和化学性质一般都相同,比旋光度的 数值相等,仅旋光方向相反。
(2)在手性环境条件下,对映体会表现出某些不同 的性质,如反应速度有差异,生理作用的不同等。
3、外消旋体: 等量的左旋体和右旋体的混合物,一
凡是含有一个手性碳原子的有机化合物分子都具有 手性,是手性分子。
* CH3CH2CHCH3 OH
* CH3CH2CHCH2OH
CH3
CH3 C H HO C2H5 H5C2
CH3 C OH H
3 旋光异构体及其构型标记
3.1 含有一个手性碳原子的化合物 1、对映体:存在实物和镜像关系,又不能重叠的
3.3 含两个不相同手性碳原子的化合物
光学异构体数目 = 2n ; (n=不同手性碳原子数) 外消旋体数目= 2n-1
COOH H HO OH H CH2OH (2R, 3S)-2,3,4三羟基丁酸 HO H COOH H OH CH2OH (2S, 3R)-2,3,4三羟基丁酸 H H COOH OH OH CH2OH (2R, 3R)-2,3,4三羟基丁酸 HO HO COOH H H CH2OH (2S, 3S)-2,3,4三羟基丁酸
COOH 中 H OH 大 CH3 小 R-(-)-乳酸 CH2Cl 中 HOCH2 Cl HO CH3 S-(+)-乳酸 最小基在竖 HOCH2 Cl 键上,纸面 走向与实际 CH2Cl 走向相同. R-2,3-二氯丙醇 H COOH
最小基在横 H 键上,纸面 走向与实际 走向相反.
小
H S-2,3-二氯丙醇
a b ba
b C=C=C a
a b
a C=C=C b a
b
a b
ab
联苯型分子
及
丙二烯型
4 外消旋体的拆分
非手性化合物合成手性化合物时,在没有外界手 性因素的影响下,得到的总是外消旋体。其中的对应 异构体用常规物理方法难以分开。目前用于拆分的主 要方法有: 1)化学分离法:通过化学反应将对映异构体转化为非 对映异构体,以便利用其物理性质的差异进行分离; 2)生物分离法:利用酶的专一催化性消耗掉对映异构 体中的一个; 3)晶种结晶法:加入左旋或右旋的晶体,使与晶种相 同的异构体优先析出; 4)柱层析法:利用不同物质对同一吸附剂的 不同吸附作用分离混合物。选择适当的光学 活性吸附剂。
