L—丝氨酸溶解度的研究
丝氨酸检验标准操作规程

1.目的建立丝氨酸的内控质量标准,保证产品生产安全、质量稳定。
2.适用范围:本规程适用于芝麻提取物的质量评价与质量控制。
3.职责质量管理部负责本规程的实施。
4.感官检查4.1外观与性状:取适量本品,在自然光下,目视观察其为白色结晶或结晶性粉末;无臭、味甜。
4.2溶解性:取适量的本品溶于水中,乙醇、丙酮或乙醚中几乎不溶。
4.3鉴别实验取本品与丝氨酸对照品各适量,分别加水溶解并稀释制成每1ML中约含0.4MG的溶液,为供试品溶液与对照品溶液。
照其他氨基酸项下的色谱条件试验,供试品溶液所显主斑点的位置和颜色应与对照品溶液的主斑点相同。
5.干燥失重的测定5.1测定范围:<0.2%5.2 操作步骤:取本品,混合均匀(如为较大的结晶,应先迅速捣碎使成2MM以下的小粒),取约1G左右,置于本品相同条件下干燥至恒重的扁形称量瓶中,厚度不可超过5MM,在105℃干燥3小时,放入烘箱时应将瓶盖取下或将瓶盖半开进行干燥,至恒重,取出时,需将称量瓶盖盖好,放入干燥器中放冷,然后称定重量。
5.3结果计算干燥失重的质量分数W,按式计算:W=×100%式中 W1 为供试品的重量(G)W2为称量瓶恒重的重量(G)W3为(称量瓶+供试品)恒重的重量(G)。
6.炽灼残渣的测定6.1 测定范围:<0.1%6.2 操作步骤:取本品1.0G,置已灼烧至恒重的坩埚中,精密称定,缓缓灼烧至完全炭化,放冷;除另有规定外,加硫酸1ML使湿润,低温加热至硫酸蒸汽除尽后,在700℃灼烧使完全灰化,移置干燥器内,放冷,精密称定后,再在700℃灼烧至恒重,既得。
6.3 计算结果灼烧残渣的质量分数W,按式计算:炽灼残渣%=(W1-W2) / W3 ×100%式中 W1为(坩埚+供试品)恒重的重量(G),W2为坩埚恒重的重量(G),W3为供试品的重量(G)。
7. 酸度的测定7.1 测定范围:5.5~6.57.2 操作步骤:取本品0.30G,加新煮沸过的冷水30ML溶解,用PH酸度计测,最后读去PH值。
等电点氨基酸溶解度

等电点氨基酸溶解度氨基酸是生物体中的重要物质,它们构成蛋白质分子,在实现基因功能和生命活动过程中发挥着重要作用。
作为一种重要的生物分子,氨基酸的溶解度对蛋白质的生物学行为影响很大。
因此,对氨基酸的溶解度的研究和了解,对于更好地理解蛋白质的生物学行为和操作,也就是研究生物膜的功能,有着至关重要的意义。
等电点(特指载体蛋白质的等电点)是衡量蛋白质是否在溶解状态下的重要指标之一,因此,研究等电点氨基酸的溶解度对于分析蛋白质性质非常关键,也是蛋白质生物学研究中重要的科学问题之一。
氨基酸的溶解度主要受到pH值,温度,和化学活性物质的影响,特别是pH值的变化最为明显,也是影响氨基酸溶解度的最主要的因素。
首先,当pH值逐渐升高时,氨基酸的溶解度也会逐渐升高。
这主要是由于随着pH值的升高,氨基酸的能量变化减少,水的生成能量降低,从而使氨基酸更容易溶解。
其次,随着pH值的降低,氨基酸的溶解度也会逐渐降低,这主要是由于随着pH值的降低,氨基酸的能量变化增加,水的生成能量增加,从而使氨基酸溶解性降低。
此外,温度也会影响氨基酸的溶解度。
随着温度升高,氨基酸溶解度也会升高,这是由于温度升高,氨基酸的能量变化减少,水的生成能量降低,从而使氨基酸更容易溶解。
另外,一些化学活性物质也会影响氨基酸的溶解度,比如有机酸、碱、盐类等。
这些物质可以改变氨基酸的结构,从而影响它们的溶解性。
氨基酸的溶解度和蛋白质的等电点有着很大的关系,若氨基酸的溶解度太高,也就意味着蛋白质的等电点过低,这类蛋白质可能会因为结构不稳定而不能完全激活生物活性,同时,太低的溶解度也可能会使蛋白质的等电点过高,蛋白质的结构可能会受到影响,从而导致蛋白质的生物活性受到影响。
当研究蛋白质的功能性时,研究和分析氨基酸溶解度以及相关因素是非常有必要的,一是可以帮助理解蛋白质之间的相互作用,二是可以用来开发新的药物来治疗疾病。
由上所述,可以看出等电点氨基酸溶解度的研究对解释蛋白质的生物学行为和操作有着重要的意义,因此研究等电点氨基酸溶解度有着重要的实际意义。
丝氨酸

丝氨酸丝氨酸是一种非必需氨基酸,它在脂肪和脂肪酸的新陈代谢及肌肉的生长中发挥着作用,因为它有助于免疫血球素和抗体的产生,维持健康的免疫系统也需要丝氨酸。
丝氨酸在细胞膜的制造加工、肌肉组织和包围神经细胞的鞘的合成中都发挥着作用。
简介丝氨酸是一种非必需氨基酸,富含于鸡蛋、鱼、大豆,人体亦可从甘氨酸中合成丝氨酸。
丝氨酸在医药上有着广泛用途。
丝氨酸可促进脂肪和脂肪酸的新陈代谢,有助于维持免疫系统。
[1]L-丝氨酸产品说明英文名:L-Serine缩写:L-SerCAS No.:56-45-1EINECS号: 206-130-6[1]分子式:C3H7NO3结构式:CH2OHCH(NH2)COOH球棍模型结构式分子量:105.09等电点:5.68密度:1.53[2]熔点:240°C结构式:2描述白色结晶体或结晶粉末,味微甜,易溶于水和甲酸,不溶于乙醇和乙醚。
丝氨酸可以从大豆、酿酒发酵剂、乳制品、鸡蛋、鱼、乳白蛋白、豆荚、肉、坚果、海鲜、种子、乳清和全麦获取。
有必要的话,人体会从甘氨酸中合成丝氨酸。
磷脂酰丝氨酸(PS)是在人体中合成的丝氨酸化合物,意大利、斯堪的纳维亚半岛和其他欧洲国家都广泛应用磷脂酰丝氨酸补充剂来治疗年老引发的痴呆症和正常的老年记忆损失。
3标准质量标准-中国药典 2010Test Items项目Specification质量指标Assay 含量≥98.5%Characteristic性状无色结晶或结晶性粉末,味微甜Specific rotation[a]D比旋+14.0°~ +15.6°度Identification 鉴别AS PER CP2010PH酸度 5.5~6.5Transmittance溶液透光率≥98.0%Chloride氯化物≤0.02%Sulfate硫酸盐≤0.02% Ammonium铵盐≤0.02% Other amino acids其他氨基≤0.5%酸Loss on drying干燥失重≤0.2%Residue on ignition炽灼残≤0.1%渣Iron铁盐≤0.001% Heavy metals(as Pb)重金属≤10ppm Arsenic砷盐≤0.0001%Bacterial endotoxins细菌≤12 EU/g 内毒素主要功能:L-丝氨酸属于非必需氨基酸,具有许多重要的生理功能和作用1.合成嘌呤、胸腺嘧啶、胆碱的前体;2. L-丝氨酸羟基经磷酸化作用后能衍生出具重要生理功能的磷丝氨酸,是磷脂的主要成分之一;3. 具有稳定滴眼液pH值的作用,且滴眼后无刺激性;重要的自然保湿因子(NMF)之一,皮肤角质层保持水分的主要角色,高级化妆品中的关键添加剂。
项目五-L-丝氨酸的酶法合成及分析

姓名:候雅媛 班级:生药1311 学号:2013040808 组别:第4组
L-丝氨酸简介
L-丝氨酸的应用
仪器及试剂
试剂 甘氨酸、甲醛溶液、PLP、四氢叶酸 仪器 三角瓶、摇床
操作步骤
1、将菌种接入LB液体培养基,37℃摇床培养24小时。 2、 将培养物超声波破碎后离心取上清液。 3、 取已破碎的菌悬液,加等体积20mmoL/L PLP溶液。 4、 37℃摇床振荡温浴,然后向反应容器中,加100mL酶反应液。
操作流程
4.1、100mL酶反应液(含10mmoL/L甘氨 酸、13.3mmoL/L甲醛、0.4mmoL/L PLP、 5mmoL/L四氢叶酸、0.2mmoL/LS-硫基乙 醇、0.1mmoL/L磷酸盐溶液(pH8.0) 5、37℃空气浴摇床震荡反应30min,调 pH7.5。 6、加甲醛使其浓度达10mmoL/L,pH降 至7.22。 7、当上升至7.42后,加甲醛至7.22,反 复添加甲醛至反应液pH不随时间变化。 反应结束后,500r/min,离心10min上清 液待分析
谢谢观看!
L-丝氨酸的提取纯化
研究酶促反应液中L-丝氨酸的分离和反应液中甲醛、丝氨酸浓度的测定
方法:采用732树脂、717树脂离子交换柱层析从酶促反应液中分离甘氨酸、 L-丝氨酸;
采用铬变酸比色法测定甲醛和丝氨酸浓度.结果:两种树脂柱层析均可不 同程度地分离两种氨基酸,但717树脂柱的分离效果更好,丝氨酸的收率可 达77%. 结论:利用717树脂柱层析可从SHMT酶促反应液中成功地分离L-丝氨酸;铬 变酸比色法可用于测定酶反应液中甲醛浓度.
L-丝氨酸的分析
பைடு நூலகம்训器材
实训试剂
1、展层剂 正丁醇:冰醋酸:水=4:1:5充分摇 匀,用分液漏斗取上层液体做展开剂。 2、样品 L-丝氨酸标准样品、酶法合成的丝氨酸 样品 3、显色剂 0.5%茚三铜溶液
中科院科技成果——微生物直接发酵法生产L-丝氨酸

中科院科技成果——微生物直接发酵法生产L-丝氨酸
项目简介
L-丝氨酸(L-Serine,L-Ser)作为一种组成蛋白的基本氨基酸广泛应用于医药、食品、化妆品等行业。
此外,以L-Ser为原料还可以合成具有抗癌、抗艾滋、调节人体神经系统等不同效用的药物20余种。
目前L-Ser的全球市场需求量为10000吨/年以上,市场潜力巨大。
但与不断增大的L-Ser市场需求相比,L-Ser的生产技术较为落后。
目前,L-Ser的工业生产方法主要有蛋白水解法、化学合成法和酶转化法等,其中蛋白水解法存在工艺复杂、分离精制困难等缺点;化学合成法存在污染重、成本高、D-Ser与L-Ser分离困难等缺点;酶转化法存在转化率过低、前体物昂贵等难题。
因此尽快开发污染小、成本低、效率高的微生物直接发酵法生产L-Ser,显得极为重要。
中科院上海高等研究院生物炼制实验室经过近些年的研究积累,在微生物直接发酵法生产L-Ser关键技术上取得了重大突破,主要成果有:(1)通过分子改造大肠杆菌合成L-Ser的代谢途径,构建了L-Ser 的基因工程菌;(2)对该基因工程菌进行发酵培养基及发酵条件的优化;最终在发酵约40h后,L-Ser的产量达到30g/L以上,可用于工业化生产。
该项目具有自主知识产权。
L-色氨酸

L-色氨酸的生产及其代谢控制育种摘要本文综述了利用微生物生产L-色氨酸的各种方法和L-色氨酸的生物合成途径及其代谢调控机制,并介绍了利用重组DNA技术选育L-色氨酸高产菌的研究现状。
L-色氨酸是含有吲哚基的中性芳香族氨基酸,为白色或略带黄色叶片状结晶或粉末,水中溶解度1.l4g(25℃),溶于稀酸或稀碱,在碱液中较稳定,强酸中分解。
微溶于乙醇,不溶于氯仿、乙醚。
它是人体和动物生命活动中必需的氨基酸之一,对人和动物的生长发育、新陈代谢起着重要的作用,被称为第二必需氨基酸,广泛应用于医药、食品和饲料等方面。
在生物体内,从-色氨酸出发可合成5-羟基色胺等激素以及色素、生物碱、辅酶、植物激素等生理活性物质,可预防和治疗糙皮病,同时具有消除精神紧张、改善睡眠效果等功效。
色氨酸代谢失凋会引起糖尿病和神经错乱,因此在医学上被用作氨基酸注射液和复合氨基酸制剂。
另外,由于色氨酸是一些植物蛋白中比较缺乏的氨基酸,用它强化食品和做饲料添加剂对提高植物蛋白质的利用率具有重要的作用,它是继蛋氨酸和赖氨酸之后的第三大饲料添加氨基酸。
1.色氨酸的生产方法色氨酸的生产最早主要依*化学合成法和蛋白质水解法,但是随着对微生物法生产色氨酸研究的不断深入,这种方法已经走向实用并且处于主导地位。
微生物法大体上可以分为直接发酵法、微生物转化法和酶法。
近年来还出现了将直接发酵法与化学合成法相结合、直接发酵法与转化法相结合生产色氨酸的研究。
另外,重组DNA技术在微生物育种和酶工业上的应用极大地推动了直接发酵法和酶法生产色氨酸的工业化进程。
1.1微生物转化法亦称前体发酵法。
这种方法使用葡萄糖作为碳源,同时添加合成色氨酸所需的前体物如邻氨基苯甲酸、吲哚等,利用微生物的色氨酸合成酶系来合成色氨酸。
这种方法同直接发酵法一样,需要解除生物合成途径中大部分酶所受到的反馈调节,以使色氨酸能够高浓度蓄积。
另外,所添加的前体物大都是抑制微生物生长的,因此添加量不可过高,一般采取分批少量添加的方法。
氨基酸溶解性
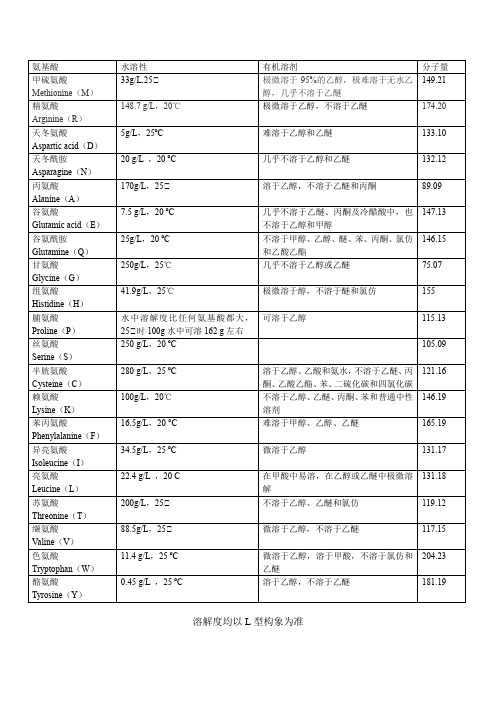
不溶于乙醇、乙醚和氯仿
119.12
缬氨酸
Valine(V)
88.5g/L,25℃
微溶于乙醇,不溶于乙醚
117.15
色氨酸
Tryptophan(W)
11.4 g/L,25 ºC
微溶于乙醇,溶于甲酸,不溶于氯仿和乙醚
204.23
酪氨酸
Tyrosine(Y)
0.45 g/L,25 ºC
氨基酸
水溶性
有机溶剂
分子量
甲硫氨酸
Methionine(M)
33g/L,25℃
极微溶于95%的乙醇,极难溶于无水乙醇,几乎不溶于乙醚
149.21
精氨酸
Arginine(R)
148.7 g/L,20℃
极微溶于乙醇,不溶于乙醚
174.20
天冬氨酸
Aspartic acid(D)
5g/L,25ºC
难溶于乙醇和乙醚
146.19
苯丙氨酸
Phenylalanine(F)
16.5g/L,20 °C
难溶于甲醇、乙醇、乙醚
165.19
异亮氨酸
Isoleucine(I)
34.5g/L,25ºC
微溶于乙醇
131.17
亮氨酸LΒιβλιοθήκη ucine(L)22.4 g/L,20 C
在甲酸中易溶,在乙醇或乙醚中极微溶解
131.18
苏氨酸
Threonine(T)
溶于乙醇,不溶于乙醚
181.19
溶解度均以L型构象为准
谷氨酰胺
Glutamine(Q)
25g/L,20 ºC
不溶于甲醇、乙醇、醚、苯、丙酮、氯仿和乙酸乙酯
146.15
毛发水解液中L丝氨酸的分离及相关分析检测方法的建立

华中科技大学硕士学位论文毛发水解液中L-丝氨酸的分离及相关分析检测方法的建立姓名:***申请学位级别:硕士专业:生物化工指导教师:余龙江;朱敏20070207摘 要L-丝氨酸具有许多重要的生理功能和作用,已广泛应用于医药、化妆品和 食品等领域。
但由于在工业化生产中分离提取难度较大,使其成为氨基酸配套生 产中的关键品种和高附加值产品。
本文旨在从除去胱氨酸和精氨酸的剩余毛发水解液中提取丝氨酸, 通过氨基 酸的综合利用,不仅可大力提高生产厂家的经济效益,而且减少环境污染。
首先,建立了一系列的氨基酸分析检测方法:莫尔法分析测定水解液中Cl - 离子浓度;纸层析法定性分析混合氨基酸的种类;茚三酮法定性分析氨基酸和定 量测定氨基酸含量;变色酸-分光光度法定量分析L-丝氨酸的含量;高效液相 色谱法在纸层析的基础上更精密准确地检测氨基酸。
并研究了不同的因素对测量 结果的影响,得出了合适的实验条件和规律。
其次,研究了盐分对氨基酸分离的影响,并提出了大孔强酸型阳离子交换树 脂脱盐的方法。
结果表明,L-丝氨酸在 717 型强碱性阴离子树脂上吸附交换随 着氯离子浓度的增大而逐渐减小,当溶液中氯离子浓度仅为0.2 mol/L时,丝氨 酸很难被交换吸附到树脂上。
而选用大孔强酸型阳离子交换树脂,控制 pH 值在 3.0左右时脱盐效果较好,脱盐率为95.51%时,氨基酸回收率达到84.13%。
本文最后确定了丝氨酸分离提取的工艺。
首先用717型强碱性阴离子交换树 脂分离出谷氨酸,然后对丝氨酸和苏氨酸进行铜氨络合化,在铜氨配位体交换柱 上达到分离,最后脱铜还原。
717型阴离子树脂的饱和吸附量为36.3g/Kg;谷氨 酸与717型阴离子树脂的亲和力较大,具有优先吸附的性质;通过717型阴离子 树脂分离,丝氨酸和苏氨酸的回收率达到 71.54%;氨基酸的侧链是氨基酸铜络 合物的交换过程中的关键因子, 此外氨基酸铜氨络合化的反应条件同时影响其分 离效果。
l-丝氨酸等电点

l-丝氨酸等电点
丝氨酸(Serine)是一种氨基酸,化学式为C3H7NO3。
它的等电点(isoelectric point,pI)是指在中性pH条件下,丝氨酸带有净电荷为零的状态。
具体的等电点值取决于该氨基酸的酸性和碱性基团的酸解离常数。
丝氨酸的等电点大约在5.68左右。
这是因为丝氨酸有两个离子化的基团:羧基(COOH)和胺基(NH2)。
在较低的pH条件下(酸性环境),羧基会失去一个质子,成为负离子(COO-),而胺基会保持带有正电荷(NH3+)。
在较高的pH条件下(碱性环境),羧基会保持带有负电荷(COO-),而胺基会失去一个质子,成为带有正电荷(NH2)。
在近中性pH条件下,丝氨酸的羧基和胺基净电荷相互抵消,达到零电荷状态,即等电点。
氨基酸溶解性

119.12
缬氨酸
Valine(V)
88.5g/L,25℃
微溶于乙醇,不溶于乙醚
117.15
色氨酸
Tryptophan(W)
11.4 g/L,25 ºC
微溶于乙醇,溶于甲酸,不溶于氯仿和乙醚
204.23
酪氨酸
Tyrosine(Y)
0.45 g/L,25 ºC
谷氨酰胺
Glutamine(Q)
25g/L,20 ºC
不溶于甲醇、乙醇、醚、苯、丙酮、氯仿和乙酸乙酯
146.15
甘氨酸
Glycine(G)
250g/L,25℃
几乎不溶于乙醇或乙醚
75.07
组氨酸
Histidine(H)
41.9g/L,25℃
极微溶于醇,不溶于醚和氯仿
155
脯氨酸
Proline(P)
水中溶解度比任何氨基酸都大,25℃时100g水中可溶162 g左右
可溶于乙醇
115.13
丝氨酸
Serine(S)
250 g/L,20 ºC
105.09
半胱氨酸
Cysteine(C)
280 g/L,25 ºC
溶于乙醇、乙酸和氨水,不溶于乙醚、丙酮、乙酸乙酯、苯、二硫化碳和四氯化碳
121.16
赖氨酸
Lysine(K)
100g/L,20℃
不溶于乙醇、乙醚、丙酮、苯和普通中性溶剂
溶于乙醇,不溶于乙醚
181.19
溶解度均以L型构象为准
133.10
天冬酰胺
Asparagine(N)
20 g/L,20 ºC
几乎不溶于乙醇和乙醚
132.12
丙氨酸
Alanine(A)
氨基酸基本的理化性质
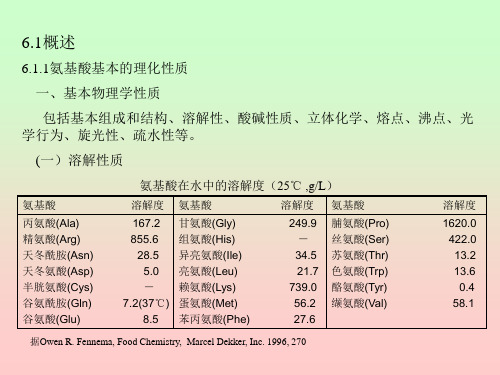
三、活性肽在食品中的应用
营养学研究证明,功能肽类在人体内的消化吸收明显优于蛋白质和单个氨基 酸,对人体内蛋白质的合成无任何不良影响,而且具有促进钙吸收、降血压、提高 免疫力等生理功能。此外,功能肽具有良好的水合性,使其溶解度增加,黏度降低、 胶凝程度减小,发泡性丧失,具有优良的加工性能。目前在食品中已经应用或出现 了应用苗头的功能肽主要有以下种类。
NH2 + RCH2CHCOOH
HSCH2CH2OH
S CH2CH2OH
N CHCOOH
(三)与荧光胺的反应 含有伯胺基的氨基酸、肽或蛋白质与荧光胺反应生成高荧光的衍生物, 在390nm时,在475nm具有最高的荧光发射。此法可被用于氨基酸、肽或蛋 白的定量分析。
COOH
O O O 荧 胺 光
NH2 + RCH2 CH COOH
R
+
产物
NH CH3
+
评论 蛋白放射性标
2
NH2
邻甲基异脲*,pH10.6,4℃,4d 乙酸酐 琥珀酸酐
R
R
NH C NH2 O
Lys转换成Arg 去除正电荷 在Lys上引入正
R
R
O
NH C CH 3
O NH C CH3
CБайду номын сангаасOH
NH C CH2 CH CH2 SH
硫代仲康酸**
在Lys残基引入
官能团及反应
R
产物同上 ROH+N2+H2O RCOOCH3+H2O RCH2OH 胺 RCH2SO3H RCH2SCH2CH2NH3+ RCH2SCH2COOH
R CH2 S CHCOOH CH2 COOH
酶法合成L_丝氨酸及反应液中氨基酸的分离_孙进

中 国 药 科 大 学 学 报Journa l of China Pharmaceutical University 2000,31(2):135~138酶法合成L-丝氨酸及反应液中氨基酸的分离孙 进 吴梧桐 吴 震1 高剑光1(中国药科大学微生物学教研室,南京210009)摘 要 含g ly A的基因工程菌所表达的SHM T可催化甲醛和甘氨酸特异地合成L-丝氨酸。
对酶法合成的部分条件进行了优化,并根据甲醛滴定的原理,确定了通过检测p H变化控制甲醛流加速度的方案,最终的反应液中L-丝氨酸浓度达0.2mo l/L。
反应结束后的酶反应液中同时含有甘氨酸和丝氨酸,利用国产717树脂获得较为理想的分离效果,丝氨酸的收率达77%,高效液相分析表明其中不含甘氨酸等杂质。
关键词 酶法合成;L-丝氨酸;甲醛;717树脂;分离 L-丝氨酸(L-Ser)在医药、化工、化妆品工业上有广泛的用途,它的生产方法有丝胶水解法、前体发酵法、化学合成法和酶法。
其中酶法系利用丝氨酸羟甲基转移酶(serine hydrom ethyltransferase, SHM T,EC.2.1.2.1)催化甲醛和甘氨酸(Gly)可逆地合成L-Ser,反应过程中SHM T需PLP和四氢叶酸(T HFA)作为其辅因子。
由于主要原料来源广泛、价格低廉,并可合成高浓度的产物,因此该法是目前最有应用前景的L-丝氨酸生产方法。
本文利用自行构建的含gly A的基因工程菌所表达的SHM T,对酶法合成L-丝氨酸的反应条件作了进一步优化。
反应结束后的酶反应液中含有甘氨酸和L-丝氨酸,由于这两种氨基酸等电点相近(pI G ly= 5.96, pI Ser= 5.69)、溶解度在L-丝氨酸稳定的温度范围内相差不大,所以两者的分离较一般的两种中性氨基酸分离要困难得多[1],我们利用国产717树脂研究了分离条件。
1 材 料1.1 菌种和培养基含g ly A的基因工程菌,中国药科大学微生物学教研室构建[2];LB培养基。
氨基酸基本的理化性质
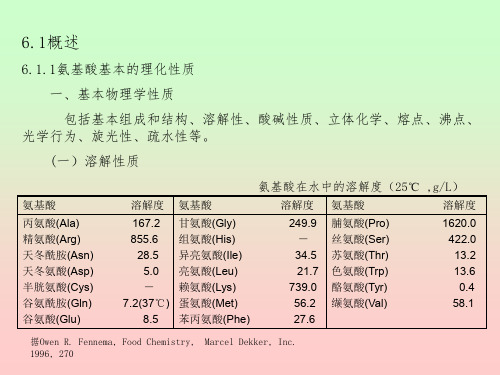
活性类型
抗菌肽 枯草菌素 乳酸链球菌素 Lactocin S 橡胶素 神经肽 脑啡肽 α -内啡肽 强啡肽 韩蛙皮素 激素肽及激素调节肽 催产素 促肾上腺皮质激素 加压素 Amylin 免疫活性肽 α -干扰素 白细胞介素-2 抗癌多肽 肿瘤坏死因子 环己肽
氨基酸数
未知 34 33 43
5 16 17 14
739.0 56.2 27.6
脯氨酸(Pro) 丝氨酸(Ser) 苏氨酸(Thr) 色氨酸(Trp) 酪氨酸(Tyr) 缬氨酸(Val)
1620.0 422.0 13.2 13.6 0.4 58.1
据Owen R. Fennema, Food Chemistry, Marcel Dekker, Inc. 1996, 270
(二)氨基酸的疏水性
氨基酸的疏水性,是影响氨基酸溶解行为的重要因素,也是影响蛋白 质和肽的物理化学性质(如结构、溶解度、结合脂肪的能力等)的重要因 素。
按照物理化学的原理,疏水性可被定义为:在相同的条件下,一种溶 于水中的溶质的自由能与溶于有机溶剂的相同溶质的自由能相比所超过的 数值。估计氨基酸侧链的相对疏水性的最直接、最简单的方法就是实验测 定氨基酸溶于水和溶于一种有机溶剂的自由能变化。
RCH2SCH2COOH
避免巯基氧 同上
苹果酸酐*****
R CH2 S CHCOOH CH2COOH
(250nm)
对汞代苯甲酸
R CH2SHg
COOH
测定巯基含量
官能团及反应
试剂和条件
产物
评价
含量
D.羟基 酯化
E.-SCH3(Met) 1.烷烃化
2.β -丙醇酸
N-乙基马来亚胺 DTNB******
氨基酸溶解性

33g/L,25C
极微溶于95%的乙醇,极难溶于无水乙
149.21
Methionine(M)
醇,几乎不溶于乙醚
精氨酸
Arginine(R)
148.7 g/L,20C
极微溶于乙醇,不溶于乙醚
174.20
天冬氨酸
Aspartic acid(D)
5g/L,25oC
难溶于乙醇和乙醚
在甲酸中易溶,在乙醇或乙醚中极微溶 解
131.18
苏氨酸
Threonine(T)
200g/L,25C
不溶于乙醇、乙醚和氯仿
119.12
缬氨酸
Valine(V)
88.5g/L,25C
微溶于乙醇,不溶于乙醚
117.15
色氨酸
Tryptophan(W)
11.4 g/L,25 oC
微溶于乙醇,溶于甲酸,不溶于氯仿和 乙醚
204.23
酪氨酸
Tyrosine(Y)
0.45 g/L,25 oC
溶于乙醇,不溶于乙醚
181.19
溶解度均以L型构象为准
133.10
天冬酰胺
Asparagine(N)
20 g/L,20 oC
几乎不溶于乙醇和乙醚
132.12
丙氨酸
Ala nine(A)
170g/L,25C
溶于乙醇,不溶于乙醚和丙酮
89.09
谷氨酸
Glutamic acid(E)
7.5 g/L,20 oC
几乎不溶于乙醚、丙酮及冷醋酸中,也 不溶于乙醇和甲醇
100g/L,20C
不溶于乙醇、乙醚、丙酮、苯和普通中性 溶剂
146.19
氨基酸

L-蛋氨酸价格比dl型的高很多,而两者生理活性相同。
L-组氨酸在水中溶解度远比盐酸盐低。
L-赖氨酸稳定性很差,一般用其盐类。
1、L-丙氨酸:白色结晶性粉末,有特殊甜味,甜度约为蔗糖的70%。
化学性能稳定,易溶于水,微溶于乙醇。
5%水溶液PH=5.5-7.0。
2、L-精氨酸:白色结晶性粉末,经水重结晶后,于105℃失去结晶水,水溶液呈强碱性,可从空气中吸收二氧化碳。
溶于水,微溶于乙醇。
成人为非必须氨基酸,但体内生成速度慢,婴幼儿为必须氨基酸,有一定解毒作用。
3、L-精氨酸盐酸盐:白色或近白色几乎无臭结晶性粉末。
干燥状态下稳定。
3%水溶液pH=5.7。
易溶于水,微溶于热乙醇。
4 、L-天冬氨酸:白色结晶性粉末,无臭。
稍有酸味,难溶于水,易溶于热水,不溶于乙醇,属非必须氨基酸。
5、L-天冬酰胺:白色结晶性粉末,稍有甜味。
遇碱水解成天冬氨酸。
溶于水,几乎不溶于乙醇,水溶液呈酸性。
为非必须氨基酸。
6、L-胱氨酸:白色针状,几乎无臭,在热碱水溶液中易分解,极难溶于水和乙醇。
为非必须氨基酸,对构成皮肤和毛发是必须物质,可促进手术及外伤的治疗,刺激造血功能,促进白血球生成。
7、L-谷氨酰胺:白色结晶性粉末,稍有甜味,结晶状态稳定,遇酸碱热水不稳定,可水解成L-谷氨酸。
溶于水呈酸性,几乎不溶于乙醇,属非必须氨基酸。
8、甘氨酸(氨基乙酸) :结晶性粉末,有特殊甜味,水溶液呈微酸性。
易溶于水,极难溶于乙醇。
9、L-组氨酸:稍有苦味,易与金属离子形成络盐。
溶于水,极难溶于乙醇。
因溶解度极小,常用其盐酸盐。
10、L-组氨酸盐酸盐:稍有酸、苦味,性质稳定。
易溶于水,在水中溶解度远比L-组氨酸大,不溶于乙醇。
属于必需氨基酸,在体内合成较慢,D-型与L-型生理效果相同。
11、DL-异亮氨酸:稍有苦味,10%溶液的pH=5.5-7.0,溶于水,几乎不溶于乙醇。
12 、L-异亮氨酸:略苦,无臭,10%溶液的pH=5.5-7.0,溶于水,化学性能稳定,加工受热时几乎无损失,微溶于热乙醇。
丝氨酸溶解度曲线

丝氨酸溶解度曲线丝氨酸是一种常见的氨基酸,广泛存在于生物体内。
它在生物体内起着重要的生理功能,比如促进骨骼和肌肉发育,参与免疫反应和酸碱平衡等。
而丝氨酸的溶解度则是指在一定温度下,单位溶剂中最大能溶解的丝氨酸的质量。
溶解度曲线是通过实验测定丝氨酸在不同温度下的溶解度而得出的,它可以反映丝氨酸在溶剂中的溶解特性。
实验方法:首先,准备一定浓度的丝氨酸溶液和一定体积的溶剂,比如水。
在某一温度下,向一系列烧杯中加入不同质量的丝氨酸溶液,并用玻璃棒搅拌均匀,使其完全溶解。
待溶液饱和后,停止加入丝氨酸溶液,并轻轻搅拌烧杯,观察是否有未溶解的固体。
若有未溶解的固体,则需要继续加入丝氨酸溶液,直到溶液饱和为止。
重复以上步骤,可以得到一组丝氨酸溶解度的数据。
将这些数据绘制成曲线,即为丝氨酸的溶解度曲线。
结果分析:丝氨酸溶解度曲线的形状是由多个因素共同决定的,其中包括溶剂的性质、温度的变化以及丝氨酸之间的相互作用等。
一般而言,在溶液中,丝氨酸分子与溶剂中的分子之间会发生吸引或斥力作用,同时丝氨酸分子之间也会相互作用。
这些作用力的强度会随着温度的升高或降低而发生变化,从而影响溶解度。
丝氨酸溶解度曲线通常呈现出“S”形状,即在开始的时候溶解度较低,在一定温度范围内溶解度迅速增加,然后在一定温度点达到最大值,再逐渐减小。
这是因为在低温下,溶剂分子之间的相互作用较强,丝氨酸分子很难与溶剂分子相互作用而溶解。
随着温度升高,溶剂分子的运动能力增强,溶剂分子与丝氨酸分子的吸引力减弱,导致溶解度增加。
当温度达到某一点时,丝氨酸分子与溶剂分子之间的相互作用达到动态平衡,溶解度达到最大值。
而在超过该温度后,溶解度开始减小,这是因为温度升高会破坏丝氨酸分子之间的相互作用,使溶解度降低。
影响溶解度的因素:1. 溶剂的性质:不同的溶剂对丝氨酸的溶解度有着不同的影响。
一般来说,极性溶剂对丝氨酸的溶解度较高,而非极性溶剂对丝氨酸的溶解度较低。
2. 温度的变化:温度是影响溶解度的主要因素之一。
l-高丝氨酸内酯盐酸盐标准

L-高丝氨酸内酯盐标准
一、盐种类
L-高丝氨酸内酯盐,也称为L-cysteine salt,是一种氨基酸盐,化学式为H2N-CH2-COOH,常温下为白色结晶或结晶性粉末,具有特殊气味。
二、盐纯度
L-高丝氨酸内酯盐的纯度应符合以下要求:
1. 游离氨基酸含量:≥98.5%
2. 氯化物含量:≤0.03%
3. 硫酸盐含量:≤0.01%
4. 铁含量:≤0.001%
5. 重金属含量:≤0.003%
6. 砷含量:≤0.0003%
7. 微生物指标:符合相关卫生标准
三、盐外观
L-高丝氨酸内酯盐应为白色结晶或结晶性粉末,无肉眼可见的杂质。
四、溶解性
L-高丝氨酸内酯盐易溶于水,在20℃时溶解度约为25g/100ml,易溶于氨水、碱溶液和极性有机溶剂。
五、咸味
L-高丝氨酸内酯盐具有轻微的咸味,是人体可接受的口感。
六、吸湿性
L-高丝氨酸内酯盐具有吸湿性,暴露在潮湿环境中容易吸湿潮解。
因此,应密封保存于干燥处。
七、水份
L-高丝氨酸内酯盐的水份应符合以下要求:
1. 加热减重法测定:≤12%
2. 卡尔·费休法测定:≤0.2%
八、硫酸盐
L-高丝氨酸内酯盐的硫酸盐含量应符合以下要求:
1. 硫酸盐含量(以SO4计):≤0.01%
2. 钡含量(以Ba计):≤0.001%
3. 钙含量(以Ca计):≤0.005%
4. 镁含量(以Mg计):≤0.002%。
