苯及同系物化学性质
【知识解析】苯的同系物

苯的同系物1 苯的同系物(1)概念芳香烃:分子中含有一个或多个苯环的烃类化合物叫芳香烃,苯是最简单的芳香烃。
苯的同系物:苯环上的氢原子被烷基取代所得到的一系列产物称为苯的同系物。
如等均为苯的同系物。
(2)苯的同系物的结构特点①分子中只有1个苯环。
②与苯环连接的全部是烷基(一个或多个)。
(3)苯及其同系物的通式为C n H2n-6(n≥6,n为正整数)。
名师提醒(1)苯的同系物的通式为C n H2n-6(n≥7,n为正整数),但符合通式C n H2n-6的烃不一定是苯的同系物,如的分子式为C10H14,但它不属于苯的同系物。
(2)苯的同系物由于所连侧链的不同和各个侧链在苯环上的相对位置的不同而具有多种同分异构体,如分子式为C8H10的苯的同系物有下列4种同分异构体:2 苯的同系物的物理性质(1)苯的同系物一般是具有类似苯的气味的无色液体,不溶于水,易溶于有机溶剂,密度比水的小。
(2)熔、沸点递变规律①随着分子中碳原子数的增加,苯的同系物的熔、沸点逐渐升高。
②对含相同碳原子数的苯的同系物的同分异构体来说,苯环上的支链数越多,熔、沸点越低;当支链数相同时,极性越小,熔、沸点越低。
如3种二甲苯的沸点:邻二甲苯>间二甲苯>对二甲苯。
3 苯的同系物的化学性质苯的同系物与苯都含有苯环,因此化学性质有相似之处。
(1)苯的同系物与苯的化学性质的相似之处①都能燃烧,燃烧时发出明亮的火焰并产生浓重的黑烟,其燃烧通式为C n H 2n -6+233O 2n n CO 2+(n -3)H 2O 。
②一定条件下都能与卤素单质发生卤代反应、与浓硝酸发生硝化反应等。
③都能与氢气发生加成反应。
名师提醒苯的同系物与卤素单质(X 2)发生取代反应时,其取代位置与反应条件有关:在催化剂作用下,取代的是苯环上的氢原子;而在光照条件下,取代的是侧链烷基上的氢原子。
如:(苯环上的氢原子被取代)(侧链烷基上的氢原子被取代)(2)由于苯环与烷基的相互作用,苯的同系物的化学性质与苯又有所不同。
苯的同系物的化学性质

02
还原反应过程中,苯环上的硝基、羰基等含氧官能团被还原成
氨基、羟基等官能团。
还原反应的发生条件和产物与苯环上取代基的性质和数量有关
03 。
CHAPTER 04
苯的同系物的应用
合成高分子材料
合成橡胶
苯的同系物可以作为合成橡胶的原料 ,如丁苯橡胶和氯丁橡胶等,具有优 良的弹性和耐久性。
合成纤维
苯的同系物可用于合成纤维,如聚酯 纤维和尼龙等,具有优良的耐磨性和 抗皱性。
发现潜在的健康问题。
THANKS
[ 感谢观看 ]
有机合成中间体
苯酚
苯的同系物可以转化为苯酚,苯酚是 许多药物和染料的中间体。
苯胺
苯的同系物可以转化为苯胺,苯胺是 许多染料和农药的中间体。
药物合成
抗癌药物
苯的同系物可以作为抗癌药物的合成原料,如顺铂和卡铂等铂类药物,具有广谱的抗癌 活性。
抗生素
苯的同系物可以作为抗生素的合成原料,如青霉素和头孢菌素等,具有抗菌消炎的作用 。
CHAPTER 05
苯的同系物的安全性
对人体的影响
致癌性
苯的同系物被认为是一种潜在的致癌物质。长期接触高浓度的苯同 系物可能导致人体患上癌症,特别是白血病和淋巴瘤等血液系统癌 症。
神经系统毒性
苯同系物对神经系统有毒性作用,长期接触可能导致头痛、头晕、 失眠、记忆力减退等神经系统症状。
免疫系统毒性
苯同系物可能影响人体的免疫系统,降低人体对疾病的抵抗力,增加 感染的风险。
对环境的影响
水污染
苯的同系物在水中不易分解,会 对水体造成污染,影响水生生物
的生存。
土壤污染
苯的同系物在土壤中不易降解,可 能对土壤造成污染,影响植物的生 长。
苯和苯的同系物

结 苯分子里不存在一般的碳碳单键、双键。它是
论
介于单键和双键之间的一种特殊的键。键长和 键角都相等。
或 平面正六边形,键角120º
苯分子中由于碳碳键的特殊性 :
既有C-C单键的性质-----取代反应; 又有C=C双键的性质------加成反应;
(但取代反应较加成反应容易)
用玻璃棒蘸一些苯,在酒精 灯上点燃,观察燃烧现象。源自-SO3H + H2O
苯磺酸
溴苯制备时,溴苯因溶解溴单质而显红褐色, 硝基苯制备时,硝基苯因溶解了NO2而显黄色。 考虑如何除去杂质,提纯分离上述有机物?
虽然苯不具有典型的碳碳双键所应有的加成反应 的性质,但在特定的条件下,苯仍然能发生加成反应 。
例如:在有镍催化剂存在和180~250℃的条件下,苯 可以与氢气发生加成反应,生成环己烷(C6H12)
(一)更易发生氧化反应,可被酸性KMnO4氧化。
CH3 +[O]
COOH
CH2CH3
+ [O]
COOH
C|H2CH3
+ [O]
| CH3
COOH
| |
COOH
╳ CH3
C-CH3 + [O]
CH3
考虑:根据以上事实总结苯同系物被高锰酸钾溶液氧化的条件 和氧化的规律?
注意:1、氧化条件:烷基上必须有α-H 。 2、规律:(1)不管烷基多大,只氧化含有H原子的α碳 (2)若苯环上有n个烷基,则氧化后得到n元酸。
几个重要的概念
1.芳香族化合物:含有苯环的化合物 2.芳香烃:含有苯环的烃 3.苯的同系物:苯环与烷基相连所构成的烃
1、只有一个苯环; 2、侧链是烷基;
4.稠环芳香烃:苯环之间共用两个碳原子而形成的烃。
苯及同系物

苯及其同系物的性质苯及其同系物:1、苯的结构:分子式:C 6H 6,最简式CH ,结构简式:(凯库勒式)结构特点:苯分子为平面结构,碳碳键的键长、键角均相等,键角120°,键长介于单、双键之间,苯分子中的键是一种独特的键,由一个大π键和6个键组成。
2、苯的性质物理性质:苯是一种无色、有特殊香味、易挥发的液体,熔点5.5℃、沸点80.5℃,当温度较低时凝结成无色晶体。
比水轻,难溶于水,是常用的有机溶剂,苯是重要的有机化工原料。
苯的化学性质:苯分子的特殊结构决定了苯分子稳定性,常温下苯不与溴水发生加成反应,也不能被酸性KMnO 4溶液所氧化,在一定条件下,苯能与Cl 2、溴单质、浓硝酸等发生反应。
⑴取代反应(与卤素单质、浓硝酸的取代): ⑵燃烧反应:⑶加成反应(与H 2加成)思考、哪些事实可证明苯分子中不存在单双键交替的结构? ①苯的邻位二元取代物只有一种 ②苯不能使溴水褪色③苯不能使酸性高锰酸钾溶液褪色④经测定,苯环上碳碳键的键长相等,都是1.40×10-10m ⑤经测定,苯环中碳碳键的键能均相等 3、苯的同系物:苯分子中的H 原子被烷基取代后的生成物,其分子通式为:C n H 2n -6(n ≥6),而芳香烃是指分子中有苯环的烃,它可以含有1个或多个苯环,苯的同系物属于芳香烃。
芳香族化合物是指分子里含有一个或多个苯环的化合物,它包括芳香烃和它们的衍生物。
苯的同系物的物理性质:苯的同系物一般为无色液体,具有特殊气味,有毒,难溶于水,密度比相对分子质量相近的烷烃及烯烃的大,但小于1,其中甲苯、二甲苯常用作有机溶剂.苯的同系物的化学性质苯的同系物中含苯环和烷基,二者共同影响,使苯的同系物的性质不是苯和烷烃的性质的简单相加。
苯的同系物的化学性质与苯相似。
①取代(比苯更容易,侧链对苯环的影响)甲苯与液溴的取代: a 、苯环上的取代 b 、侧链上的取代 α-H 的卤代例如:C 6H 5CH 3Cl 2C 6H 5CH 2ClC 6H 5CCl 3+C 6H 5CH 2CH 2光照C 6H 5CHBrCH 3HBr注1、需要光照或高温(与苯环上取代机理不同,条件不同);2、侧链有多个H ,反应发生在α-位。
苯的同系物性质及其污染防治

苯的同系物性质及其污染防治【摘要】苯是一种常见的化学物质,其同系物具有不同的性质,包括结构、毒性等方面。
苯的同系物对环境和人体健康都存在一定的风险,需要采取相应的污染防治措施。
本文通过对苯同系物性质进行分析,探讨了其毒性影响及相关防治技术。
同时介绍了苯的监测和控制方法,以及处理和处理技术。
在提出了苯同系物的综合管理措施,探讨了未来的污染防治方向,并提出了环境治理建议。
这些信息对于加强苯污染防治工作,保护环境和人类健康具有一定的指导意义。
【关键词】苯、同系物、污染、风险、性质、毒性、防治技术、监测、控制方法、处理技术、综合管理措施、环境治理建议、苯的环境治理、污染防治方向。
1. 引言1.1 苯的同系物概述苯的同系物是一类具有相似结构与性质的有机化合物,基本结构均为苯环,并在苯环上加入不同的官能团或取代基而形成。
苯的同系物包括甲苯、乙苯、二甲苯等,它们在工业生产、燃烧过程以及化学品的使用中普遍存在。
甲苯是最简单的苯的同系物之一,其结构与苯相似,但在苯环上加入一个甲基基团。
甲苯主要用于溶剂、涂料和染料的生产中,具有较高的挥发性,易挥发进入大气中造成空气污染。
乙苯是另一种常见的苯的同系物,其结构中加入一个乙基基团。
乙苯广泛应用于化工领域,用作溶剂或原料,但其毒性较大,长期接触可造成严重健康问题。
二甲苯则是在苯环上加入两个甲基基团而成的化合物,常用作溶剂和原料。
由于其毒性较高,二甲苯在使用过程中应注意防护和安全管理。
苯的同系物虽然在工业生产和日常生活中有广泛应用,但其挥发性、毒性与环境影响等问题也需引起重视和关注。
在污染防治中需要综合考虑各种同系物的特性,制定有效的监测和控制措施,以减少其对环境和人体健康的危害。
1.2 苯的污染风险苯是一种常见的有机化合物,其同系物具有较高的毒性和危害性。
苯的污染风险主要体现在以下几个方面:苯在大气中易于挥发,会通过空气传播到周围环境,对人体和其他生物造成危害。
长期暴露于苯污染环境中,可能导致呼吸系统疾病、神经系统问题甚至癌症等严重后果。
苯的同系物

1.苯的同系物:
苯的苯环上氢原子被烷基代替而得到的芳烃。 只含有一个苯环,且侧链为C-C单键的芳香烃。
2.通式:CnH2n-6 (n≥6)
CH3 |
CH2CH3 |
CH3 |
H3C H3C
CH3 | CH3 CH3 | CH3
| CH3
甲苯(C7H8) 乙苯( C8H10) 对二甲苯(C8H10)
ቤተ መጻሕፍቲ ባይዱ
CH3 | —C—CH3 | HOOC— CH3 | COOH
HOOC |
可用KMnO4酸性溶液作试剂鉴别苯的同系 物和苯、苯的同系物和烷烃。
⑵侧链影响苯环,使苯环邻对位上的氢易取代
CH3
CH3
CH3
NO2
2
+ 2 HNO3
浓硫酸
300C
+
+ 2 H 2O
NO2 对硝基甲苯
CH3 |
侧链影 响苯环 + 3HNO3
稠环 芳烃
烷烃、烯烃、炔烃、芳香烃的比较
有机物
代表物
烷烃
烯烃
炔烃
芳香烃
CH4
全部单键 饱和烃
C2H4
含碳碳双键不饱 和
C2H2
含碳碳叁 键不饱和
C6H6
特殊的键不 饱和
平面正六边形
结构特点
空间结构 物理性质 燃烧
正四面体 平面形 直线形 无色气体,难溶于水
无色液体
与溴水
KMnO4 主要反应类型
易燃,完全燃烧时生成CO2和H2O 不反应 加成反应 加成反应 不反应 不反应 氧化反应 氧化反应 侧链可氧化
①侧链影响苯环,使苯环上的氢原子比苯更易 被取代 ②苯环影响侧链,使侧链能被强氧化剂氧化
苯及苯的同系物的化学性质

一、苯的化学性质
1.氧化反应——燃烧反应
2C6H6+15O2
点燃
12CO2+6H2O
现象:火焰明亮,伴有浓烟。 注意:苯不能使酸性KMnO4溶液褪色, 也不与溴水反应,但苯能将溴从溴水中 萃取出来而使溴水褪色,是物理变化。
由于苯分子中的碳碳键是介于单键
和双键之间的独特的键,使苯在一定条
件下既能发生取代反应(与烷烃类似),
【练习1】关于苯的下列说法中不正确的是( D ) A.组成苯的12个原子在同一平面上 B.苯环中6个碳碳键键长完全相同 C.苯环中碳碳键的键能介于C-C和C=C之间 D.苯只能发生取代反应
【练习2】苯环结构中不存在碳碳单键与碳碳双 键的交替结构,下列可以作为证据的事实是( D ) ①苯不能使高锰酸钾酸性溶液褪色 ②苯不能使溴水因发生化学反应而褪色 ③苯在加热和有催化剂存在的条件下能还原成 环己烷 ④苯中碳碳键长完全相等 ⑤邻二氯苯只有一种 ⑥间二氯苯只有一种 A.①② B.①⑤ C.③④⑤⑥ D.①②④⑤
【练习6】下列关于甲苯的实验中,能说明侧 链对苯环有影响的是( A ) A.甲苯硝化生成三硝基甲苯 B.甲苯能使高锰酸钾酸性溶液褪色 C.甲苯燃烧带有浓厚的黑烟 D.甲苯与氢气可以发生加成反应
2.取代反应 (1)溴代反应。
冷凝水出口
冷凝水进口
NaOH溶液
碱石灰
苯和液溴 蒸馏水
铁粉
实验操作: a.连接好仪器,检查装置的气密性。 b.在三颈烧瓶中加入少量铁粉,向三颈烧瓶上 冷凝水的一个分液漏斗中加入5mL苯和1mL液 溴的混合物。 c.向另一个分液漏斗中加入30mL 10%的氢氧化 钠溶液。 d.在锥形瓶中加入蒸馏水,在干燥管中加入碱 石灰,通入冷凝水。 e.先向三颈烧瓶中加入苯和液溴的混合物,观 察三颈烧瓶和锥形瓶中出现的现象。 f.反应完毕,向三颈烧瓶中加入氢氧化钠溶液。
高中化学 最易错系列 苯和苯同系物的结构与性质

考点5 苯和苯同系物的结构与性质【考点定位】本考点考查苯和苯同系物的结构与性质,把握苯的同系物的性质以及基团的变化即可得到反应的规律,在苯的同系物中,由于侧链受苯环影响,易被氧化生成苯甲酸。
【精确解读】一、苯的化学性质1.苯的基本结构①分子式:C6H6;最简式(实验式):CH②苯分子为平面正六边形结构,键角为120°.③苯分子中碳碳键键长为40×10-10m,是介于单键和双键之间的特殊的化学键.④结构式:⑤结构简式(凯库勒式):2.苯的物理性质无色、有特殊气味的液体;密度比水小,不溶于水,易溶于有机溶剂;熔沸点低,易挥发,用冷水冷却,苯凝结成无色晶体;苯有毒.3.苯的化学性质(1)氧化反应:苯较稳定,不能使酸性KMnO4溶液褪色;也不能使溴水褪色,但苯能将溴从溴水中萃取出来.苯可以在空气中燃烧:苯燃烧时发出明亮的带有浓烟的火焰,这是由于苯分子里碳的质量分数很大的缘故.(2)取代反应①卤代反应:苯与溴的反应在有催化剂存在时,苯与溴发生反应,苯环上的氢原子被溴原子取代,生成溴苯.苯与溴反应:化学方程式:②硝化反应:苯与浓硝酸和浓硫酸的混合物水浴加热至55℃—60℃,发生反应,苯环上的氢原子被硝基取代,生成硝基苯.硝基苯,无色,油状液体,苦杏仁味,有毒,密度大于水,难溶于水,易溶于有机溶剂③磺化反应苯与浓硫酸混合加热至70℃-80℃,发生反应,苯环上的氢原子被—SO3H取代,生成苯磺酸.—SO3H叫磺酸基,苯分子里的氢原子被硫酸分子里的磺酸基所取代的反应叫磺化反应.④加成反应虽然苯不具有典型的碳碳双键所应有的加成反应的性质,但在特定的条件下,苯仍然能发生加成反应.例如,在有催化剂镍的存在下,苯加热至180℃-250℃,苯可以与氢气发生加成反应,生成环己烷,.二、苯的同系物1.物理性质简单的苯的同系物通常状况下都是无色液体、有特殊气味,不溶于水,并比水密度小,易溶于有机溶剂,其本身也是有机溶剂.2.化学性质苯的同系物的性质与苯相似,能发生取代反应、加成反应.但由于侧链的存在,使苯和苯的同系物的化学性质既有相似之处也有不同之处.(1)都能燃烧,发出明亮的带浓烟的火焰,其燃烧通式为C n H2n-6+3n−3O2nCO2+(n-3)H2O2(2)苯的同系物的苯环易发生取代反应(与卤素单质、硝酸、硫酸等).如:由此说明明苯的同系物的侧链对苯环有很大的影响,它能使苯环更易发生取代反应(3)苯的同系物的侧链易氧化:这个反应说明烷基侧链受苯环的影响,苯的同系物能被酸性KMnO4溶液氧化,所以可以用来区别苯和苯的同系物.【精细剖析】1.苯的同系物的性质以及基团的变化即可得到反应的规律,在苯的同系物中,由于侧链受苯环影响,易被氧化生成苯甲酸.2.芳香烃与苯的同系物的区别,分子中有且含有1个苯环,与苯分子间相差1个或n个CH2原子团的化合物属于苯的同系物。
苯及其同系物

苯是 无 色,有 特殊芳香 气味 的 液 体,密度 小于 水,易溶 于 有机溶剂 ,不溶于 水 ,熔点 5.5℃, 沸点80.1℃,易 挥发(密 封保存),苯蒸气 有 毒.
一、苯的结构和化学性质
1.苯的结构 苯分子具有 平面正六边形 结构。 苯环上的碳碳键不是由碳碳单键和 双键交替的,而是 6 个碳原子之间 的 键 完 全 相 同 , 是 一 种 介 于 单键和双键之间的独特的键 。
2.苯的化学性质
氧化反应 取代反应 加成反应
在空气 中燃烧
溴 代
硝 化
与氢气 加成
(1)可燃性:火焰明亮,带有浓烟 点燃 2C6H6+15O2→ 12CO2+6H2O
(2)苯跟卤素的取代反应
在有催化剂存在时,苯与液溴(剧毒 易挥发液体)发生反应,生成溴苯,溴 苯是无色液体,密度比水大。
1.苯和液溴混合后,需要加入催化剂 溴化铁或铁粉才能迅速反应 2.两种反应物均易挥发且有毒,均易 溶于有机溶剂 3.反应本身放热,不需要加热
2,4,6—三硝基甲苯简称三硝基甲苯,又 叫梯恩梯(TNT),是一种淡黄色的晶体, 不溶于水。它是一种烈性炸药,广泛用 于国防、开矿、筑路、兴修水利等。
(2)特性归纳
苯
甲苯
KMnO4
(H2SO4)
不反应
不反应
不反应,萃取 有FeBr3, 取代
被氧化,溶 液褪色
Br2(CCl4)
不反应
不反应,萃取 有FeBr3,取代; 光照,取代
(1)类比迁移
氧化反应
甲苯在空气中点燃:
2C7H8+9O2→ 7CO2+4H2O
加成反应
甲苯和氢气,镍作催化剂并加热:
CH3
苯及同系物的化学性质
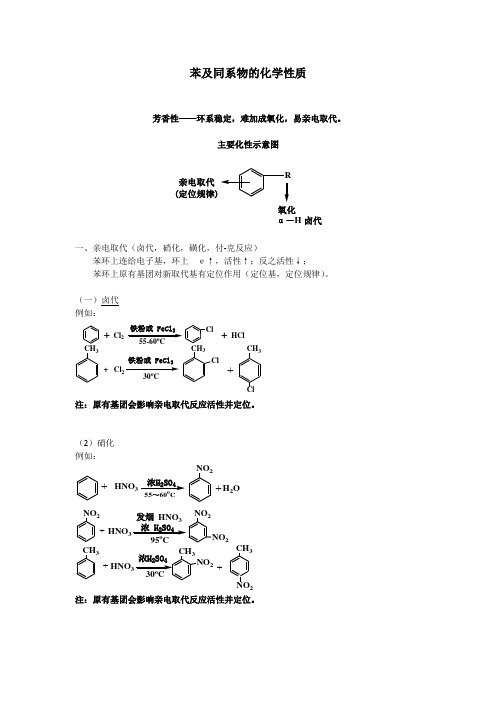
苯及同系物的化学性质芳香性——环系稳定,难加成氧化,易亲电取代。
主要化性示意图R亲电取代氧化(定位规律)α-H 卤代一、亲电取代(卤代,硝化,磺化,付-克反应)苯环上连给电子基,环上e↑,活性↑;反之活性↓; 苯环上原有基团对新取代基有定位作用(定位基,定位规律)。
(一)卤代 例如:+Cl 2o Cl+HClCH 3+Cl 铁粉或 FeCl 3CH 3CH 3+ClCl注:原有基团会影响亲电取代反应活性并定位。
(2)硝化 例如:+H 2O+HNO 3oNO 2浓H 2SO 4+HNO 3o NO 2浓 H 2SO 4NO 2NO 2发烟 HNO 3++HNO 330o CCH 3浓H 2SO 4CH 32CH 3NO 2 注:原有基团会影响亲电取代反应活性并定位。
例如:H 2SO++3H H 2O++H 2SO 4CH 3CH 3SO 3HCH 3SO 3H2479%CH3CH 3SO 3Ho(常用于合成)注:1、甲苯高温磺化主要进入对位;2、磺酸基可水解脱去,故常用于合成时“占位”。
(4)傅-克反应 ①烷基化 例如:+RCl3R+CH 3CH 2CH 2Cl+3)2CH 2CH 2CH 3(主)注:1、卤代烃基大于乙基常发生C +重排;2、吸电子基取代时,傅-克烷基化不可进行;3、Ph-Cl 、CH 2=CHCl 不能用作烷基化试剂(共轭使碳卤键强↑)。
4、其他方法的烷基化(先生成C +中间体,再亲电取代):+ CH 3CH=CH 2H 2SO 4CH(CH 3)2解:CH 3CH=CH 2H +CH 3CH 2CH 3+,……+ CH 3CHCH 2H 2SO 4CH(CH 3)2OH解:CH 3CHCH 3OH H +CH 3CH 2CH 3+CH 3CHCH 3OH2+-H 2O,……HClCH 3C O ClCO CH 3++AlCl 3乙酰氯 苯乙酮EtZn-Hg 浓HCl(克莱门森 rec.)CH 3+CH 3COOH +CH 3C OO AlCl 3CH 3C O CH 3OCH 3C乙酐 对甲基苯乙酮注:1、吸电子基取代时付-克酰基化不能进行;2、先进行酰基化再通过克莱门森反应还原羰基,也可在苯环上引入烃基;3、酰基化试剂一般选用活性较高的酰卤和酸酐。
苯及其同系物的结构和性质

苯及其同系物的结构和性质一、苯1.苯分子的结构苯的分子式,结构简式:,凯库勒式:,空间构型:,键角。
具有的键。
思考、哪些事实可证明苯分子中不存在单双键交替的结构①②③④2.苯的物理性质3.苯的化学性质:易取代,能加成,难氧化。
(1)取代反应:①卤化反应:②硝化反应:③磺化反应:(2)加成反应:(3)氧化反应:燃烧现象:4.苯的提取和用途将煤焦油在低温(170℃)条件下蒸馏可得苯,大量的苯可从石油工业中获得;常用于合成纤维、合成橡胶、塑料、农药、医药、染料、香料等。
苯也常用作有机溶剂。
二、苯的同系物1.定义芳香族化合物是分子里含有一个或多个苯环的化合物。
芳香烃:分子里含有一个或多个苯环的碳氢化合物属于芳香烃。
苯的同系物:凡分子里只含有一个苯环结构,且符合通式的所有芳香烃都是苯的同系物。
如甲苯、二甲苯等。
2.写出C8H10含苯环的同分异构体并命名3.苯的同系物化学性质与苯类似。
(1)取代反应①卤化反应:与溴蒸汽,光照与液溴,铁②硝化反应:(2)加成反应(3)氧化反应①可燃性②苯的同系物能使酸性KMnO溶液褪色。
苯环的侧链不论长短,4有几个侧链,就被氧化为几个羧基而成为羧酸。
(苯环所连的侧链的碳原子上必须有氢)CH COOH如:三、烃的结构特点和鉴别方法四、烃的分类烃烃的风雷6.取代反应断键规律(1)卤代反应断键规律:断C-H键(A)烷烃的卤代反应条件:光照、溴蒸汽(纯态)方程式:(B)苯的卤代反应条件:催化剂(Fe3+)、液溴方程式:(C)苯的同系物的卤代反应条件:催化剂、液溴方程式:原因:苯环上的邻、对位上的氢原子受侧链的影响而变得活泼。
(2) 硝化反应断键规律:断C-H键(A)苯的硝化反应条件:浓硫酸作催化剂,吸水剂,水浴加热到55℃-60℃。
方程式:(B)苯的同系物的硝化反应条件:浓硫酸作催化剂,吸水剂。
加热。
方程式:原因:苯环上的邻、对位上的氢原子受侧链的影响而变得活泼。
(3)磺化反应断键规律:断C-H键反应条件:水浴加热到70℃-80℃方程式:7.以苯的实验为基础的有机实验网络(1)溴苯制取实验——长导管的作用——带有长导管的实验:(2)硝基苯的制取实验——水浴加热——需水浴加热的实验:等。
苯及其同系物的化学性质

苯及其同系物的化学性质苯及其同系物的化学性质苯是一种无色、有臭味的芳香烃化合物,它是最简单的芳香烃,分子式为C6H6,结构式为六个碳原子构成一个环,并且每个碳原子均连接一个氢原子。
苯分子中的每个碳原子都是 sp2 混合轨道形成的,使苯分子呈现平面六角形的构象。
苯的芳香性质非常强,并且容易进行反应,具有很多重要的化学性质。
1. 加成反应苯可以进行加成反应,与一些烯烃和亚烷基烯烃发生加成反应,生成环烷烃。
例如,苯与丙烯发生加成反应,生成环己烷:CH2=CHCH3 + C6H6 → C6H11CH3苯还可以与乙烯发生加成反应,生成环己烯:C2H4 + C6H6 → C6H5CH=CH22. 取代反应苯可以发生取代反应,即通过原子或基团的取代,使苯环上的氢原子被取代。
取代反应的速度和方向性受到取代基的影响。
如苯环上的氢原子可以被取代成三氯甲基,得到三氯甲基苯:C6H6 + CHCl3 → C6H5Cl + HCl苯还可以发生烷基取代反应,烷基丁醇或溴丁烷与苯反应,可以得到取代的苯:C6H6 + CH3CH2CH2OH → C6H5CH2CH2OH + H2O3. 烷基化反应苯还可以发生烷基化反应,在高温下将苯和氯甲烷(或溴甲烷)进行反应,可以得到苯甲烷(或叔丁基苯):C6H6 + CH3Cl → C6H5CH3 + HCl4. 氧化反应苯可以发生氧化反应,例如,苯可以被空气中的氧气氧化,生成苯酚:C6H6 + O2 → C6H5OH苯还可以与过氧化氢反应,生成苯醌:C6H6 + H2O2 → C6H5O2H5. 磺酸化反应苯可以发生磺化反应,通过磺酸的取代,使苯分子上的氢原子转化为苯基磺酸基,成为磺酸苯。
例如,苯可以与浓硫酸反应,生成苯磺酸:C6H6 + H2SO4 → C6H5SO3H6. 氢气化反应苯可以发生氢气化反应,苯和氢气在催化剂的催化下,发生氢化反应,得到环己烷。
C6H6 + 3 H2 → C6H12同系物的化学性质苯是一类六元环上带有不同取代基的芳香烃,因此苯的同系物存在着不同的取代基,具有不同的物理化学性质和化学性质。
苯及其同系物的化学性质

烷基 苯基
◇ 结构: ① 苯的同系物是烷烃和苯的结合 ② 烷基和苯基之间相互影响
◇ 性质: ① 苯的同系物化学性质与烷烃和苯 相似 ② 苯的同系物化学性质有其独特性
◇ 取代反应
苯及其同系物的性质
① 苯的结构与价键特点 ② 苯的化学性质 ③ 苯的同系物的化学性质
◇ 物理性质: 无色、有特殊气味的有毒液体,难溶于水,
密度比水小。用冰冷却,可凝成无色晶体。
法拉第
苯凝成晶体
分子式:C6H6
热拉尔
结构简式:
凯库勒
结构特点:6个C和6个H均在同一平面
苯分子高度对称
分子式:C6H6 Ω=4
铁粉
问题2:如何提纯溴苯?
AgNO3溶液
溴苯的制取实验装置
◇ 取代反应(硝化反应)
浓硫酸
+ HO-NO2 50-60℃
+ H2O
① 反应温度控制在50~60℃,需水浴加热 ② 苯分子中H被-NO2取代的反应叫硝化反应 ② 温度高于70℃会发生副反应
苯
浓HNO3 浓H2SO4
注意事项: ① 温度计水银球的位置; ② 长导管的作用; ③ 浓硫酸的作用。
大π键
易取代,难加成
◇ 取代反应 + Br2 FeBr3
Br
+ HBr
溴苯(无色液体,密度大于水)
① 苯与溴水“只萃取,不取代”; ② 催化剂FeBr3可用Fe粉代替。
◇ 溴苯的制取
【实验现象】
① 导管口出现白雾;
② AgNO3溶液中出现浅黄色沉淀; ③ 烧瓶底部有褐色不溶于水液体。
液溴
苯及其同系物的结构和性质

苯及其同系物的结构和性质苯及其同系物的结构和性质⼀、苯1.苯分⼦的结构苯的分⼦式,结构简式:,凯库勒式:,空间构型:,键⾓。
具有的键。
思考、哪些事实可证明苯分⼦中不存在单双键交替的结构?①②③④2.苯的物理性质3.苯的化学性质:易取代,能加成,难氧化。
(1)取代反应:①卤化反应:②硝化反应:③磺化反应:(2)加成反应:(3)氧化反应:燃烧现象:4.苯的提取和⽤途将煤焦油在低温(170℃)条件下蒸馏可得苯,⼤量的苯可从⽯油⼯业中获得;常⽤于合成纤维、合成橡胶、塑料、农药、医药、染料、⾹料等。
苯也常⽤作有机溶剂。
⼆、苯的同系物1.定义芳⾹族化合物是分⼦⾥含有⼀个或多个苯环的化合物。
芳⾹烃:分⼦⾥含有⼀个或多个苯环的碳氢化合物属于芳⾹烃。
苯的同系物:凡分⼦⾥只含有⼀个苯环结构,且符合通式的所有芳⾹烃都是苯的同系物。
如甲苯、⼆甲苯等。
2.写出C8H10 含苯环的同分异构体并命名3.苯的同系物化学性质与苯类似。
(1)取代反应①卤化反应:与溴蒸汽,光照与液溴,铁②硝化反应:(2)加成反应(3)氧化反应①可燃性②苯的同系物能使酸性KMnO4溶液褪⾊。
苯环的侧链不论长短,有⼏个侧链,就被氧化为⼏个羧基⽽成为羧酸。
(苯环所连的侧链的碳原⼦上必须有氢)CH COOH 如:三、烃的结构特点和鉴别⽅法四、烃的分类烃烃的风雷6.取代反应断键规律(1)卤代反应断键规律:断C-H键(A)烷烃的卤代反应条件:光照、溴蒸汽(纯态)⽅程式:(B)苯的卤代反应条件:催化剂(Fe3+)、液溴⽅程式:(C)苯的同系物的卤代反应条件:催化剂、液溴⽅程式:原因:苯环上的邻、对位上的氢原⼦受侧链的影响⽽变得活泼。
(2) 硝化反应断键规律:断C-H键(A)苯的硝化反应条件:浓硫酸作催化剂,吸⽔剂,⽔浴加热到55℃-60℃。
⽅程式:(B)苯的同系物的硝化反应条件:浓硫酸作催化剂,吸⽔剂。
加热。
⽅程式:原因:苯环上的邻、对位上的氢原⼦受侧链的影响⽽变得活泼。
苯的同系物的知识点总结

苯的同系物的知识点总结一、苯的结构与性质苯是一种无色、具有特殊芳香气味的有机化合物。
其化学式为C6H6,分子结构为一个具有六个碳原子的碳环,每个碳原子与相邻的碳原子之间都连接有一个氢原子。
苯具有很高的稳定性和芳香性,是一种重要的有机溶剂和化工原料。
苯的稳定性主要体现在其芳香性上。
苯环的结构中存在π-电子系统,使得苯环上的所有C-C键都具有同样的键长,呈现出等价性,因此苯环的结构比较稳定。
由于芳香性的存在,苯环上的碳-碳键也是平面构型的,且苯环上的电子密度均匀分布,使得苯环对电子云的能级差异相对较小,因此苯分子对外部的电子云也有较好的亲和性。
苯的特殊性质主要包括其稳定性和芳香性。
稳定性使得苯是一种重要的有机溶剂,可用于溶解许多有机化合物。
芳香性使得苯可以发生许多特殊的化学反应,例如亲电取代反应、亲核取代反应、氧化反应等。
二、苯的同系物及其特性苯的同系物是指化学式和苯相同,但是分子结构略有不同的一类有机化合物。
根据苯的结构特点,我们可以将苯的同系物分为以下几类:1. 单一取代苯单一取代苯是指苯环上的一个或多个氢原子被同一种官能团所取代得到的化合物。
常见的单一取代苯有苯甲醛、苯甲酸、苯酚等,它们分别是苯环上一个氢原子被CHO、COOH、OH官能团取代而得到的化合物。
这些单一取代苯的特点是它们对苯的芳香性和稳定性产生一定的影响。
2. 二取代苯二取代苯是指苯环上的两个不同位置的氢原子被同一个或不同的官能团取代而得到的化合物。
常见的二取代苯有对二甲苯、间二甲苯、邻二甲苯等,它们分别是苯环上两个不同位置的氢原子被CH3官能团取代而得到的化合物。
二取代苯的特点是它们在空间构型上存在不对称现象,因此在一些化学反应中会表现出不同的活性。
3. 多取代苯多取代苯是指苯环上的多个位置的氢原子被不同的官能团取代而得到的化合物。
常见的多取代苯有甲基苯、对二甲苯、苯甲酸甲酯等,它们分别是苯环上多个位置的氢原子被不同的官能团取代而得到的化合物。
课件 苯_苯的同系物及其性质

()
A.15种
B.16种
C.17种
D.18种
【解题指南】解答本题需注意以下两点:
(1)含有羧基的C8H8O2的芳香族化合物的同分异构体; (2)利用等效氢原理确定一氯代物的数量。
【解析】选C。能与NaHCO3反应生成CO2,说明含有羧基,当苯环上有两个取 代基时,分别为—CH3、—COOH,可取代的不同氢原子的位置有:
、
、
;当苯环上只有一个取代基时,可取
代的不同氢原子的位置有:
,所以该化合物连在碳原子上的氢原子被
氯原子取代后的一氯代物共有5+5+3+4=17种,C项正确。
【规律方法】苯的同系物的同分异构体 (1)烷基的类别与个数,即碳链异构。 (2)若有2个侧链,则存在邻、间、对三种位置异构。若有3个侧链则存在邻、偏、 均三种位置异构。
结构简式
侧链烃基
上一氯代
2
1
物种数
1
1
苯环上 一氯代 物种数
一氯代物 种数
乙苯 3 5ຫໍສະໝຸດ 邻二甲苯 2间二甲苯 3
对二甲苯 1
3
4
2
3.蒽(
)和菲(
)是何种关系?二者的一氯代物分别是多少
种?
提示:蒽和菲的分子式相同,均为C14H10,二者互为同分异构体。蒽的一氯代物 有3种,菲的一氯代物有5种:
。
4.萘(
(2)苯的同系物的组成和结构特点: ①苯的同系物是苯环上的氢原子被_烷__基__取代后的产物,其分子中只有一个 _苯__环__,侧链都是_烷__基__,分子组成通式为_C_n_H_2_n_-6_(_n_>_6_)。
②分子式C8H10对应的苯的同系物有4种同分异构体,分别为
苯及同系物

苯及其同系物的性质苯及其同系物:1、苯的结构:分子式:C 6H 6,最简式CH ,结构简式:(凯库勒式)结构特点:苯分子为平面结构,碳碳键的键长、键角均相等,键角120°,键长介于单、双键之间,苯分子中的键是一种独特的键,由一个大π键和6个键组成。
2、苯的性质物理性质:苯是一种无色、有特殊香味、易挥发的液体,熔点5.5℃、沸点80.5℃,当温度较低时凝结成无色晶体。
比水轻,难溶于水,是常用的有机溶剂,苯是重要的有机化工原料。
苯的化学性质:苯分子的特殊结构决定了苯分子稳定性,常温下苯不与溴水发生加成反应,也不能被酸性KMnO 4溶液所氧化,在一定条件下,苯能与Cl 2、溴单质、浓硝酸等发生反应。
⑴取代反应(与卤素单质、浓硝酸的取代): ⑵燃烧反应:⑶加成反应(与H 2加成)思考、哪些事实可证明苯分子中不存在单双键交替的结构? ①苯的邻位二元取代物只有一种 ②苯不能使溴水褪色③苯不能使酸性高锰酸钾溶液褪色④经测定,苯环上碳碳键的键长相等,都是1.40×10-10m ⑤经测定,苯环中碳碳键的键能均相等 3、苯的同系物:苯分子中的H 原子被烷基取代后的生成物,其分子通式为:C n H 2n -6(n ≥6),而芳香烃是指分子中有苯环的烃,它可以含有1个或多个苯环,苯的同系物属于芳香烃。
芳香族化合物是指分子里含有一个或多个苯环的化合物,它包括芳香烃和它们的衍生物。
苯的同系物的物理性质:苯的同系物一般为无色液体,具有特殊气味,有毒,难溶于水,密度比相对分子质量相近的烷烃及烯烃的大,但小于1,其中甲苯、二甲苯常用作有机溶剂.苯的同系物的化学性质苯的同系物中含苯环和烷基,二者共同影响,使苯的同系物的性质不是苯和烷烃的性质的简单相加。
苯的同系物的化学性质与苯相似。
①取代(比苯更容易,侧链对苯环的影响)甲苯与液溴的取代: a 、苯环上的取代 b 、侧链上的取代 α-H 的卤代例如:C 6H 5CH 3Cl 2C 6H 5CH 2ClC 6H 5CCl 3+C 6H 5CH 2CH 2光照C 6H 5CHBrCH 3HBr注1、需要光照或高温(与苯环上取代机理不同,条件不同);2、侧链有多个H ,反应发生在α-位。
苯及笨的同系物

苯及笨的同系物苯(苯环:C 6H 6)芳香烃包括苯的同系物(通式:C 6H 2n-6)稠环芳烃(高中不学)一、 苯 1.A. 化学式:C 6H 6,结构式:CH 。
(碳碳或碳氢)键角:120°,苯分子中的碳碳键是一种介于碳碳单键和碳碳双键之间的特殊的共价键。
苯中无碳碳单键、碳碳双键。
2. 苯的物理性质A. (苯实际B. 可进行)③主要生成物:溴苯(无色比水重的油状液体,实验室制得的溴苯由于溶解了溴而显褐色)(苯环上的氢原子被溴原子取代,生成溴苯。
溴苯是无色液体,密度大于水)在有催化剂存在的条件下,苯可以和液溴发生取代反应,生成溴苯。
(所以苯和溴水不反应) 苯的卤代反应——苯环上的氢原子被卤原子(X)取代。
说明:①X 2须用纯的单质,不能用卤素(X 2)的水溶液。
②苯的卤代反应产物一般只考虑其—取代的产物,而不同于烷C C C C C CH H HH H H烃的卤代反应产物—多种多元卤代烃同时共存。
③苯环上一个氢原子被取代时,仍需一个卤素(X2)分子,同时生成1个HX分子,和烷烃的取代反应的这一特点相同。
④溴苯是一种无色油状液体,密度比水大,且不溶于水。
⑤该反应中常会看到液面上有大量白雾出现,这是由于生成的3易分且不溶于水。
⑤硝基苯在写结构简式时,硝基(—NO2)中应是氮原子与苯环上的碳原子相连,而不能写成氧原子与碳原子相连。
如硝基苯还可写成O2N—,不能写成NO2—⑥注意比较“—NO2”、“NO2—”、“NO2”三种表示形式的异同。
相同点:都由一个氮原子和两个氧原子构成。
不同点:“—NO2”表示硝基,是一种中性基团,不能单独稳定存在,短线“—”与氮原子相连。
也可写成“O 2N —”。
“NO 2-”表示亚硝酸根离子,是带一个单位负电荷的阴离子,也不能单独稳定存在,短线“—”只能写在基团“NO 2”的右上角。
“NO 2”表示二氧化氮气体分子,是一种中性物质,可以单独稳定存在,在其周围不能标出短线“—”。
苯及同系物

Cl2
HCl
位取代为主
⑵硝化反应
Cl
CH3—对苯环的影响 使取代反应更易进行
三硝基甲苯(TNT),淡黄色针状晶 体,不溶于水,平时比较稳定,受 热或撞也不易爆炸,但在雷酸汞引 爆下能猛烈爆炸,TNT为烈性炸药。
问题:甲基对苯环的影响,使
甲苯苯环上可发生取代,反过 来,苯环对甲基是否会产生影 响呢?请问甲苯和氯气混合光 照会发生反应吗?
③加成反应:
小结: 在苯的同系物中,由于烃 基与苯环的相互影响。使苯 环上的氢原子更易被取代, 而烃基则易被氧化。
芳烃的分类与命名
一、芳烃的分类
1、单环芳烃
如:
2、多环芳烃 如: 3、稠环芳烃 如:
注意:
①铁粉起催化剂的作用(实际上是FeBr3),如果 没有催化剂则苯与溴水混合发生的是萃取反应。
②导管的作用:一是导气,二是冷凝欲挥发出的 苯和溴使之回流,并冷凝生成的HBr。注意导管末 端不可插入锥形瓶内液面以下,否则将发生倒吸。
③为什么溴苯留在烧瓶中,而HBr挥发出来?因 为溴苯的沸点较高,156.43℃。 ④褐色是因为溴苯中含有杂质溴,可用NaOH溶 液洗涤产物,除去溴,而得无色的溴苯。
CH3 KMnO4、H+ COOH
(苯甲酸)
这样的氧化反应,都是苯环上的烷烃基被 氧化,说明了苯环上的烷烃基比烷烃性质活泼。 这活泼性是苯环对烷烃基影响的结果。
2/21/2019 9:05 AM
二、苯的同系物
②苯的同系物的氧化反应
| —C—H | O || C—OH |
反应机理:
酸性高锰酸钾溶液
烷基上与苯环直接相连的碳直接连氢原子
CH3 | NO2
是一种淡黄色晶体,不溶于水,是一种烈性炸药
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
栏 目
应生成溴苯和溴化氢。根据以上信息,填写下表。
开
关
学习·探究区
第4课时
装置中的导管具有导气、冷凝回流的作用
实验
本
课 栏
装置
目
开
关
实验 将苯和少量液溴放入烧瓶中,同时加入少量铁屑作 步骤 催化剂,用带导管的塞子塞紧烧瓶
学习·探究区
第4课时
①常温下,整个烧瓶充满___红__棕__色__气__体______,在导管
目 开
物质分别与酸性 KMnO4 溶液反应的情况见下表。
关
学习·探究区
第4课时
同分异
本 构体
课 栏 目 开
关 与酸
_________ _________ _____________
KMnO4 溶液反
__不__褪__色__
___褪__色____
___褪__色___
___褪__色____
应现象
学习·探究区
课 栏
A.2丁烯
B.甲苯
目 开
C.1丁烯
D.
关
自我·检测区
第4课时
4.与链烃相比,苯的化学性质的主要特征是( )
本
A.难氧化、难取代、难加成
课 栏
B.易氧化、易取代、易加成
目
开
C.难氧化、易取代、难加成
关
D.易氧化、易取代、难加成
自我·检测区
口有___白__雾__(_H__B_r_遇__水__蒸__气______)形成
本 课 栏 目
实验 ②反应完毕后,向锥形瓶中滴加AgNO3溶液,有 现象 ____浅__黄__色__的__A_g_B__r沉__淀_____生成,
开 关
③把烧瓶里的液体倒入盛有冷水的烧杯里,烧杯底部
有____褐__色__不__溶__于__水__的__液__体_____生成
学习·探究区
第4课时
3.已知,当苯环上有烃基支链时,苯环由于受支链影响,苯 环上与支链相邻的氢及与支链相对的氢都变得更为活泼,
本
课 试写出(1)甲苯与液溴在一定条件下的反应方程式:
栏 目 开 关
____________________________________
学习·探究区
第4课时
(2)当苯环上连有—NO2或—SO3H时可以使苯环上其间位氢 原子变得较为活泼,试写出硝基苯与液溴在一定条件下的
开
关 可以与溴水中的溴发生加成反应,而使溴水褪色;甲苯使溴水
褪色是由于溴易溶于有机溶剂,而发生了萃取现象,溴水中的
溴溶解在甲苯中,而使水层变无色,故答案为 D。
学习·探究区
第4课时
4.农业生产中曾用过一种农药,俗称六六六粉,其化学成
分为 C6H6Cl6,生产这种农药的原料为苯和液氯,试写出
本
其工业生产的化学方程式
本 课
A.将 SO2 通入酸性 KMnO4 溶液使其褪色
栏
目
B.将乙烯通入酸性 KMnO4 溶液使其褪色
开
关
C.将己烯加入溴水使其褪色
D.将甲苯加入溴水使其褪色
学习·探究区
第4课时
答案 D
解析 SO2、乙烯使酸性 KMnO4 溶液褪色,均是因为发生了
本
课
栏 目
氧化还原反应,从而使 MnO- 4 消耗褪色;己烯含有
目
开 则需干燥剂干燥,分离出干燥剂则只能用蒸馏的方法,所
关
以最后两步应为③①。
学习·探究区
第4课时
探究点二 与氢气的反应
本 1.苯环上碳原子之间形成的是一种介于单双键之间特殊的化
课 栏
学键,一般情况下较为稳定,所以苯及其同系物不易发生
目 开
__加__成___反应,而易发生__取__代____反应。但是从组成上看
目 开
取代反应。
关
(2)另外,由于苯的同系物的分子中有与苯环相连的支链,
使得苯的同系物表现与苯不同的性质,如甲苯与浓 HNO3
反应可生成三硝基甲苯。
学习·探究区
第4课时
[活学活用] 1.下列关于苯的说法中,正确的是( )
A.苯的分子式是 C6H6,不能使酸性高锰酸钾溶液褪色,
所以属于饱和烃
本
课
栏 目
学习·探究区
第4课时
[归纳总结]
(1)苯及其同系物较难发生加成反应进一步说明苯环上
本
课 并不含与烯烃中相同的碳碳双键。
栏
目 开
(2)苯及其同系物均不能使溴的四氯化碳溶液褪色。但因
关
为发生萃取作用可以使溴水褪色,并不是因发生加成反
应褪色。
学习·探究区
第4课时
[活学活用]
3.下列不是因为发生化学反应而使溶液褪色的是( )
课
栏
目
开
关
___________________________________________
学习·探究区
第4课时
探究点三 苯的同系物与酸性 KMnO4 溶液的反应 1.苯___不__能____使溴的四氯化碳溶液褪色,也___不__能____使
本
酸性 KMnO4 溶液褪色。但是苯的某些同系物可以使酸
2.实验室用溴和苯反应制取溴苯,得到粗溴苯后,要用如
本 课
下操作精制:①蒸馏 ②水洗 ③用干燥剂干燥 ④10%
栏 目
NaOH 溶液洗 ⑤水洗,正确的操作顺序为( )
开 关
A.①②③④⑤
B.②④⑤③①
C.④②③①⑤
D.②④①⑤③
学习·探究区
第4课时
本 答案 B
课 栏
解析 本题的关键是弄清精制溴苯的最后两步,用水洗,
别插入沸水和冰水中,将会发现前者_____沸__腾_____,后
者_____凝__结__成__无__色__晶__体____。
知识·回顾区
第4课时
2.苯的分子式是_____C_6_H__6 _____,结构简式是__________,
其分子结构特点:
本 课
(1)苯分子为平面_____正__六__边__形_______结构;
栏 目
(2)分子中 6 个碳原子和 6 个氢原子
开 关
__都__在__同__一__平__面__内____;
(3)6 个碳碳键_____键__长__完__全__相__同____,是一种介于
____碳__碳__单__键__和__碳__碳__双__键_______之间的一种特殊化学
键。
知识·回顾区
第4课时
目
开 关
CH2原子团,只有D符合。
自我·检测区
第4课时
2.下列有关芳香烃的说法中,正确的是( A )
本 课
A.苯是结构最简单的芳香烃
栏 目
B.芳香烃的通式是CnH2n-6(n≥6)
开 关
C.含有苯环的有机化合物一定属于芳香烃
D.芳香烃就是苯和苯的同系物
自我·检测区
第4课时
本 3.下列分子中所有碳原子不在同一平面上的是( C )
本 故A不正确;
课
栏 苯的凯库勒式并不能代表苯分子的真实结构,用凯库勒式
目
开 关
表示苯的结构式只是一种习惯用法,苯分子中的碳碳键完
全相同,是一种介于碳碳单键和碳碳双键之间的一种特殊
的化学键,故B不正确;
在催化剂作用下,苯与液溴反应生成溴苯,是一种取代反
应,而不是加成反应,故C不正确。
学习·探究区
第4课时
C选项中产生黑烟是苯中碳的含量高造成的;
D选项中无论是苯还是苯的同系物均能与H2发生加成反应并 且比例为1∶3。
学习·探究区
本 课 栏 目 开 关
第4课时
自我·检测区
第4课时
1.下列物质中属于苯的同系物的是( )
本 课 栏 目 开 关
自我·检测区
第4课时
本 答案 D
课
栏 解析 同系物概念:结构相似,分子组成相差1个或若干个
栏
目 开
B.苯的同系物是分子中仅含有一个苯环的所有烃类物质
关
C.苯和甲苯都不能使酸性 KMnO4 溶液褪色
D.苯和甲苯都能与卤素单质、硝酸等发生取代反应
学习·探究区
第4课时
答案 D
本 解析 芳香烃是分子中含有一个或多个苯环的烃类物质,而
课
栏 苯的同系物仅指分子中含有一个苯环且侧链全部为烷基的
目
开 关
第4课时
本 通过实验,可以看出与苯环直接相连的பைடு நூலகம்原子上如果没有
课
栏 目
氢原子,则不能使酸性 KMnO4 溶液褪色。
开
关
学习·探究区
第4课时
[归纳总结]
(1)苯的同系物由于出现了支链,支链与苯环相互影响,
本
所以苯的同系物与苯比较,性质并不完全相同,苯环受
课 栏
支链影响,苯环上的氢变得较为活泼,支链上的烃基由
3.苯易发生__取__代___反应,能发生__加__成___反应,难被
本
__氧__化____,其化学性质不同于烷烃和烯烃。
课 栏
(1)苯__不___能___使酸性高锰酸钾溶液褪色,在空气中能够燃
目 开
烧,燃烧时产生____明__亮__的_____火焰并有浓烟产生,燃烧的
关
化学方程式为
点燃 ____2__C_6_H__6+___1_5_O_2_―__―__→__1_2_C__O__2+___6_H_2_O___________。
D.1 mol甲苯与3 mol氢气发生加成反应
学习·探究区
第4课时
答案 A
解析 侧链对苯环的影响,应是原来无侧链时没有的性质,
本 现在因为有侧链而有了相应的性质。A选项中甲苯硝化反应
