残留溶剂分析方法验证方案报告
残留溶剂分析方法验证方案

残留溶剂分析方法验证方案引言:残留溶剂是指在制药、食品、化妆品、印刷等工业生产过程中可能残留在最终产品中的有机溶剂。
残留溶剂的检测和分析对于保障产品质量和消费者的健康非常重要。
本文将介绍一个残留溶剂分析方法验证的方案,确保该方法能够准确、可靠地检测残留溶剂。
一、验证目的和范围1.验证目的:验证残留溶剂分析方法的准确性、精密度、特异性、灵敏度和线性范围等性能指标。
2.验证范围:本验证方案适用于残留溶剂分析方法的验证。
二、验证实验设计1.准备样品:收集一批含有已知浓度残留溶剂的样品,确保样品的浓度分布能够覆盖方法的线性范围。
2.准备溶剂标准品:根据实际需要,准备残留溶剂的标准品,浓度与样品中的残留溶剂浓度相对应。
3.确定分析方法:根据实际情况,选择一种适用的残留溶剂分析方法,确保该方法能够准确地检测样品中的残留溶剂。
4.验证参数:(1)准确性:通过对样品添加已知浓度的残留溶剂标准品,并进行多次重复测定,计算准确度参数。
(2)精密度:通过对样品进行多次重复测定,计算精密度参数。
(3)特异性:通过对样品进行干扰试验,判断分析方法是否能够准确检测出残留溶剂。
(4)灵敏度:通过对样品进行逐步稀释,测定最低检测限,并评估方法的灵敏度。
(5)线性范围:通过对样品不同浓度的残留溶剂进行测定,并绘制标准曲线,估算线性范围和相关系数。
三、验证结果和数据分析1.准确性参数:根据重复测定数据,计算准确度参数,如相对标准偏差(RSD)和回收率。
2.精密度参数:根据重复测定数据,计算精密度参数,如RSD。
3.特异性结果:记录干扰试验结果,判断方法是否能够准确检测出残留溶剂。
4.灵敏度结果:记录最低检测限,并评估方法的灵敏度。
5.线性范围结果:通过绘制标准曲线,记录线性范围和相关系数。
四、验证结论和建议1.准确性和精密度:根据验证结果,评估方法的准确性和精密度,并根据实际需要确定接受范围。
2.特异性:确认方法的特异性,并排除其他可能的干扰物。
残留溶剂方法学验证方案
阿莫西林残留溶剂分析方法验证方案文件编号: VP-01-06-00-041方案起草方案审核方案批准生效日期:年月日1、概述在阿莫西林制备工艺中,使用了甲醇与丙酮两种对人体具有危害的二类溶剂,我公司为了确保阿莫西林原料中甲醇与丙酮的残留在国家要求范围内,开发了阿莫西林胶囊中甲醇与丙酮残留的检测方法,按照《中国药典》2015年版的要求对此检测方法进行方法学验证。
2、验证目的证明本方法能满足阿莫西林原料中甲醇与丙酮的残留溶剂测定,确保阿莫西林原料中甲醇与丙酮的残留溶剂检测方法准确、重现并耐用,检测结果数据真实可靠。
3、验证范围本验证方案适用于阿莫西林中甲醇与丙酮的残留溶剂检验方法验证。
4、确认小组成员及职责5、验证前的风险评估5.1验证小组人员按照《质量风险管理规程》,对分析方法进行了风险评估,确定了需进行方法确认的项目。
5.1.1严重性(S):危害可能产生后果的程度。
严重程度分为五个等级。
5.1.2可能性(P):影响检测结果的事件发生的可能性频率或概率,建立以下五个等级:5.1.3可检测性(D):检测到异常情况存在的能力的程度,定义如下:5.2风险优先数量等级判定(RPN)5.2.1风险等级判定标准的确定RPN是事件发生的严重程度、可能性和可探测性三者乘积,用来衡量可能的仪器缺陷,以便采取可能的预防措施。
RPN = Severity(严重程度)×Possibility(发生的可能性)×Detection(可探测性)5.2.2风险评价和处理注:当RPN≤8,但严重性S为5时,仍需按中等以上风险进行后续控制。
5.3风险分析6、验证前的准备6.1人员培训在本方案实施前,已对方案实施过程中涉及人员进行培训,以保证方案顺利实施,做好培训记录,培训记录见表1。
表1 训确认表7、验证内容7.1验证项目及可接受标准7.2仪器配置检查(见表2)表2仪器配置表7.3验证所用的试剂及样品(见表3)表3验证所用试剂及样品7.3实验条件:检测器:FID(氢火焰离子化检测器)色谱柱:WEL-624 30m×0.32mm×0.25um升温程序:50℃,维持6min,60℃/min的速率升温至240℃,维持3分钟进样口温度:200℃检测器温度:260℃载气:氮气流速:2.98 ml/min分流比1:1 进样方式:顶空进样,顶空瓶平衡温度80℃,平衡时间30min7.4方法学验证7.4.1专属性试验7.4.1.1目的:确定所需测定的目标溶剂可以很好的分离,并且不会受到来自溶媒及可能出现的杂质的干扰。
残留溶剂顶空分析方法验证方案模版最新版本

方案批准注:在方案批准部分签字表明签字者同意方案中规定的检测项目检测方法和记录要求。
在执行本方案的过程中可能会出现影响严格执行本方案的偏差,对较小的偏差将通过偏差报告的形式来解决,对于关键性偏差,如对方法的调整、对参数或接受标准的调整必须制定出增补方案并按照原方案批准程序得到批准才能进行。
所有的偏差报告和增补方案必须在提交验证报告供批准时一同提交。
目录1.概述 (3)2.参考资料 (4)3. 职责 (4)4. 色谱系统及色谱条件 (4)5. 器材与试剂 (5)6. 验证试验 (5)6.1系统适应性 (5)6.2专属性 (6)6.3耐用性 (7)6.4定量限 (7)6.5检测限 (8)6.6线性与范围 (8)6.7准确度 (9)6.8精密度 (11)7.再验证周期 (12)8.偏差及纠正措施 (12)9.最终审核和批准 (12)药品残留溶剂顶空分析方法草案 (14)1.概述1.1根据ICH对药品中残留溶剂含量的要求及盐酸噻氯匹定生产工艺,必须控制盐酸噻氯匹定生产工艺中使用到的溶剂乙醇、丁酮、甲苯、N,N-二甲基甲酰胺(DMF)的残留量。
限度分别为:乙醇≤5000ppm、丁酮≤5000ppm、甲苯≤890ppm、DMF≤880ppm。
1.2分析方法草案见附件。
1.3本分析方法属于杂质定量分析,因此需要验证的项目有:系统适应性、专属性、线性、准确度、检测限、定量限、精密度、耐用性,具体参数及接受标准要求见下表:2.参考资料ICH Q3C (R3), November 2005.ICH Q2 (R1), November 2005.<467> Residual Solvents, United States Pharmacopoeia 31, November 2007. <20424> Residual Solvents, European Pharmacopoeia 6.0, June 2007.3. 职责4.1色谱系统5.表2. 器材列表6. 验证试验6.1系统适应性目的:对由分析设备、实验操作、被分析供试品组成的完整的系统进行评估。
残留溶剂分析方法验证方案DOC

残留溶剂分析方法验证方案DOC一、目的和范围该验证方案的目的是验证残留溶剂分析方法的适用性和可靠性,以确保其在实际样品中的准确性和精密性。
该验证方案适用于分析实验室中使用的残留溶剂分析方法,包括仪器和设备的检验的验证。
二、实验室设备和试剂1.装备:(1)高效液相色谱仪(HPLC)(2)气相色谱仪(GC)(3)质谱仪(MS)2.试剂:(1)残留溶剂标准物质(2)气相色谱柱(3)质谱校准物三、验证参数1.准确性:通过添加已知浓度的标准物质到实际样品中,检测其残留浓度与添加浓度之间的差异来评估方法的准确性。
2.精密性:通过重复测定同一样品多次,计算相对标准偏差(RSD)来评价方法的精确性和重复性。
3.线性范围:通过在一系列浓度范围内测定溶剂标准物质的浓度,并绘制峰面积与浓度的线性回归曲线来评估方法的线性范围。
4.检出限和定量限:通过测定稀释系列标准物质的峰高或峰面积,并根据信号噪声比进行计算来确定方法的检出限和定量限。
四、方法验证步骤1.准备一系列已知浓度的溶剂标准物质,尽量覆盖预计样品中的溶剂浓度范围。
2.对每个标准物质进行HPLC、GC和MS的分析,记录峰高或峰面积。
3.根据测定结果绘制标准曲线,并计算线性回归方程和相关系数。
4.确定方法的线性范围,并计算线性回归曲线的斜率、截距和相关系数。
5.随机选择多个实际样品并进行多次测定(至少3次),计算RSD。
6.将已知浓度的标准物质添加到实际样品中,分析其残留浓度,并与已知浓度进行比较,计算准确性。
7.测定不同浓度的稀释系列标准物质的峰高或峰面积,并计算检出限和定量限。
8.整理实验数据并进行统计分析,评估方法的可靠性和适用性。
五、验证结果与评价根据验证结果,对方法的准确性、精密性、线性、检出限和定量限进行评价。
如果结果符合规定的标准和要求,则证明方法可靠且可应用于实际样品中。
如果结果不符合要求,则需要对方法进行修正或重新验证。
六、记录和报告将验证过程的所有数据、结果和评价进行详细记录,形成验证报告。
残留溶剂简短报告模板
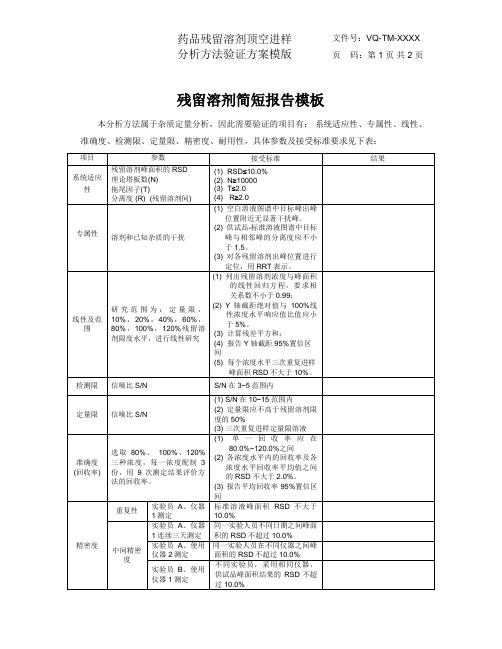
本分析方法属于杂质定量分析,因此需要验证的项目有:系统适应性、专属性、线性、准确度、检测限、定量限、精密度、耐用性,具体参数及接受标准要求见下表:
项目
参数
接受标准
结果
系统适应性
残留溶剂峰面积的RSD
理论塔板数(N)
拖尾因子(T)
分离度(R) (残留溶剂间)
(1) RSD≤10.0%
(1)列出残留溶剂浓度与峰面积的线性回归方程,要求相关系数不小于0.99;
(2) Y轴截距绝对值与100%线性浓度水平响应值比值应小于5%。
(3)计算残差平方和;
(4)报告Y轴截距95%置信区间
(5)每个浓度水平三次重复进样峰面积RSD不大于10%。
检测限
信噪比S/N
S/N在3~5范围内
定量限Байду номын сангаас
信噪比S/N
耐用性
1.改变流速(±XX%)
同“系统适应性要求”
2.改变初始柱温(±XX℃)
3改变色谱柱的批号
(3)报告平均回收率95%置信区间
精密度
重复性
实验员A、仪器1测定
标准溶液峰面积RSD不大于10.0%
中间精密度
实验员A、仪器1连续三天测定
同一实验人员不同日期之间峰面积的RSD不超过10.0%
实验员A、使用仪器2测定
同一实验人员在不同仪器之间峰面积的RSD不超过10.0%
实验员B、使用仪器1测定
不同实验员,采用相同仪器,供试品峰面积结果的RSD不超过10.0%
(1) S/N在10~15范围内
(2)定量限应不高于残留溶剂限度的50%
(3)三次重复进样定量限溶液
准确度
(回收率)
残留溶剂方法学验证方案

残留溶剂方法学验证方案残留溶剂是指在其中一种溶剂处理过程中,溶剂不能完全挥发,残留在处理物中的化合物。
残留溶剂的测试和分析对于保证产品质量和安全性非常重要。
下面是一个关于残留溶剂方法学验证方案的简要说明,包含实验步骤、仪器设备、数据处理和结果评估等。
1.实验目的:验证残留溶剂的测试方法是否准确可靠,适用于特定产品或材料的检测。
2.实验步骤:2.1样品准备:选取代表性的产品样品或材料样品,并按照标准或法规的要求制备样品。
2.2定量添加溶剂:根据实际应用情况,向样品中添加已知浓度的溶剂,以模拟实际环境中的残留情况。
2.3提取和浓缩:使用适当的提取方法(如固相萃取、溶剂萃取等)将残留溶剂从样品中提取出来,并将提取液浓缩。
2.4仪器分析:使用适当的分析仪器(如气相色谱-质谱联用仪、高效液相色谱仪等),对浓缩后的提取液进行定量分析。
3.仪器设备:3.1分析仪器:根据需要选择适当的分析仪器,如气相色谱-质谱联用仪(GC-MS)、高效液相色谱仪(HPLC)、液相色谱-质谱联用仪(LC-MS)等。
3.2样品制备设备:如研磨仪、超声波清洗器、离心机等,用于样品制备和处理。
4.数据处理:4.1标准曲线绘制:根据已知浓度的溶剂标准品,利用分析仪器进行测定,得到残留溶剂的峰面积与浓度之间的关系,绘制标准曲线。
4.2样品测定:将提取液注入分析仪器,进行测定。
根据标准曲线,计算样品中残留溶剂的浓度。
5.结果评估:5.1方法验证:通过实验结果,验证残留溶剂的测试方法是否能准确测定残留溶剂的浓度,并评估方法的重复性和精密度。
5.2检出限和定量限:根据实验结果,计算出测定方法的检出限和定量限,评估方法的敏感度和适用范围。
5.3结果分析:对于不同样品的测定结果,进行统计分析和比较,评估残留溶剂的含量是否符合标准要求。
5.4结论:根据实验结果,得出对于残留溶剂测试方法的验证结论,并提出改进建议。
以上为残留溶剂方法学验证方案的简要说明,具体实验细节和方法参数需要根据实际情况进行调整。
残留溶剂GC检查方法的设计验证

02
溶剂
03
温度
04
不分流进样
05
顶空瓶体积
八、提高灵敏度
利用盐析作用,即在水溶液中加入无机盐(硫酸钠)来改变挥发性组分的分配系数。常用高浓度,甚至用饱和浓度。盐析作用对极性组分的影响远大于对非极性组分的影响。
例如在水溶液样品溶剂中加入0.01mol/L氯化钠溶液可使甲醇、乙醇灵敏度提高5倍(这种方法不常用)。
不可研磨样品,必须原态取样
01
不可超声、不能加热溶解样品
02
样品置顶空瓶中压盖后可以超声、加热
03
样品与对照品配制方法一致,避免基质效应
04
前述三类溶剂取样量尽可能大,至少0.1g/ml
05
四、供试品制备
01
进样方式首选顶空,基线干净
02
卤代烃直接进样容易灭火
五、进样方式
ICH限度并不是最高要求
不主张使用污染性大、毒性大的溶媒!
前述三类溶剂如果顶空进样应选择K小的溶媒!
其次溶媒是否能溶解待测溶剂?
水、DMF、DMSO、不挥发酸碱溶液,不可使用盐酸液和氨水,顶空进样可选择在80~90°C加热能溶解样品的试剂。
苯、甲苯、三氯甲烷等水溶性不好的溶剂,可先用少量乙醇或甲醇溶解待查溶剂再用水稀释。
三、溶媒
直接进样:
水、合适的有机溶媒或混合液。对于非极性色谱柱,水对柱有影响,会缩短柱的使用寿命。
A
B
顶空小平加盖后可超声加热助溶
有报道加5%SDS助溶。
助溶方式:
不可超声或加热助溶* ,以免残留溶剂挥发;如果顶空进样,样品置顶空瓶封盖之后可以超声或加热溶解。
大颗粒样品不可以研磨取样,只能取原态样品(或冷冻粉碎)。
残留溶剂方法验证方案

残留溶剂方法验证方案残留溶剂方法验证是一种常用的分析技术,用于检测和确定样品中残留的溶剂成分。
该方法主要通过提取和分离样品中的残留溶剂,并使用合适的分析仪器进行定性和定量分析。
本文将介绍残留溶剂方法验证的步骤和注意事项。
一、验证步骤1. 确定验证的目的和范围:首先需要明确验证的目的是为了确认样品中是否存在残留溶剂,以及残留溶剂的种类和含量。
范围包括验证的样品类型、溶剂种类、检测限和精确度要求等。
2. 选择合适的提取方法:根据样品的性质和溶剂的特点,选择合适的提取方法。
常用的提取方法包括溶剂浸提、固相微萃取、超声波提取等。
3. 分离和纯化:通过色谱技术或其他适当的分离方法,将提取得到的样品中的残留溶剂与其他组分分离开来,以便后续的定性和定量分析。
4. 分析仪器的选择和校准:选择合适的分析仪器进行残留溶剂的定性和定量分析。
常用的仪器包括气相色谱-质谱联用仪、液相色谱仪等。
在使用仪器前,需要进行校准和验证,确保分析结果的准确性和可靠性。
5. 定性和定量分析:根据仪器的分析原理和方法,进行残留溶剂的定性和定量分析。
定性分析主要是通过比对样品中残留溶剂的特征峰和质谱图,与标准品进行对比,确定残留溶剂的种类。
定量分析则是通过仪器的响应因子和标准曲线,计算出样品中残留溶剂的含量。
6. 数据处理和结果评定:根据分析结果,进行数据处理和统计分析,确定残留溶剂的含量是否符合规定的限量要求。
同时还要对分析的准确性和可靠性进行评定,包括重复性、中间精密度、回收率等指标。
7. 报告编制和归档:根据验证结果,编制验证报告,并将相关数据和记录进行归档。
报告中应包括验证的目的和范围、方法和仪器的选择、样品处理过程、分析结果和评价等内容。
二、注意事项1. 样品的选择和处理:样品应代表性,并且要注意样品的保存和处理方法,避免对残留溶剂的蒸发和降解。
2. 仪器的校准和验证:在使用仪器前,需要进行校准和验证,确保仪器的准确性和可靠性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
残留溶剂分析方法验证方案报告**制药股份有限公司版本号: 第1版验证名称 XX产品残留溶剂分析方法验证方案验证编号 YZ-FX-13-001(P) 页码:Page 1 of 12***产品残留溶剂分析方法验证方案20**年**月**制药股份有限公司版本号: 第1版验证名称 XX产品残留溶剂分析方法验证方案验证编号 YZ-FX-13-001(P) 页码:Page 2 of 12验证方案的起草与审批验证小组成员部门人员职责验证小组组长职责部门人员负责组织起草验证方案并按批准方案组织实施;督促验证人员做好记录;负责各阶段验证结果汇总及评价、组织起草验证报告;组织相关培训方案审核审核签名及日期验证委员会方案批准批准人批准日期方案实施日期:**制药股份有限公司版本号: 第1版验证名称 XX产品残留溶剂分析方法验证方案验证编号 YZ-FX-13-001(P) 页码:Page 3 of 12目录1. 验证目的 ..................................................................... ............................................................. 4 2. 方法简介与确认范围...................................................................... ........................................ 4 3. 标准品、供试品 ..................................................................... ................................................. 4 4. 风险评估 ..................................................................... ............................................................. 4 5. 验证的可接受标准...................................................................... ............................................ 5 6. 验证步骤 ..................................................................... ............................................................. 6 6.1系统适应性 ..................................................................... .......................................................... 6 6.2专属性 ....................................................................................................................................... 6 6.3定量限与检测限...................................................................... ................................................. 7 6.4线性 ..................................................................... . (7)6.5准确度 ..................................................................... .................................................................. 86.6精密度 ..................................................................... .................................................................. 9 6.7范围 ..................................................................... . (9)6.8耐用性 ..................................................................... .................................................................. 9 6.9样品测定 ..................................................................... ............................................................ 10 7.偏差 ..................................................................... ....................................................................... 10 8.风险的接收与评审...................................................................... .............................................. 10 9.再验证 ..................................................................... . (10)10.确认结果评审和结论...................................................................... . (10)10 11.更改历史 ..................................................................... .............................................................12. 附录 ..................................................................... . (10)**制药股份有限公司版本号: 第1版验证名称 XX产品残留溶剂分析方法验证方案验证编号 YZ-FX-13-001(P) 页码:Page 4 of 121. 验证目的根据法规的要求,分析方法应进行验证,证明采用的方法适合于相应的检测要求。
这个验证方案的目的是为验证提供具体方法参数、可接受标准和研究步骤。
2. 方法简介与确认范围***产品生产过程中用到有机溶剂乙醇、丙酮、二氯甲烷、乙酸乙酯、四氢呋喃,为了准确测定溶剂在成品中的残留量,现对该测定方法进行验证,验证包括方法的专属性、检测限与定量限、线性、范围、准确度、精密度及耐用性。
3. 标准品、供试品3.1标准品名称批号来源3.2供试品名称批号来源4. 风险评估按照《质量风险管理规程》,质量控制部和质量管理部共同对分析方法进行了风险评估,确定了需进行方法确认的项目。
具体见下表:风险现有控制措风险S P D RPN 建议采取措施风险可能影响效应级别因素施杂质和主峰不能首次使用前,不具有3 3 3 27 中专属性有效分离,含量不无对专属性进行专属性准确验证定量限对该方法的定定量限小的杂质不能被3 3 3 27 中与检测无量限进行验高检出限证。
精密度不同时间或人员每次测试前进首次使用前,精密度 3 3 3 27 中差测定的结果不一行系统适用性对精密度进行**制药股份有限公司版本号: 第1版验证名称 XX产品残留溶剂分析方法验证方案验证编号 YZ-FX-13-001(P) 页码:Page 5 of 12致测试验证首次使用前,回收率3 3 3 27 中准确度含量结果不准确无对准确度进行低验证首次使用前,线性不3 3 3 27 中线性含量结果不准确无对线性进行验好证首次使用前,浓度超过范围后3 3 3 27 中范围范围窄无对范围进行验结果不准确证首次使用前,耐用性参数微小变化对3 3 3 27 中耐用性无对耐用性进行差结果影响很大验证风险评估人:评估日期:5. 验证的可接受标准项目可接受标准专属性各组分之间分离度不低于1.5,溶剂无干扰定量限与检测限 LOD&LOQ?0.05% 乙醇LOD&LOQ?0.05% 乙酸乙酯LOD&LOQ?0.05% 丙酮LOD&LOQ?0.0072% 四氢呋喃LOD&LOQ?0.012% 二氯甲烷各溶剂LOQ精密度:RSD%?15%2线性 R?0.999准确度回收率在70~130%范围内精密度重复性RSD%?15%中间精密度RSD%?15%精密度:两组数据平均检测结果的相对偏差?20%范围应至少为定量限浓度到指标的120%**制药股份有限公司版本号: 第1版验证名称 XX产品残留溶剂分析方法验证方案验证编号 YZ-FX-13-001(P) 页码:Page 6 of 12耐用性评估柱温、流速、色谱柱、溶液放置时间对检测结果的影响 6. 验证步骤6.1系统适应性精密称取乙醇200mg、丙酮200mg、二氯甲烷24mg、乙酸乙酯200mg、四氢呋喃28.8mg,置于已加入10ml二甲基亚砜的50ml量瓶中,用二甲基亚砜溶解并稀释至刻度,作为对照溶液储备液;精密移取对照液储备液5ml,置于一100ml量瓶中,用二甲基亚砜稀释至刻度;精密移取5ml,置于20ml顶空瓶中,密封。
