ACS双联抗血小板治疗必要性与特殊情况下抗血小板治疗处理原则
急性冠脉综合征特殊人群抗血小板治疗中国专家建议解读

5
Chen ZM, et al. Lancet. 2005 Nov 5;366(9497)1607-21.
高龄
高龄患者中,替格瑞洛与氯吡年亚组(≥75岁)分析:氯吡格雷与替格瑞洛治疗的缺血性终点和 大出血发生率无显著差异
• KAMIR-NIH研究中的东亚人群分析: ≥75岁患者,替格瑞洛TIMI大出血风险显著 高于氯吡格雷(HR:5.352; 95% CI 1.412 - 20.288)
溶栓治疗
ACS特殊人群——溶栓治疗患者 抗血小板治疗中国专家建议
溶栓治疗患者抗血小板治疗的临床推荐
1. STEMI 溶 栓 患 者 尽 早 给 予 双 联 抗 血 小 板 治 疗 ( dual antiplatelet therapy, DAPT):阿司匹林负荷量200~300mg(嚼服),随后100mg/d,≤75岁者给予氯吡 格雷300mg负荷剂量(>75岁者不予负荷剂量),随后75mg/d,持续治疗至少12个 月。 2. STEMI溶栓患者不推荐使用替格瑞洛,但溶栓后进行PCI的患者,可权衡出血和缺 血风险,考虑在溶栓48h后使用替格瑞洛。
此外,高龄患者常被排除在随机对照研究之外。因此,高龄ACS患者的抗血小板治疗缺乏 循证医学证据,更应谨慎用药。
1. 海峡两岸医药卫生交流协会老年医学专业委员会. 中华老年医学杂志, 2016,35(7):683-691.
2. 中华医学会老年医学分会. 中华老年医学杂志. 2016,35(7):683-691.
合用口服抗凝药
ACS特殊人群——合用口服抗凝药患者 抗血小板治疗中国专家建议
合用口服抗凝药患者抗血小板治疗的临床推荐
Sabatine M S, et al. New England Journal of Medicine, 2005, 352(12): 1179-1189.
最新:冠心病双联抗血小板治疗中国专家共识要点

最新:冠心病双联抗血小板治疗中国专家共识要点大量临床研究证实,在急性冠状动脉综合征(ACS)和/或接受经皮冠状动脉介入治疗(PCI)或冠状动脉旁路移植术(CABG)的人群中应用双联抗血小板治疗(DAPT),较阿司匹林单药治疗可显著减少缺血事件,如心血管病死亡、心肌梗死、缺血性卒中、支架内血栓等。
第一部分:DAPT策略一、DAPT方案概述血小板的激活与聚集在动脉粥样硬化血栓形成的发生发展过程中具有重要作用,因此抗血小板是治疗冠心病的关键。
血小板环氧化酶(COX)-1抑制剂:阿司匹林通过不可逆地抑制COX-1从而阻止血栓素A2的合成及释放,抑制血小板聚集;吲哚布芬可逆性地抑制COX-1,对前列腺素抑制率较低,胃肠道反应较小、出血风险较低,可考虑作为出血及胃溃疡风险高等阿司匹林不耐受患者的替代治疗。
P2Y12受体抑制剂:二磷酸腺苷(ADP)是血小板活化与聚集过程中的重要激动剂,P2Y12受体抑制剂能够阻碍ADP 与血小板表面受体结合,有效地减弱ADP的级联反应,降低血小板聚集效应。
目前国内常用的P2Y12受体抑制剂主要为氯吡格雷和替格瑞洛。
二、DAPT实施中的缺血与出血风险评估1. 临床缺血与出血危险因素:临床常见的高缺血风险因素包括:既往心肌梗死或卒中史、心电图ST 段压低、高龄、肾功能不全、糖尿病、贫血、左心室功能障碍、冠状动脉多支病变、复杂冠状动脉PCI(如左主干、分叉、慢性完全闭塞、弥漫性长病变、仅存冠状动脉)等。
高出血风险因素包括:高龄、女性、肾功能不全、慢性心力衰竭、血小板减少或抗血小板治疗后抑制过度、贫血、低体重指数、合用口服抗凝药(OAC)等。
以上可供临床初步判断缺血和出血风险。
2. 缺血与出血风险评分:专门用于指导DAPT疗程制定的风险评分的应用应当优先于其他风险评分,如PRECISE-DAPT评分和DAPT 评分(表5和6)。
(1)PRECISE-DAPT评分:(2)DAPT评分:3. 血小板功能检测:接受P2Y12受体抑制剂治疗时的血小板反应性对缺血和出血事件有中等程度的预测价值。
急性冠状动脉综合征特殊人群抗血小板治疗中国专家建议

3.ACS合并痛风治疗,应考虑阿司匹林对血尿酸的影 响,小剂量阿司匹林(75~325 mg/d)可轻度升高血尿 酸,一旦证实阿司匹林增加了痛风风险,立即停用阿司 匹林或换用西洛他唑+氯吡格雷。
3.DAPT期间发生消化道出血的患者,在尽快明确出血原因并积极治疗 原发病的基础上,应权衡出血和缺血风险决定是否停用抗血小板治疗及何 时恢复抗血小板治疗。轻度出血无需停用DAPT,如有明显出血(血红蛋 白下降>3 g或需要住院治疗,但未引起血流动力学紊乱),可考虑首先停 用阿司匹林,如出现危及生命的活动性出血,可停用所有抗血小板药物。 病情稳定后,在确保安全的情况下尽快恢复抗血小板治疗,一般3~5 d后 恢复氯吡格雷,5~7 d后恢复阿司匹林。
3.对于肾功能不全患者,如需联用ARB治疗,DAPT首选氯吡 格雷+阿司匹林。
9.合并痛风/高尿酸血症患者的抗血小板治 疗 建议
1.痛风急性发作时首选氯吡格雷75~150 mg/d,病情 稳定后尽早服用阿司匹林75~100 mg/d+氯吡格雷75 mg/d,6~12个月后改为氯吡格雷75 mg/d长期维持。
10.缺铁性贫血患者的抗血小板治疗 建议
1.贫血患者选择抗栓治疗时需充分权衡缺血和出血风险,如果 贫血原因不明或难以纠正,应限制使用DES,因为后者需延长 DAPT的时间。
2.经DES治疗后的ACS合并贫血患者,推荐DAPT治疗12个月, 治疗过程中应对出血风险及骨髓抑制风险进行监测,并依据实际 情况调整DAPT疗程,如患者伴高出血风险,则应考虑DAPT治 疗6个月后停用P2Y12受体抑制剂。
3.如ACS患者血小板计数低于30×109/L建议停用所有抗血小板 药物,并避免行PCI。
ACS抗血小板治疗

新型ADP受体拮抗剂
如cangrelor,可在手术过程中快速逆转抗血 小板作用,降低围手术期血栓风险。
抗血小板治疗的个体化方案研究
根据患者的基因型、危险因素和临床 特征制定个体化的抗血小板治疗方案 ,以提高治疗效果并降低不良反应。
研究不同患者对不同抗血小板药物的 反应差异,为临床提供更精确的治疗 选择。
防止血栓形成
血小板在血栓形成过程中起关键作用,通过抗血小板治疗 可有效抑制血小板聚集,预防血栓形成,从而降低心肌梗 死、中风等严重心血管事件的发生率。
改善患者预后
及时、规范的抗血小板治疗有助于改善ACS患者的临床预 后,提高患者的生活质量和生存率。
临床实践中的注意事项与挑战
01 02
出血风险
抗血小板治疗会增加出血风险,特别是消化道出血、脑出血等严重出血 事件。医生需根据患者情况谨慎评估抗血小板治疗的利弊,选择合适的 药物和剂量。
01
02
03
抑制血小板活化
抗血小板药物通过抑制血 小板表面的受体或酶,阻 止血小板活化,从而降低 血栓形成的风险。
抑制血小板聚集
抗血小板药物可以抑制血 小板之间的聚集反应,防 止血栓形成和血管阻塞。
增加血小板溶解
某些抗血小板药物可以促 进血小板溶解,从而降低 血小板数量和活性,减少 血栓形成的风险。
ACS的分类与临床表现
NSTEMI/UA
非ST段抬高型心肌梗死和不稳定型心绞痛的病理生理机制相似,冠状动脉存在 不稳定的粥样斑块,但没有完全闭塞,心电图表现为非ST段抬高。临床表现为 阵发性胸痛、呼吸困难、心悸等。
STEMI
ST段抬高型心肌梗死是由于冠状动脉完全闭塞导致心肌缺血坏死,心电图表现 为ST段抬高。临床表现为持续剧烈胸痛、心力衰竭、心律失常甚至心脏骤停。
急性冠脉综合征ACS-PCI后的DAPT双联抗血小板治疗策略(全文)

急性冠脉综合征ACS-PCI后的DAPT双联抗血小板治疗策略(全文)双联抗血小板治疗(dual antiplatelet therapy,DAPT)和经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)均被证实为治疗急性冠脉综合征(acute coronary syndrome,ACS)的有效临床手段。
现阶段对置入药物洗脱支架(drug eluting stents,DES)后DAPT的使用时间指南建议为12个月,以减少晚期或超晚期的支架内血栓的形成,对于高危ACS患者则建议延长DAPT使用时间。
研究发现,新一代DES由于改良了血管愈合和再内皮化的特性,疗效优于早期DES,临床应用比例逐渐增加。
应用光学相干断层成像术(OCT)对二代和三代DES置入后血管进行观察研究,结果发现87%支架术后3个月内新生内膜完全覆盖支架,提示新一代DES置入后可能不必延长DAPT应用时间[1-3]。
这些发现引发有关ACS患者DAPT使用时长的讨论。
PCI后双联抗血小板治疗的必要性2005 ACC/AHA/SCAI PCI指南[4]指出:支架较PTCA显著降低了血管再狭窄(BENESTENT II:PTCA31%vs. 支架17%;STRESS:PTCA42%vs. 支架32%)。
DES可对冠脉病变局部提供缓慢和长期高浓度的药物释放,抑制细胞过度增生和抗血管重塑,进一步降低了支架内再狭窄率:裸支架36%vs. 西罗莫司洗脱支架9%;裸支架27%vs. 紫杉醇洗脱支架8%。
DES的应用,在进一步降低了支架内再狭窄率的同时,由于药物及涂层本身抑制了支架表面的内皮化,从而增加了支架植入术后晚期血栓形成的风险。
通过观察停用氯吡格雷后晚期缺血事件的发生率,发现停用DAPT增加DES晚期血栓形成,增加了死亡或非致死性心肌梗死的发生率[5]。
晚期和超晚期支架血栓的主要危险因素为过早停用抗血小板药物[6]。
ACS 患者最佳双联抗血小板治疗方案是什么?

近期,法国研究者 Angoulvant 等人在BMJ 杂志上发表文章,以探讨急性冠脉综合征(ACS)最佳双联抗血小板治疗方案。
研究提到,2014 年欧洲心脏病指南建议急性冠脉综合征(ACS)患者应服用双联抗血小板药物12 个月,并提出阿司匹林联合普拉格雷或替格瑞洛的效果优于阿司匹林联合氯吡格雷。
但毫无疑问这两种新型P2Y12 抑制剂均会增加出血风险。
对于普拉格雷,在ST 段抬高型心肌梗死(STEMI)的老年患者、瘦弱患者和既往有脑血管疾病患者中的出血风险更高。
而替格瑞洛增加非CABG 相关出血风险更为明显。
Swiss 研究纳入了2148 例患者,研究ACS 后普拉格雷或者氯吡格雷联合阿司匹林治疗出血的风险。
结果表明两者之间出血风险无明显差异,但普拉格雷组心脏病死亡率及缺血事件发生率较氯吡格雷组低。
有趣的是,普拉格雷组1 年的非CABG 相关的TIMI 出血事件与TRITON-TIMI 38 研究中发生率相似。
而氯吡格雷组中非CABG 相关的TIMI 出血事件较TRITON-TIMI38 研究发生率高。
主要原因或许是普拉格雷组中患者管理优于氯吡格雷组。
作者认为两者在评估出血风险时,其效应相似。
但至今仍未有对于普拉格雷与替格瑞洛这两种新型P2Y12 抑制剂的临床效果及安全性的头对头研究。
这两个药物的药效动力学及药代动力学不一样,这可以解释在TRITON-TIMI 38 研究和PLATO 研究中的出血风险不一致。
普拉格雷不可逆抑制P2Y12 受体从而缩短血小板寿命,替格瑞洛可逆抑制P2Y12 受体。
这可以解释在CABG 相关TIMI 出血风险中,普拉格雷与氯吡格雷相比出血风险增加。
而在替格瑞洛中并未观察到该现象。
为预防出血,CABG 术前7 天需停用普拉格雷,氯吡格雷需停用5 天,而替格瑞洛需3 天。
故心脏病专家需仔细评估CABG 手术指征并选用合适的抗血小板治疗药物。
Swiss 研究中,71%-75% 患者植入药物支架,随之而来血栓形成风险增加。
2021年ACS合并肾功能不全患者的抗血小板治疗(全文)

2021年ACS合并肾功能不全患者的抗血小板治疗(全文)急性冠脉综合征是在冠状动脉粥样硬化不稳定斑块破裂或糜烂的基础上继发血栓形成、冠状动脉痉挛狭窄甚至闭塞,心肌缺血缺氧而产生的一系列临床综合症。
主要包括不稳定型心绞痛和非ST段抬高型心肌梗死,合称为非ST段抬高型急性冠脉综合症(non-ST segment elevation acute coronary syndrome,NSTEACS);急性ST段抬高型心肌梗死(ST segment elevation acute coronary syndrome,STEACS )。
ACS的治疗原则是尽快恢复血流灌注,预防严重不良反应后果,其中抗血小板治疗是必不可少的重要治理措施。
但是,对于伴有肾功能不全患者来说,因为抗血小板药物在体内的药物代谢动力学和药物效应动力学的改变,导致出血风险增加,所以临床上应密切结合患者肾功能情况合理选择药物及其剂量。
本文旨在通过对国内外近期研究进行分析总结ACS合并肾功能不全患者抗血小板治疗策略。
1.流行病学现状2019年一项前瞻性城乡流行病学研究[1]揭示全球疾病死亡新趋势:心血管疾病是最常见的死亡原因,总占比为40%,低收入和中等收入国家分别为43%和41%,而在高收入国家为23%,这与过去二十年高收入国家心血管疾病死亡率数据相比发生了明显下降。
心血管疾病是全球处于35-70岁阶段内成年人死亡的主要原因。
Baber等研究[2]选择了19832例ACS行PCI治疗患者,其中合并慢性肾功不全的患者占28.3%。
Sattar等人做的一项回顾性队列研究[3]观察了160名接受PCI治疗的ACS合并肾功能不全患者,在住院期间三分之一的患者发生肾功能恶化,经常出现不良事件,住院死亡率高达17.5%。
一项研究[4]表明肾功能不全使ACS患者的心血管病风险更大,预后更差,一旦透析患者出现STEMI或NSTEMI,2年死亡率均超过70%。
急性冠脉综合征(ACS)的抗血小板 双联抗血小板 实用总结全

急性冠脉综合征(ACS)的抗血小板双联抗血小板实用总结急性冠脉综合征(ACS):冠脉不稳定斑块破裂或糜烂继发新鲜血栓致急性缺血综合征,包括:STEMI和非ST段抬高型心肌梗死(NSTEMI)、不稳定性心绞痛(UA),NSTEMI与UA合称NSTE-ACS o基本治疗抗血小板、抗缺血。
无论ACS是否血运重建史,接受长期DAPT(双联抗血小板)是获益的。
-:非血运重建ACS者的DAPT(双联抗血小板)建议:(目前尚缺乏ACS患者P2Y12受体抑制剂单独使用临床证据)1 :接受单纯药物治疗者建议DAPT至少12个月。
2 :既往有心梗病史且存在高缺血风险者,若12个月内耐受DAPT 且无出血并发症,可阿司匹林基础上予替格瑞洛60mgbid延长方案,最长36个月。
3 :处于高出血风险(如PREQSE-DAPT>25分或符合ARC-HBR 标准)者至少1个月DAPT o4 :P2Y12受体抑制剂建议用替格瑞洛而非氯毗格雷,除非出血风险大于潜在缺血获益。
因替格瑞洛疗效优于氯叱格雷且不增加主要出血事件。
对于未计划血运重建且无高出血风险可予P2Y12负荷量预治疗。
(注:ACS为急性冠状动脉综合征;DAPT为双联抗血小板治疗;ARC-HBR为学术研究联合会高出血风险工作组)二:ACS者接受PCI术后DAPT的建议:1:PCI术前均阿司匹林150~300mg负荷剂量联合P2Y12受体抑制剂负荷剂量预治疗:P2Y12受体抑制剂首选替格瑞洛(负荷剂量18Omg,维持剂量90mgbid),当替格瑞洛不可及、无法耐受或有禁忌证时,用氯叱格雷(负荷剂量300〜600mg,维持齐(]量75mgqd)o①替格瑞洛与氯叱格雷相比作用更强、起效更快。
PQ术前服用替格瑞洛后1年的MACE(心血管事件)发生率低于氯叱格雷组且主要出血风险无差异。
院前启用替格瑞洛较院内启用降低术后24h和30d 内支架血栓形成发生率。
在排除主动脉夹层/脑出血后,对低危出血风险者尽早予替格瑞洛预治疗。
ACS患者双联抗血小板和抗凝治疗流程图
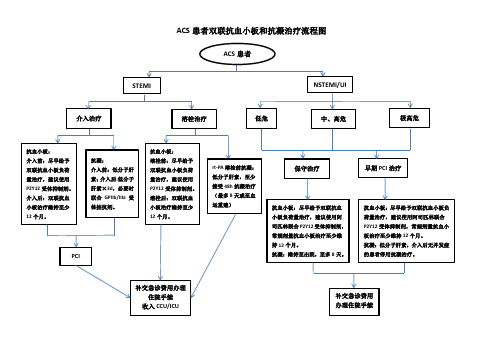
抗血小板: 溶栓前:尽早给予 双联抗血小板负荷 量治疗,建议使用 P2Y12 受体抑制剂。 溶栓后:双联抗血 小板治疗维持至少 12 个月。 rt-PA 溶栓前抗凝: 低分子肝素,至少 接受 48h 抗凝治疗 (最多 8 天或至血 运重建) 抗血小板:尽早给予双联抗血 小板负荷量治疗,建议使用阿 司匹林联合 P2Y12 受体抑制剂, 常规剂量抗血小板治疗至少维 持 12 个月。 抗凝:维持至出院,至多 8 天。 抗血小板:尽早给予双联抗血小板负 荷量治疗,建议使用阿司匹林联合 P2Y12 受体抑制剂,常规剂量抗血小 板治疗至少维持 12 个月。 抗凝:低分子肝素,介入后无并发症 的患者停用抗凝治疗。
ACS 患者双联抗血小板和抗凝治疗流程图
ACS 患者
STEMI
NSTEMI/UI
介入治疗
ห้องสมุดไป่ตู้
溶栓治疗
低危
中、高危
极高危
抗血小板: 介入前:尽早给予 双联抗血小板负荷 量治疗,建议使用 P2Y12 受体抑制剂。 介入后:双联抗血 小板治疗维持至少 12 个月。 抗凝: 介入前:低分子肝 素; 介入后:低分子 肝素×3d,必要时 联合 GPIIb/IIIa 受 体拮抗剂。
保守治疗
早期 PCI 治疗
PCI
补交急诊费用办理 住院手续 收入 CCU/ICU
补交急诊费用 办理住院手续
ACCAHA 指南冠心病患者双联抗血小板治疗

ACC/AHA 指南:冠心病患者双联抗血小板治疗简介冠心病是一种常见的心血管疾病,它导致的心肌缺血和缺氧会引起心肌梗死甚至猝死。
抗血小板治疗是冠心病治疗中重要的一环,可以预防血栓形成和心肌梗死。
双联抗血小板治疗已被广泛应用于冠心病的治疗中,但其使用仍存在一些争议。
双联抗血小板治疗概述双联抗血小板治疗是指同时使用两种抗血小板药物来预防血栓形成和心肌梗死。
常见的双联抗血小板治疗方案包括阿司匹林与氯吡格雷/双嘧达莫。
阿司匹林可抑制血小板聚集和血栓形成,氯吡格雷/双嘧达莫则可通过抑制ADP-受体来减少血小板聚集和血栓形成。
治疗方案的选择使用双联抗血小板治疗方案的患者必须被仔细评估,包括冠心病危险因素、症状、临床情况等。
通常,双联抗血小板治疗适用于下列患者:•对阿司匹林敏感或已经使用阿司匹林但效果不佳的患者;•ACS(急性冠状动脉综合征)的患者,包括无ST段抬高型心肌梗死(NSTEMI)和ST段抬高型心肌梗死(STEMI)的患者;•PCI(经皮冠状动脉介入)手术后的患者。
对于那些存在出血风险或不能耐受抗血小板药物的患者,单用阿司匹林是更合适的治疗方案。
双联抗血小板治疗的副作用双联抗血小板治疗的主要副作用是出血,特别是在手术前。
即使在手术后,双联抗血小板治疗也可能会引起出血,并增加术后并发症的风险。
因此,在进行手术前必须评估患者的出血风险,必要时暂停抗血小板治疗。
双联抗血小板治疗是冠心病治疗中的重要一环,已被广泛应用于临床。
在选择治疗方案时,医生必须仔细评估患者的情况,并权衡治疗的益处和风险。
对于那些不能耐受抗血小板药物或存在出血风险的患者,应该采用单用阿司匹林的治疗方案。
在治疗期间,需要密切监测患者的临床症状和检查结果,以及副作用的发生情况。
缺血性卒中发生acs的抗血小板治疗

综合治疗
除了抗血小板治疗和介入治疗外, 急性冠脉综合征患者还需要接受 综合治疗,包括药物治疗、生活
方式的改变和心血管康复等。
ACS抗血小板治疗的药物选择
01
阿司匹林
阿司匹林是常用的抗血小板药物之一,通过抑制环氧化酶和血栓烷A2
的合成达到抑制血小板活化的作用。
02
氯吡格雷、替格瑞洛
这些药物属于ADP受体拮抗剂,通过抑制ADP与其受体结合,达到抑制
然而,部分患者对抗 血小板治疗存在抵抗 或不良反应,需要个 体化治疗。
在临床实践中,阿司 匹林和氯吡格雷是常 用的抗血小板药物。
抗血小板治疗在缺血性卒中患者中的指南建议
根据相关指南,对于缺血性卒中患者,建议长期使用阿司匹林或氯吡格雷进行抗血 小板治疗。
对于高危患者,可以考虑联合使用阿司匹林和氯吡格雷进行强化抗血小板治疗。
感谢您的观看
THANKS
减少心血管事件
抗血小板治疗也能够减少缺血性卒中患者的心血 管事件,如心肌梗死和脑梗塞等。
安全性评估
在临床实践中,应定期评估抗血小板治疗的安全 性,关注出血等不良反应的发生情况。
04
抗血小板治疗的临床实践与 指南
抗血小板治疗在缺血性卒中患者中的实践现状
抗血小板治疗是预防 缺血性卒中复发和降 低心血管事件风险的 重要手段。
分类
根据病因和发病机制,缺血性卒 中可分为动脉粥样硬化性血栓性 脑梗死、腔隙性脑梗死、脑栓塞 等类型。
缺血性卒中的病理生理机制
01
02
03
动脉粥样硬化
动脉粥样硬化是缺血性卒 中的主要病因,斑块形成 导致血管狭窄或闭塞,影 响脑部供血。
血栓形成
动脉粥样硬化斑块破裂后, 可形成血栓,进一步阻塞 血管,导致脑组织缺血、 坏死。
急性冠状动脉综合征特殊人群抗血小板治疗中国专家建议PPT课件

对于年龄≥75岁的ACS患者,建议在阿司匹林基础上选择氯吡格 雷作为首选的P2Y12抑制剂。用法:75 mg、1次/d,如此次发病 前未用此药,建议予负荷量300 mg。建议DAPT疗程为12个月, 可根据患者缺血与出血风险适当延长或缩短。
3
2.溶栓治疗患者的抗血小板治疗 建议
6
5.卒中/短暂性脑缺血发作(TIA)患者抗 血小板治疗 建议
1.既往有缺血卒中或TIA病史的ACS患者,推荐阿司匹林(100 mg/d)+氯吡格雷(75 mg/d)持续12个月。
2.ACS应用DAPT期间发生颅内出血,应停用DAPT,权衡出血 和再发缺血事件的风险,于病情稳定2~8周后,适时恢复适度的 抗栓治疗,可先启用氯吡格雷治疗,随后继续应用DAPT。
1.STEMI溶栓患者尽早给予双联抗血小板治疗(dual antiplatelet therapy, DAPT):阿司匹林负荷量200~300 mg(嚼 服),随后100 mg/d;≤75岁者给予氯吡格雷300 mg负荷剂量 (>75岁者不予负荷剂量),随后75 mg/d,持续治疗至少12个 月。
7
6.近期消化道出血病史患者的抗血小板治 疗 建议
1.具有高危消化道出血风险的ACS患者(包括老年人、服用华法林、糖 皮质激素或者NSAIDS等),推荐在氯吡格雷和阿司匹林DAPT基础上服 用PPI 1~3个月。
2.既往有消化道出血史及抗血小板治疗过程中发生消化道出血的ACS患 者,应联合应用PPI 3~6个月,其后可考虑继续或间断服用PPI。
2.高出血风险(HAS-BLED评分≥3分)的ACS合并NVAF患者, 不论临床状况(稳定性冠心病或ACS)和置入支架类型(BMS 或新一代DES),应根据缺血风险给予起始NOAC或华法林+氯 吡格雷双联治疗,或NOAC/华法林+阿司匹林+氯吡格雷三联抗 栓治疗持续1个月,再NOAC或华法林+阿司匹林或氯吡格雷双联 抗栓至12个月。
中国急诊急性冠状动脉综合征患者抗血小板治疗的临床实践指南

中国急诊急性冠状动脉综合征患者抗血小板治疗的临床实践指南中国急诊急性冠状动脉综合征(ACS)患者抗血小板治疗的临床实践指南引言:急性冠状动脉综合征是一种严重的心血管疾病,包括不稳定型心绞痛和非ST 段抬高型心肌梗死。
患者在急诊中往往需要紧急处理,其中抗血小板治疗是最重要的一环。
本文基于国内外文献和临床经验,总结了中国急诊急性冠状动脉综合征患者抗血小板治疗的临床实践指南。
一、抗血小板药物的选择:目前,常用的抗血小板药物包括阿司匹林和氯吡格雷。
根据患者具体情况,选择适当的抗血小板药物是十分重要的。
1. 阿司匹林:阿司匹林是急性冠状动脉综合征患者的首选抗血小板药物。
常用剂量为75-100mg/日。
对于对阿司匹林过敏或不能耐受的患者,可选择其他抗血小板药物。
2. 氯吡格雷:氯吡格雷是一个适用于急性冠状动脉综合征患者的另一种常用抗血小板药物。
对于有高风险特点的患者(如存在糖尿病、高龄、多支血管病变)或同时使用支架术的患者,可以考虑联合使用氯吡格雷与阿司匹林,减少心脏相关的不良事件。
二、抗血小板治疗的持续时间:对于急性冠状动脉综合征患者,抗血小板治疗的持续时间也是至关重要的。
根据不同患者的风险评估,抗血小板治疗的持续时间会有所不同。
1. 高危患者:对于高危患者,一般需要至少12个月的双抗血小板治疗,并且要根据患者的临床情况进行密切监测。
治疗的剂量和使用的药物也需要根据患者的情况进行调整。
2. 低危患者:对于低危患者,可以根据具体情况考虑适当缩短抗血小板治疗的持续时间。
但是,一般仍建议至少6个月的抗血小板治疗。
三、抗血小板药物使用策略:除了选择合适的抗血小板药物和确定治疗持续时间之外,还需要制定合适的抗血小板药物使用策略,以确保患者获得最佳的治疗效果。
1. 急诊期间使用抗血小板药物:在急诊期间,患者需要尽早使用阿司匹林,并考虑使用300mg的负荷剂量,以迅速达到治疗效果。
此外,对于有PCI需求的患者,应在术前72小时内使用氯吡格雷,并酌情考虑300mg的负荷剂量。
10ACS患者双抗规范化治疗

急性冠脉综合征(ACS) 应尽早启动抗血小板治疗
• 血小板活化出现在动脉粥样硬化早期 动脉粥样硬化病变过程1
动脉粥样斑块形成期
(无临床症状,血小板已活化)
• 血管内皮损伤,血液高切变应力等因素促发血 小板活化;血小板活化启动动脉粥样硬化斑块 形成2
ACS急性期
(心绞痛、心梗)
• 斑块破裂,血小板粘附、活化、 聚集,血栓形成,导致ACS急性 发作2,3
迟 发 支 架 内 血 栓 形 成
5.6%
1.1%
氯吡格雷治疗12个月组 氯吡格雷治疗18个月组
(n=160)
(n=176)
研究纳入的高风险患者为:合并糖尿病、低射血分数(<45%)、分叉 病变、多支病变、弥散大病变(>20mm)、小血管病变(<2.5mm)
总生存率
月更为显著地预防支架迟发血栓 形成,提高了患者生存率.
0.7*
*p<0.05, BMS vs 12个月DES组 +p<0.05, BMS vs 12和24个月DES组
DES, %
12个月 (n=173)
24个月 (n=274)
2
2
3
3
6
4
2
0.4
0
0
0.6
0.4
0
0
2
0
3
0.4
P值 12 vs 24个月
0.74 0.78 0.35 0.30
0.03 0.02
长期获益
氯吡格雷预处理,实现早期临床获益
氯吡格雷预处理降低院内和30天死亡风险
30天联合终点*1
RRR= 30%
P=0.03
院内死亡**2
RRR= 40%
ACS非血运重建患者的抗血小板治疗

长期抗血小板治疗需要定期监测和调整药物剂量, 以确保治疗效果和安全性。
对临床医生的建议
01
在对ACS非血运重建患者进行治疗时,应优先考虑使用抗血小 板药物。
02
在选择抗血小板药物时,应根据患者的具体情况和医生的经验
进行个体化治疗。
对临床实践的指导意义
根据最新研究结果,临床医生应为ACS非血运重建患者选择联合抗血小板 治疗方案,以提高治疗效果。
对于特殊人群,如高龄、肾功能不全等,需谨慎评估抗血小板治疗的获益 与风险,制定个体化治疗方案。
关注新型抗血小板药物的研发进展,以便及时将最新治疗策略应用于临床 实践。
05
ACS非血运重建患者抗血小板治疗的
研究结果与结论
大部分临床研究结果显示,对于ACS非血运重 建患者,联合抗血小板治疗相比单一药物治疗 能够显著降低心血管事件的发生率。
新型抗血小板药物在减少心血管事件方面显示 出优于传统药物的潜力,但仍需进一步研究证 实其长期疗效和安全性。
针对不同患者的个体差异,选择合适的抗血小 板治疗方案对治疗效果至关重要。
早期研究
早期的研究主要关注单一抗血小 板药物在ACS非血运重建患者中 的疗效,如阿司匹林和氯吡格雷。
联合治疗研究
随着研究的深入,研究者开始探 索联合抗血小板治疗的疗效,如 阿司匹林联合氯吡格雷、阿司匹 林联合替格瑞洛等。
新型药物研究
近年来,新型抗血小板药物如普 拉格雷和替卡格雷在ACS非血运 重建患者中的研究也取得了进展。
02
ACS非血运重建患者的抗血小板治疗
的重要性
抗血小板治疗的作用
防止血小板聚集
冠状动脉介入术后双联抗血小板治疗的最佳疗程

冠状动脉介入术后双联抗血小板治疗的最佳疗程刘培光;周智宏【摘要】Dual antiplatelet therapy (DAPT) has become routine after percutaneous coronary intervention (PCI) for at least 12 months recommended by guidelines , however, more clinical trials have suggested that there were no significant differences in duration of DAPT between six-month and 24-month. Related literatures were reviewed in this article on exploring optimal duration of DAPT after PCI and suggestions on how to identify optimal duration were also presented in individual patients .%冠状动脉介入治疗后进行双联抗血小板治疗已经成为临床治疗的常规,指南推荐至少使用12个月,然而,近年来越来越多的临床试验表明6个月和24个月的疗程对临床后果无明显影响,现通过复习文献对双联抗血小板治疗的最佳疗程做一介绍,并提出如何确定最佳的治疗疗程.【期刊名称】《心血管病学进展》【年(卷),期】2013(034)003【总页数】4页(P404-407)【关键词】双联抗血小板治疗;冠心病;经皮冠状动脉介入治疗;出血;支架内血栓形成【作者】刘培光;周智宏【作者单位】河北联合大学附属医院心内科;感染性疾病科,河北,唐山,063000【正文语种】中文【中图分类】R815;R331.1+43经皮冠状动脉介入治疗(PCI)是当前治疗冠心病最主要的方法之一,在PCI后需要长期服用包括抗血小板药物治疗在内的针对冠心病二级预防的多种药物治疗。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Censored Median Survival (95% CL)
STEMI
1403
22% (313) 78% (1090) NA
(3569 NA)
Non-STEMI+UA
2020
26% (521) 74% (1499) NA
(3611 NA)
GRACE研究,即全球急性冠脉事件登记研究,是世界上首个于多个国家进行的针 对所有类型、未经筛选ACS患者的前瞻性观察研究。研究于1999年4月启动,迄今 全球共有30个国家、247家医院参与,入选ACS患者102341例。
ST:支架内血栓;MACE:主要心血管事件
尽管BMS在1个月时可观察到支撑 物周围炎症,但是到3和8个月时, 可见血管完全愈合,并形成新内 膜。而Taxus支架则表现为早期纤 维蛋白沉积在支架周围( ),并持 续8个月,是延迟愈合的标志。相 反,Cypher支架则显示早期(1和3 月)有大量的炎症细胞浸润,包括 巨细胞形成( ),而纤维蛋白沉积 在8月时更为明显( )。
GRACE研究5年随访结果证实:UA/NSTEMI与STEMI患者具有同样高的 长期死亡风险(P=0.21)。
1
STEMI
0.8
Non-STEMI + UA
0.6
0.4
0.2
HR (95% CI): 1.026 (0.89, 1.18)
0
0
1000
2000
随访时间(天)
3000
No. of SubjectsEvents
目录
1 非血运重建者双抗治疗必要性
2
PCI患者双抗治疗必要性
3
ACS治疗现状及原因解析
4
患者依从性不佳的探讨
ARC 对支架血栓的定义
1个月
1年
早期血栓 ≤ 1 个月
1个月< 晚期血栓 ≤ 1年
超晚期血栓 > 1年
急性 ≤1天
亚急性 >1天 - ≤1个月
0天 >1天 >1个月
到1天 到1个月 到1年 >1年
4000
Fox KA, Carruthers KF, Dunbar DR, et al. Eur Heart J. 2010;31(22):2755-64.
非血运重建ACS患者院内死亡风险更高
三组中p均小于0.001
CRUSADE研究在2001年7月至2006年12月共随访了美国400多家大型急救中心的 超过200000例NSTEMI患者和后期的8800余例STEMI患者,按照调整的PURSUIT 危险评分模型以三分法分为低、中、高三个危险级别进行早期介入策略对临床结局 的评估,院内死亡率是其主要的结局指标。结果发现无论何种危险等级患者,非介 入治疗患者院内死亡率均显著高于接受介入治疗患者。 Bhatt DL, et al. JAMA. 2004;292(17):2096-2104. 400.2015.016.023
非血运重建治疗 的ACS患者
高龄(>75岁) 不稳定心绞痛(冠脉狭窄程度 <50%3) 伴合并症(CKD、糖尿病、 心衰等) 多支血管弥漫性病变 造影剂过敏 经济条件不佳 其他
病情稳定 后出院疗
门诊
*血运重建治疗:包括PCI、CABG和溶栓治疗
1. Steinberg BA, et al. Am J Cardiol. 2007; 99: 1212-1215. 2. 2009年《急性冠状动脉综合征非血运重建患者的抗血小板治疗中国专家共识》 3. 2011年美国不稳定型心绞痛和非ST段抬高心肌梗死治疗指南
ACS双联抗血小板治疗的必要性 及特殊情况下抗血小板治疗的处理原则
目录
1 非血运重建者双抗治疗必要性
2
PCI患者双抗治疗必要性
3
ACS治疗现状及原因解析
4
患者依从性不佳的探讨
GRACE研究中国亚组分析提示: 非血运重建治疗的ACS患者比例超过50%
胸痛、 胸闷发作
确诊 ACS
血运重建治疗* 的ACS患者
病人因素:糖尿病、急性冠状动脉综合征、肾功能衰竭、左室射血 分数降低、30天内发生MACE、心肌梗死、对支架药物过敏、抗血 小板药物抵抗
损伤因素:C型病变、分叉、钙化、多支、完全闭塞、小血管及其 病变、桥血管病变
技术因素:置入支架后血流缓慢、支架未充分扩张、残余夹层、采 用Crush技术
临床实践中接受非血运重建治疗的 ACS患者主要有三大类
尚缺乏大规模临床 试验研究,因此指 南证据不充分的高 龄或合并多种高危 疾病的ACS患者
临床实践中未能遵 循指南进行血运重
建的患者
遵循指南采用非血 运重建治疗的患者
这两部分人群更加值得关注
生存率
ACS患者存在长期高死亡风险 UA/NSTEMI与STEMI长期死亡率相当
Lüscher TF, et al. Circulation. 2007;115(8):1051-8. 300.2015.004.012
延迟再内皮化是晚期ST的基础病生理变化
DES
3种支架置入后1~8个月动脉愈合过程
1个月
3个月
8个月
BMS
Taxus
Cypher
支架周围纤维蛋白沉积
炎细胞浸润(包括巨细胞形成)
抑制再内皮化
抑制EPC 归巢/增生
TF诱导
西罗莫司 紫杉醇
抑制内膜新生
西罗莫司和紫杉醇通过抑制血管平滑肌迁移和增殖减少新生内膜形成(绿色箭头)。但是,该药物 也抑制内皮化,从而导致动脉愈合延迟,同时诱导组织因子(TF)表达,并可防止内皮祖细胞归巢 和增殖(红色箭头),这些因素都将为支架内血栓形成创造潜在环境 EPC:内皮祖细胞;TF:组织因子
ST:支架内血栓
Lüscher TF, et al. Circulation. 2007;115(8):1051-8. 300.2015.004.012
晚期及超晚期支架内血栓(ST)形成 的危险因素
急性和亚急性ST是ACS患者急诊PCI的最主要危险因素 晚期和超晚期ST的主要危险因素为过早停用抗血小板药物 晚期和超晚期ST的其他预示因素
ARC:美国学术研究联合会
Cutlip DE, et al. Circulation. 2007;115(17):2344-2351. 300.2015.004.008
急性支架血栓 亚急性支架血栓 晚期支架血栓>1年 超晚期支架血栓
DES减少新生内皮的形成 是增加支架血栓(ST)形成倾向的关键
西罗莫司/紫杉醇洗脱支架置入后对在局部血管壁的作用
