2010版中国药典各类用水标准
2010版《中国药典》纯化水标准及检测项目
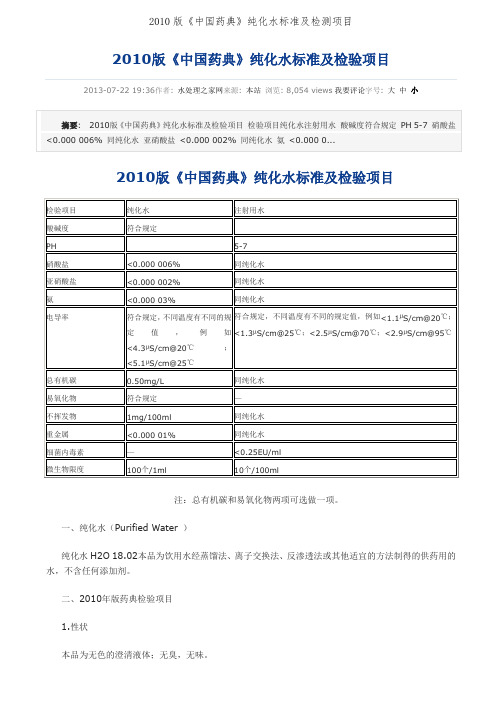
2010版《中国药典》纯化水标准及检验项目2013-07-22 19:36作者: 水处理之家网来源: 本站浏览: 8,054 views我要评论字号: 大中小注:总有机碳和易氧化物两项可选做一项。
一、纯化水(Purified Water )纯化水H2O 18.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的供药用的水,不含任何添加剂。
二、2010年版药典检验项目1.性状本品为无色的澄清液体;无臭,无味。
取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
3.硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000 006%)。
4.亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml及盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO2))0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(.0000 02%)。
5.氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.000 03%)。
中国药典中药水分通则

中国药典中药水分通则
中国药典中药水分通则是指在中药的质量标准中,对于水分含量进行规定和要求的规则和原则。
它的主要目的是为了保证中药的质量和有效性,并指导相关的生产、质检和使用工作。
根据中国药典中药水分通则的规定,中药的水分含量一般应符合以下要求:
1. 水分含量限制:中药一般应保持一定的水分含量,既不能过高也不能过低。
具体的水分含量限制是根据中药的性质、保存方式和用途等因素来确定的。
2. 检测方法:中国药典中药水分通则还规定了水分含量的检测方法和评估标准。
其中包括常见的干燥法、紫外分光光度法、气相色谱法等多种方法,以确保水分含量的准确测定。
3. 控制方法:为了保持中药的水分含量在合理范围内,中国药典中药水分通则还提出了一些控制方法和要求。
例如,在中药的生产、贮存和运输过程中要严格控制湿度、温度等环境条件,以防止水分的过多或过少。
总之,中国药典中药水分通则是为了规范中药的生产和使用而制定的一系列规定和原则。
它的实施有助于确保中药的质量和安全性,提高中药的疗效和治疗效果。
制药用水有哪些分类和水质标准

制药用水分类和水质标准:制药用水(加工用水:药品制造过程中使用的水,如饮用水,纯净水和注射用水)分类1.饮用水:自来水或深井水,通常由自来水公司提供,也称为原水,其水质必须符合国家标准GB5749-85“饮用水卫生标准”。
有。
根据《2010年中国药典》,饮用水不能直接用于制备或测试。
2.纯化水(Purified Water):制药用水,由原水通过蒸馏,离子交换,反渗透或任何其他合适的方法制成,无任何添加剂。
纯化水可用作制备普通药物制剂的溶剂或测试水。
它不能用于准备注射剂。
通过非热处理(例如离子交换,反渗透和超滤)制备的纯净水通常也称为去离子水。
通过使用特殊设计的蒸馏器蒸馏制备的纯净水通常称为蒸馏水。
3. 注射用水:通过将水纯化为原水,再用专门设计的蒸馏水蒸馏,冷凝和冷却后通过膜过滤得到的水。
注射用水可以用作注射溶剂。
4. 无菌注射用水:根据注射液的生产工艺准备注射用水。
注射用无菌水是用于粉末消毒的溶剂或稀释剂。
制药用水的水质标准:1.饮用水:应符合中华人民共和国国家标准《生活饮用水卫生标准》(GB5749-85)2.纯化水:应符合《2010中国药典》所收载的纯化水标准。
在制水工艺中通常采用在线检测纯化水的电阻率值的大小,来反映水中各种离子的浓度。
制药行业的纯化水的电阻率通常应≥0.5MΩ.CM/25℃,对于注射剂、滴眼液容器冲洗用的纯化水的电阻率应≥1MΩ.CM/25℃。
3.注射用水:应符合2010中国药典所收载的注射用水标准二:2010年中国药典对纯水、注射用水、灭菌注射用水的pH、电导率、总有机碳(TOC)的检测提出如下要求:1. 药典对pH检测的新要求:pH值应处在5.0~7.0。
2.药典对电导率检测的新要求:调节待测样品的温度至25℃。
标示装量为10ml或10ml以下时,电导率限度为25μS/cm;标示装量为10ml以上时,电导率限度为5μS/cm。
测定的电导率值不大于限度值,则判为符合规定;如电导率值大于限度值,则判为不符合规定。
中国药典纯化水制药用水标准

中国药典纯化水(制药用水)标准本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【总有机碳】不得过0.50mg/L。
【易氧化物】取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
以上总有机碳和易氧化物两项可选做一项。
【重金属】取本品100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液(pH3.5)2ml与水适量使成25ml,加硫代乙酰胺试液2ml,摇匀,放置2分钟,与标准铅溶液1.0ml加水19ml用同一方法处理后的颜色比较,不得更深(0.000 01%)。
【电导率】应符合规定(附录)【铝盐】(供透析液生产用水需检查)取本品400ml,置分液漏斗中,加醋酸盐缓冲液(pH 6.0)10ml和水100ml ,用0.5% 8-羟基喹啉三氯甲烷溶液提取3次(20ml,20ml,10ml),合并三氯甲烷提取液于50ml量瓶中,加三氯甲烷至刻度,摇匀,即得供试品溶液;另取标准铝盐溶液[称取硫酸铝钾0.352g,置100ml量瓶中,加1mol/L硫酸溶液10ml溶解后,用水稀释至刻度,摇匀,作为贮备液。
临用前,精密量取贮备液1ml,置100ml量瓶中,用水稀释至刻度,摇匀,即得(每1ml相当于2μg的Al)]2.0ml,置分液漏斗中,加醋酸盐缓冲液(pH 6.0)10ml和水98ml,同法操作,即得标准溶液;取醋酸盐缓冲液(pH 6.0)10ml和水100ml,置分液漏斗中,同法操作,作为空白溶液。
取上述溶液,照荧光分析法(附录ⅣE),在激发光波长392nm与发射光波长518nm处分别测定荧光强度。
供试品溶液的荧光强度不得大于标准溶液的荧光强度(0.000 001%)。
2010版药品GMP指南水系统

水系统1、概述水在制药工业中是应用最广泛的工艺原料,用做药品的成份、溶剂、稀释剂等。
制药用水作为制药原料,各国药典定义了不同质量标准和使用用途的工艺用水,并要求定期检测。
水极易滋生微生物并助其生长,微生物指标是其最重要的质量指标,在水系统设计,安装,验证,运行和维护中需采取各种措施抑制其生长。
水是良好的溶剂、尤其是与自然界失去平衡的纯化水和注射用水,具有极强的溶解能力和极少的杂质,广泛用于制药设备和系统的清洗。
鉴于水在制药工业中的既作为原料又作为清洗剂,各国药典对制药用水的质量标准,用途都有明确的定义和要求;各个国家和组织的GMP将制药用水的生产和储存分配系统视为制药生产的关键系统,对其设计,安装,验证,运行和维护等提出明确要求。
在指南第二章将具体介绍我国和其他国家药典和GMP对制药用水的要求。
我国幅员辽阔,各地水质不同,季节的变化也会导致水质的巨大变化,我国制药企业使用的最初原料水未必常年符合饮用水的标准要求,需将其依次处理成饮用水,纯化水,注射用水等制药用水,适合不同的工艺需求。
在指南第三章中将介绍制药用水处理的各种技术,工艺和设备。
制药生产中其它原料、辅料、包装材料是按批检验和释放的,而作为原料的制药用水(饮用水,纯化水或注射用水)通常是通过管道连续流出的,随时取用的,其微生物属性等质量指标通常无法连续地实时检测到。
通常是先使用到产品中,若干天后才能知道其微生物指标是否合格,为保证制药用水系统生产出的水在任何时候是好的,即水系统生产质量的稳定性和一致性是各国药品监管部门和制药企业共同关注的重大问题。
各国GMP对水系统的设计和验证有严格要求,第四章将介绍水系统的设计和验证。
在水系统的设计、验证和运行过程中,制药企业、药监部门都遇到各种各样的疑问、问题和争议,我们参照国际组织尤其是ISPE(国际制药工程协会)的指南和工程实践,在第五章对常见问题进行了讨论。
第六章介绍一些关于水的化学和微生物知识以及水系统的钝化技术。
水 分 测 定 法(中国药典2010第一部)

水分测定法测定用的供试品,一般先破碎成直径不超过3mm的颗粒或碎片;直径和长度在3mm以下的可不破碎;减压干燥法需通过二号筛。
第一法(烘干法)本法适用于不含或少含挥发性成分的药品。
测定法取供试品2 ~ 5 g , 平铺于干燥至恒重的扁形称量瓶中,厚度不超过5mm,疏松供试品不超过l0mm,精密称定,打开瓶盖在100~105t干燥5小时,将瓶盖盖好,移置干燥器中,冷却30分钟,精密称定,再在上述温度干燥1小时,冷却,称重,至连续两次称重的差异不超过5mg为止。
根据减失的重量,计算供试品中含水量(%)。
第二法(甲苯法)本法适用于含挥发性成分的药品。
仪器装置如图。
A为5 0 0 m l的短颈圆底烧瓶;B为水分测定管;C为直形冷凝管,外管长40cm。
使用前,全部仪器应清洁,并置烘箱中烘干。
图甲苯法仪器装置测定法取供试品适量(约相当于含水量l~4ml),精密称定,置A瓶中,加甲苯约200ml,必要时加人干燥、洁净的沸石或玻璃珠数粒,将仪器各部分连接,自冷凝管顶端加人甲苯,至充满B管的狭细部分。
将A瓶置电热套中或用其他适宜方法缓缓加热,待甲苯开始沸腾时,调节温度,使每秒钟馏出2滴。
待水分完全馏出,即测定管刻度部分的水量不再增加时,将冷凝管内部先用甲苯冲洗,再用饱蘸甲苯的长刷或其他适宜的方法,将管壁上附着的甲苯推下,继续蒸馏5分钟,放冷至室温,拆卸装置,如有水黏附在B管的管壁上,可用蘸甲苯的铜丝推下,放置,使水分与甲苯完全分离(可加亚甲蓝粉末少量,使水染成蓝色,以便分离观察)。
检读水量,并计算供试品中的含水量(%)。
【附注】用化学纯甲苯直接测定,必要时甲苯可先加水少量,充分振摇后放置,将水层分离弃去,经蒸馏后使用。
第三法(减压干燥法)本法适用于含有挥发性成分的贵重药品。
减压干燥器取直径12cm左右的培养皿,加入五氧化二磷干燥剂适量,使铺成0. 5~lcm的厚度,放人直径30cm的减压干燥器中。
测定法取供试品2~4g,混合均匀,分取约0. 5~lg,置已在供试品同样条件下干燥并称重的称量瓶中,精密称定,打开瓶盖,放人上述减压干燥器中,减压至 2. 67kPa(20mmHg)以下持续半小时,室温放置24小时。
中国药典制药用水要求详解

中国药典制药用水要求详解中国药典中对GMP制药用水的要求非常严格,主要包括以下方面的要求:源水质量、处理系统、水质监控和操作规范等。
下面将对这些要求进行详解。
首先,源水质量的要求。
制药用水的源水必须符合国家相关标准的要求,例如GB3838《地表水环境质量标准》和GB5749《生活饮用水卫生标准》等。
源水的硬度、总溶解固体、细菌等指标必须控制在一定范围内,以保证经过处理后的水质符合GMP规定的标准。
其次,处理系统的要求。
制药用水的处理系统应该使用适当的工艺和设备,确保水质符合GMP标准。
处理设备必须符合相关国家标准,并定期进行维护和保养,以保证其正常运行和稳定性。
处理系统应该包括预处理、反渗透(RO)或电离(DI)等水质处理工艺,以去除源水中的悬浮物、杂质和离子等。
同时,处理系统还应设有适当的消毒装置,以保证制药用水在输送过程中不会被污染。
第三,水质监控的要求。
制药用水的质量必须经过严格的监控和检测。
监控方案应包括源水和处理水的定期监测,以及系统设备运行参数的实时监控。
监控指标包括水质指标(如溶解氧、电导率、总溶解固体、细菌总数等)、温度、流量等。
同时,制药用水应进行定期的微生物监测,确保不会存在细菌、霉菌和其他微生物的污染。
最后,操作规范的要求。
制药用水的生产和使用过程应该符合相关的操作规范,包括工艺和设备的操作规范、生产记录的填写要求、设施和设备的清洁消毒规范等。
制药用水的输送和储存设施应有专门的管理和维护人员,负责设施、设备的日常维护和保养,以及水质监控和检查等工作。
总之,中国药典对GMP制药用水的要求非常严格,主要包括源水质量、处理系统、水质监控和操作规范等方面。
这些要求旨在确保制药用水的质量稳定和安全,保证药品的质量符合相关标准。
制药企业在生产和使用制药用水时,需严格按照中国药典的要求进行操作和管理,以保证药品质量和安全性。
中国药典纯化水制药用水标准

中国药典纯化水(制药用水)标准本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【总有机碳】不得过0.50mg/L。
【易氧化物】取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
以上总有机碳和易氧化物两项可选做一项。
【重金属】取本品100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液(pH3.5)2ml与水适量使成25ml,加硫代乙酰胺试液2ml,摇匀,放置2分钟,与标准铅溶液1.0ml加水19ml用同一方法处理后的颜色比较,不得更深(0.000 01%)。
【电导率】应符合规定(附录)【铝盐】(供透析液生产用水需检查)取本品400ml,置分液漏斗中,加醋酸盐缓冲液(pH 6.0)10ml和水100ml ,用0.5% 8-羟基喹啉三氯甲烷溶液提取3次(20ml,20ml,10ml),合并三氯甲烷提取液于50ml量瓶中,加三氯甲烷至刻度,摇匀,即得供试品溶液;另取标准铝盐溶液[称取硫酸铝钾0.352g,置100ml量瓶中,加1mol/L硫酸溶液10ml溶解后,用水稀释至刻度,摇匀,作为贮备液。
临用前,精密量取贮备液1ml,置100ml量瓶中,用水稀释至刻度,摇匀,即得(每1ml相当于2μg的Al)]2.0ml,置分液漏斗中,加醋酸盐缓冲液(pH 6.0)10ml和水98ml,同法操作,即得标准溶液;取醋酸盐缓冲液(pH 6.0)10ml和水100ml,置分液漏斗中,同法操作,作为空白溶液。
取上述溶液,照荧光分析法(附录ⅣE),在激发光波长392nm与发射光波长518nm处分别测定荧光强度。
供试品溶液的荧光强度不得大于标准溶液的荧光强度(0.000 001%)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
纯化水
Chunhuashui
Purified Water
H2O 18.02 本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄清液体;无臭,无味。
【检查】酸碱度取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释至100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μg NO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000 006%)。
亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐溶液(1→100)1ml及盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释至100ml,再精密量取1ml,加水稀释至50ml,摇匀,即得(每1ml相当于1μgNO2)]0.2ml,加无硝酸盐的水9.8ml,用同一方法处理后的颜色
比较,不得更深(0.000002%)。
氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.0003%)。
电导率应符合规格(附录ⅧS)。
总有机碳不得过0.50mg/L(附录ⅧR)。
易氧化物取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
以上总有机碳和易氧化物两项可选做一项。
不挥发物取本品100ml,置105℃恒重的蒸发皿中,在水浴上蒸干,并在105℃干燥至恒重,遗留残渣不得过1mg。
重金属取本品100ml,加水19ml,蒸发至20ml,放冷,加醋酸盐缓冲液(pH3.5)2ml与水适量使成25ml,加硫代乙酰胺试液2ml,摇匀,放置2分钟,与标准铅溶液1.0ml加水19ml用同一方法处理后的颜色比较,不得更深(0.00001%)。
微生物限度取本品,采用薄膜过滤法处理后,依法检查(附录ⅪJ),细菌、霉菌和酵母菌总数每1ml不得过100个。
【类别】溶剂,稀释剂。
【贮藏】密闭保存。
择自《中华人民共和国药典2010年版二部》
注射用水
Zhusheyong Shui
Water for Injection
本品为纯化水经蒸馏所得的水.
【性状】本品为无色的澄明液体;无臭,无味。
【检查】pH值取本品100ml,加饱和氯化钾溶液0.3ml,依法测定(附录ⅥH),pH值应为5.0~7.0。
氨取本品50ml,照纯化水项下的方法检查,但对照用氯化铵溶液改为1.0ml,应符合规定(0.00002%)。
硝酸盐与亚硝酸盐、电导率、总有机碳、不挥发物与重金属照纯化水项下的方法检查,应符合规定。
细菌内毒素取本品,依法检查(附录ⅪE),每1ml中含内毒素量应小于0.25EU。
微生物限度取本品至少200ml,采用薄膜过滤法处理后,依法检查(附录ⅪJ),细菌、霉菌和酵母菌总数每100ml不得超过10个。
【类别】溶剂。
【贮藏】密闭保存。
择自《中华人民共和国药典2010年版二部》
灭菌注射用水
Miejun Zhusheyong Shui
Sterule Water for Injection
本品为注射用水照注射剂生产工艺制备所得。
【性状】本品为无色的澄明液体;无臭,无味。
【检查】pH值取本品100ml,加饱和氯化钾溶液0.3ml,依法测定(附录ⅥH),pH值应为5.0~7.0。
氯化物、硫酸盐与钙盐取本品,分置三支试管中,每管各50ml,第一管中加硝酸5滴与硝酸银试液1ml,第二管中加氯化钡试液5ml,第三管中加草酸铵试液2ml,均不得发生浑浊。
二氯化碳取本品25ml,置50ml具塞量筒中,加氢氧化钙试液25ml,密塞振摇,放置,1小时内不得发生浑浊。
易氧化物取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
硝酸盐与亚硝酸盐、氨、电导率、不挥发物、重金属与细菌内毒素照注射用水项下的方法检查,应符合规定。
其他应符合注射剂项下有关的各项规定(附录ⅠB)。
【类别】溶剂、冲洗剂。
【规格】(1)1ml(2)2ml(3)3ml(4)5ml(5)10ml(6)20ml (7)50ml(8)500ml(9)1000ml(10)3000ml(冲洗用)【贮藏】密闭保存。
择自《中华人民共和国药典2010年版二部》。
