(教师参考)高中化学 3.1.2 碳及其化合物间的转化课件2 鲁科版必修1
2019-2020年高中化学 3.1.2《碳及其化合物间的转化》教学设计 鲁科版必修1
2019-2020年高中化学 3.1.2《碳及其化合物间的转化》教学设计 鲁科版必修1一、教材分析(一)知识脉络碳及其化合物在自然界中的广泛存在以及在我们的生产、生活中的广泛应用与碳的多样性紧密相关。
本节教材在初中化学知识的基础上,通过介绍、归纳金刚石、石墨、C 60、碳纳米管的物理性质和用途,体现碳单质的多样性;通过探究碳酸钠、碳酸氢钠的化学性质,认识碳酸盐与碳酸氢盐这些含碳化合物的性质及转化关系,体现碳的化合物的多样性;通过介绍自然界和生产、生活中碳及其化合物间的转化,认识碳单质、一氧化碳、二氧化碳、碳酸盐、碳酸氢盐之间的转化,体现碳元素转化的多样性。
(二)知识框架(三)新教材的主要特点:知识更具有时代性和实用性。
通过活动探究的形式使学生获取知识,在关注获取知识结果的同时,也关注获取知识的过程。
更容易实现三维目标的培养。
二、教学目标(一)知识与技能目标1、通过介绍各种碳单质,使学生了解同素异形体的概念,知道碳有三种同素异形体,它们的物理性质有较大的差别,导致物理性质相异的主要原因是碳原子的排列不同。
2、知道含碳元素的化合物种类繁多,一般分为含碳的无机化合物和有机化合物两大类,通过活动探究认识碳酸钠和碳酸氢钠的主要性质,初步体会它们性质的差异。
3、根据生产、生活中的碳元素转化的实例,了解碳单质、一氧化碳、二氧化碳、碳酸盐、碳酸氢盐之间的转化,从而进一步了解它们的性质。
使学生能够解释与含碳化合物有关的现象和解决简单问题,如水垢的形成与消除、木炭燃烧的现象、工业上炼铁的原理等,体会化学在人类生产、生活中的应用,激发学生学习化学的兴趣。
(二)过程与方法目标1、通过探究碳酸钠和碳酸氢钠的主要性质,进一步熟悉研究物质性质的基本程序,培养学生利用实验科学探究的能力。
2、体会将自然界中的转化与实验室中的转化统一起来的科学思维方法。
(三)情感态度与价值观目标1、通过实验探究激发学生探究化学的兴趣,发扬合作学习的精神,养成严谨科学的学习习惯。
高中化学第3章第1节课时2碳及其化合物间的转化课件鲁科必修1鲁科高一必修1化学课件

栏目导航
CO2与NaOH溶液反应(fǎnyìng)用量和产物分析
有关反应:CO2+2NaOH===Na2CO3+H2O ① CO2+NaOH===NaHCO3 ②
12/11/2021
第十九页,共四十九页。
栏目导航
n(CO2) n(NaOH)
<1∶2 =1∶2 12<nn((NCaOO2H))<1
(4)在 Ca(HCO3)2==△===CaCO3↓+CO2↑+H2O 中,碳元素既表
现氧化性又表现还原性。()Fra bibliotek[答案]
12/11/2021
(1)×
(2)×
(3)√ (4)×
第十五页,共四十九页。
栏目导航
2.下列不属于自然界中碳的循环过程的是( ) A.植物光合作用 B.动物的遗体被微生物分解破坏,最终变成二氧化碳等物质 C.空气中的二氧化碳被海水吸收,通过水生生物的贝壳和骨骼 转移到陆地 D.石墨矿的开采利用
12/11/2021
第八页,共四十九页。
栏目导航
(4)过程
写出下列反应的化学方程式:
①CO 的生成: _C_+__O__2_(足__量__)_=_点=_=_燃=_=_C__O_2__、__C_+__C__O_2_=_高=_=_温=_=_2_C__O____;
②铁矿石被还原: _F_e_2_O__3+__3_C__O_=_高=_=_温=__=_2_F_e_+__3_C_O__2 ____。
12/11/2021
第九页,共四十九页。
栏目导航
2.木炭的燃烧
(1)燃烧过程中碳及其化合物的转化关系。
(2)转化过程中的反应方程式。 ①_2_C__+__O_2_(_不__足__)=_点=_=_燃=__=_2_C_O____; ② 2CO+O2=点==燃==2CO2 ; ③ CO2+C=高==温==2CO ; ④ C+O2(充足)=点==燃==CO2 。
高中化学 第3章 第1节 第2课时 碳及其化合物间的转化课件 鲁科版必修1

自然界中 溶洞(róngdòng)的形成
生产 (shēng chǎn) 和生活 中
高炉炼铁
碳三角
水垢形成
第十五页,共21页。
1.要除去CO2气体中混有的CO,常采用的方法 是( D ) A.通过澄清石灰水 B.通过灼热(zhuórè)炭 C.通过水 D.通过灼热(zhuórè)的CuO粉末
第十六页,共21页。
【答案(dá àn)】 6.4g
第二十页,共21页。
克服畏惧、建立自信的方法(fāngfǎ),就 是去做你害怕的事,直到你获得成功的经验。
第二十一页,共21页。
【实验(shíyàn) 探探究究任】务:请根据(gēnjù)提供的试剂和仪器设计一
个简单模拟溶洞形成的实验。 提供试剂(shìjì)和仪器: Ca(OH)2 溶液、稀盐酸、大理石、试管、试管夹、酒精 灯、单孔塞、导管等。
第八页,共21页。
实验(shíyàn) 方案: 澄清石灰水
持续 通入CO2
澄清溶液
化
海洋 动物 岩石
动植物遗体演变
第五页,共21页。
【思考(sīkǎo)与 交流】
如果大气中二氧化碳含量(hánliàng)过多,会对人类
的生存环境造成什么样的影响?
【提示】温室效应
全球气候变暖
第六页,共21页。
溶
溶洞(róngdòng)是怎么形
洞
成的?
奇
所有的地域都能形成溶
观
洞吗?
第七页,共21页。
加热
白色沉淀
第九页,共21页。
实验(shíyàn)
记录:
实验内容 实验现象
澄清石灰水 持续通 入CO2
开始出现白 色沉淀 (chéndiàn), CO2过量时沉 淀(chéndiàn) 溶解
高中化学第3章自然界中的元素3.1.2碳及其化合物间的相互转化课件鲁科版必修1

(3)若 少?
n(CO2 ) =4
n NaOH 7
时,n( CO32 )∶n( HCO3)等于多
Ⅱ.将CO2通入含0.1 mol Ca(OH)2的澄清石灰水中,所得沉 淀质量与通入的CO2的体积的关系如图所示,当溶液中生成 8 g沉淀时,通入的CO2的体积(标准状况)是多少?
答案:Ⅰ.(1) 1 ∶3 (2)(1)n( CO)32= 0.4 mol,n( (3) 3 ∶1 Ⅱ.1.792 L或2.688 L
(4)用醋酸除水垢的离子方程式为
2CH3COOH+CaCO3 === Ca2++2CH3COO-+CO2↑+H2O。( √ ) (5)在Ca(HCO3)2 ==△==CaCO3↓+CO2↑+H2O中,碳元素既表现氧 化性又表现还原=性。( × )
探究三 CO2与碱溶液反应产物的判断与计算
1.CO2与碱反应的原理
C+H2O(g)==高=温=__H_2+_C_O_。
=
二、碳的氧化物
三、碳及其化合物的转化
1.自然界中碳及其化合物的转化 (1)植物通过_光__合__作__用__吸收空气中的_二__氧__化__碳__形成_葡__萄__ _糖__,并释放出_氧__气__,再转化为淀粉。 (2)空气中的_二__氧__化__碳__有很大一部分被海水吸收,溶于水 的_二__氧__化__碳__逐渐转变为_碳__酸__盐__沉积于海底形成新的岩石, 或通过水生生物的贝壳和骨骼转移到陆地。这些_碳__酸__盐__又 与空气中的CO2和水反应生成_可__溶__性__的__碳__酸__氢__盐__。
2.以下气体因与人体中的血红蛋白作用而引起中毒的是( C )
A.Cl2
高中化学鲁科版必修1课件:3.1.2 碳及其化合物间的转化

合物,还合成出许多自然界中并不存在的有机物。
-8-
第2课时 碳及其化合物间 的转化
首页
自主阅读 自主检测
12
自主预习
探究学习
随堂演练
1.下列不属于自然界中碳的循环过程的是( ) A.植物的光合作用 B.动物的遗体被微生物分解破坏,最终变成二氧化碳等物质 C.空气中的二氧化碳被海水吸收,通过水生生物的贝壳和骨骼转 移到陆地 D.石墨矿的开采利用 解析:A、B、C三项都属于碳的循环;石墨矿的开采利用属于人 类生产,不属于自然界中碳的循环。 答案:D
-14-
第2课时 碳及其化合物间 的转化
首页
自主预习
探究学习
随堂演练
探究一
探究二
问题探究 知识点拨 典例引领
CO2 与 NaOH 反应有关量和产物的分析 CO2 与碱反应时产物与二者的相对量有关,当碱足量时生成碳 酸盐,当 CO2 足量时,生成碳酸氢盐。如: CO2 不足时:CO2+2NaOH Na2CO3+H2O ① CO2 足量时:CO2+NaOH NaHCO3 ② (1)当���������(���N(CaOO2H)) ≤ 12时,仅发生反应①,所得产物为 Na2CO3; (2)12 < ���������(���N(CaOO2H))<1 时,发生反应①②,所得产物为 Na2CO3 和 NaHCO3 的混合物; (3)当���������(���N(CaOO2H))≥1 时,仅发生反应②,所得产物为 NaHCO3。 实际求某物质的物质的量时,常根据某元素的守恒关系来求解。
探究学习
随堂演练
自主阅读 自主检测
一二
4.碳在无机物和有机物之间的转化
(1)植物通过光合作用吸收空气中的二氧化碳,形成葡萄糖并释放
高中化学 第3章 第1节 第2课时 碳及其化合物间的转化课件 鲁科版
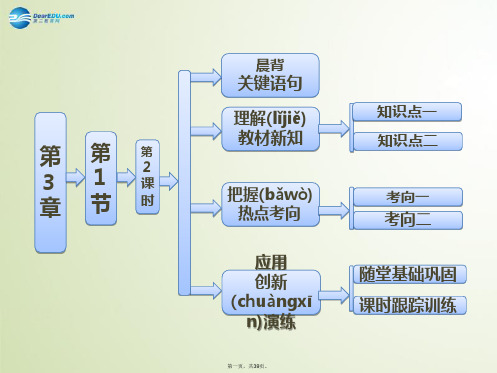
A、B、C、D、E五种物质的转化(zhuǎnhuà)关系如下图 所示,已知A为二元碱,微溶于水且溶解度随温度升高而 降低。
第三十六页,共39页。
(1)写出各物质的化学式: A________,B________,C________,D________, E________。 (2)写出下列两个变化(biànhuà)的离子方程式: B→D:______________________________________。 B→E:______________________________________。
③C+O2=点==燃==CO2;
第十六页,共39页。
3.水垢的形成 (1)成分: CaCO3 、Mg(OH)2。 (2)形成过程的化学反应方程式: ① Ca(HCO3)2==△===CaCO3↓+CO2↑+H2O 。 ②Mg(HCO3)2==△===MgCO3↓+H2O+CO2↑, MgCO3+H2O==△===Mg(OH)2+CO2↑
第十四页,共39页。
[自学教材·填要点(yàodiǎn)]
1.高炉(gāolú)炼铁
第十五页,共39页。
2.木炭(mùtàn)的 燃烧
C、CO、CO2的转化
(zhuǎnhuà)关系为 用化学方程式表示为:① 2C+O2(不足)=点==燃==2CO 。
② 2CO+O2=点==燃==2CO2; 。 ④ C+CO2=高==温==2CO 。
第三十页,共39页。
(1)A、C、E、F的化学式: A_______,C_______,E_______, F_______。 (2)向饱和的C的溶液中通入足量CO2,会出现的现象 是 ______________________________________________, 有关反应的化学方程式为__________________________。 (3)鉴别C与F溶液应选(yīnɡ xuǎn)用的试剂是 ________,有关反应的离子方程式为 _________________________。
高中化学鲁科版必修一 第3章第1节第2课时 碳及其化合物间的转化 课件(27张)

题组二 水垢的形成
3.有一种黑色固体 A 在氧气中充分燃烧生成气体 B。向充有 B 的集气瓶中加入少量澄清石灰水,出现白色沉淀 C,振荡后沉 淀消失得溶液 D。把 D 分成两份,一份中加入稀盐酸,又生成
气体 B,另一份中加入足量 NaOH 溶液又生成 C。 (1)A、 B、 C、 D 的名 称分 别 为 ____炭______、 __二__氧__化__碳__、 __碳__酸__钙____、__碳__酸__氢__钙__。 (2)写出有关反应的化学方程式。 B→C_C__O_2_+__C_a_(_O__H_)_2=__=_=_C_a_C__O_3_↓__+__H__2O_________________。 C→D_C__a_C_O__3+__C__O_2_+__H__2O__=_=_=_C__a_(H__C_O__3_)2________________。 D→B_C__a_(_H_C__O_3_)2_+__2_H__C_l_=_=_=_C__a_C_l_2+__2_C__O_2_↑__+__2_H_2_O_______。
D.可能小于 2.24 L,也可能大于 2.24 L
解析:往 Ca(OH)2 溶液中通入 CO2 气体,可能发生两个反应: CO2 + Ca(OH)2===CaCO3↓ + H2O , CaCO3 + H2O + CO2===Ca(HCO3)2,由题目可知所给 Ca(OH)2 的物质的量 n[Ca(OH)2]=74 7g.·4mgol-1=0.1 mol,理论上最多可制得碳酸钙 10 g,消耗 CO2 2.24 L。而现在只制得碳酸钙 8 g,则可能有两 种情况:一种是 CO2 的量不足,只发生第一个反应,另一种情 况是 CO2 稍过量,一部分 CO2 参与了第二个反应。
③__C_a_(_H__C_O__3)_2_=_=△_==_=__C_a_C_O__3_↓__+__C_O__2↑__+__H__2O____
高中化学鲁科版必修1课件:第3章 第1节 第2课时 碳及其化合物间的转化
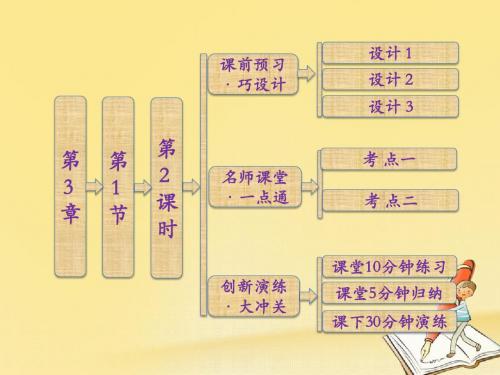
高温 2.反应中:3CO+Fe2O3=====2Fe+3CO2↑。 CO 做________、Fe2O3 被________、Fe 是________ 产物。若 1.6 吨 Fe2O3 参加反应。生成 Fe 的质量为 ________吨,同时产生____________ L 的 CO2 气体 (标况)。
现象分别是
方程式为
有白色沉淀生成 、
无明显现象 ,反应的离子
- 2+ CO2 + Ca ===CaCO3↓ 3 。
(3)写出下列反应的离子方程式:
①NaHCO3溶液与NaOH溶液:
2 HCO3 +OH ===CO3 +H2O 。
- - -
②NaHCO3溶液与稀盐酸:
HCO3 +H ===H2O+CO2↑
- +
。
一、自然界中碳及其化合物间的转化
1.转化示意图
2.溶洞及钟乳石的形成原理(模拟实验)
写出有关反应方程式: 溶洞的形成: CaCO3+CO2+H2O===Ca(HCO3)2 。 △ 钟乳石的形成:Ca(HCO3)2=====CaCO3↓+H2O+CO2↑ 。
二、生产和生活中碳及其化合物间的转化 1.高炉炼铁 (1)原料: 焦炭 和 铁矿石 。 高温 2Fe+3CO ↑ 2 (2)铁矿石被还原:3CO+Fe2O3===== 。
有效减弱“温室效应”。
(4)加热碳酸氢钙溶液会变浑浊,加热碳酸氢钠溶液也 会变浑浊。 (5)钟乳石、石笋是由于CaCO3和Ca(HCO3)2的相互转 化形成的。
分析:CO2气体在水中的溶解度不大,但海洋中的水可溶
解一部分CO2气体,自然界中同时存在产生CO2和消耗
CO2的过程,正常条件下CO2“收支平衡”,自然界中的 CO2就会保持不变,否则就会产生温室效应;Ca(HCO3)2 不稳定,其溶液加热会分解,而NaHCO3固体受热分解, 在溶液中不分解。 答案:(1)(2)(3)(5)
高中化学 3.1.2 碳及其化合物间的转化学案 鲁科版必修1

高中化学 3.1.2 碳及其化合物间的转化学案鲁科版必修1学习目标定位:1.根据生产、生活中的碳元素转化的实例,了解碳单质、一氧化碳、二氧化碳、碳酸盐、碳酸氢盐之间的转化,从而进一步了解它们的性质。
2.能够解释与含碳物质有关的现象和问题,如水垢的形成与消除、木炭燃烧的现象、工业上炼铁的原理等。
知识点一自然界中碳及其化合物间的转化【探究活动】1.自然界中,碳及其化合物间进行着永不停息的转化,这些转化是非常重要的。
观察下图,分析下列问题:(1)二氧化碳有哪些途径进入大气中?(2)水体中的含碳物质是从哪里来的?(3)自然界消耗CO2的过程有哪些?(4)温室效应是怎样产生的?有什么危害?2.碳的化合物在自然界中的转化创造了许多奇迹,请看下面一幅图片。
(1)①溶洞形成的化学方程式为_____________________________________________________________。
②钟乳石、石笋形成的化学方程式为_______________________________________________________。
(2)设计实验模拟溶洞的形成,完成下列表格实验内容实验现象有关化学方程式(或离子方程式)Ca(OH)2(aq)中通入CO2澄清石灰水变浑浊Ca(OH)2+CO2===CaCO3↓+H2O (Ca2++2OH-+CO2===CaCO3↓+H2O)CaCO3浊液中通入足量CO2CaCO3浊液变澄清CaCO3+H2O+CO2===Ca(HCO3)2 (CaCO3+H2O+CO2===Ca2++2HCO-3)将澄清溶液加热澄清溶液变浑浊Ca(HCO3)2=====△CaCO3↓+CO2↑+H2O(Ca2++2HCO-3=====△CaCO3↓+CO2↑+H2O)【学以致用】1.以下属于自然界中碳及其化合物间转化过程的是( )①植物通过光合作用吸收二氧化碳形成葡萄糖②以无机化合物氰酸铵(NH4CNO)为原料合成尿素[CO(NH2)2] ③钟乳石、石笋的形成④石油、天然气等化石燃料的形成A.①②③④ B.只有②③④C.只有①②③ D.只有①③④2.A、B、C、D、E五种物质的转化关系如下图所示。
鲁科版高中化学必修一课件第三章第1节第2课时碳及其化合物间的转化

综合推断
某混合气体中可能含有H2、CO、CO2、HCl、 NH3及水蒸气中的两种或多种。当混合气体依次通过下列 物质时会发生括号中所说明的现象:①澄清的石灰水(无浑 浊现象);②氢氧化钡溶液(有浑浊现象);③浓硫酸(无明显 现象);④灼热的氧化铜(变红);⑤无水硫酸铜(变蓝)。对 该混合气体成分的正确判断是( ) A.一定没有CO2,肯定有CO和H2
解析:解答本题可借用“相似类推法”,以旧知识迁 移应用于题给信息。解题思路为:由碳酸钙、碳酸镁在高 温时分解生成金属氧化物和二氧化碳的事实可推知:碳酸 锌在高温时也分解,生成氧化锌和二氧化碳气体;由碳与 氧化铜在高温时反应生成铜和二氧化碳的事实可推知:碳 在高温时也能将赤铜(Cu2O)中的铜和氧化锌中的锌置换出来, 本身被氧化成二氧化碳。由此可知答案。
变式训练 2.常温下,将一定体积的CO2通入V L NaOH溶液中, 已知NaOH完全反应,若在反应后的溶液中加入足量的澄清 石灰水,得到a g沉淀,若在反应后的溶液中加入足量CaCl2 溶液,得到b g沉淀,则下列说法中正确的是( ) C A.参加反应的CO2体积为0.224a L B.由上述数据不能确定NaOH溶液的物质的量浓度 C.若a=b,则CO2与NaOH溶液反应的产物只有 Na2CO3 D.b可能等于a、小于a或大于a
变式训练 3.按下图示装置持续通人气体X,并在管口P处点燃, 实验结果使澄清石灰水变浑浊,则X、Y可能是( )
A.H2和NaHCO3B.CO和Na2CO3 C.CO和CuO D.H2和Fe2O3
解析:由题意可知,澄清石灰水变浑浊,说 明有CO2生成,并且X气体或X与Y加热后生成的气 体能够燃烧,符合条件的有A、C。 答案:AC
(3)碳酸钙 碳酸氢钙
HC 3)2=====CaCO3↓+CO2↑+H2O Ca(CHO
高中化学鲁科版必修1课件:3.1.2 碳及其化合物间的转化

例1
某固体物质A受热分解,生成B、C、D三种物质。B是一种钾盐,向B
的水溶液中加入澄清石灰水,产生白色沉淀E;E溶于盐酸放出无色无味气 体D;将D通入澄清石灰水中,先出现浑浊现象,然后又变澄清; C在常温 下是一种无色液体。 (1)写出A、B、E的化学式。 A:__________,B:__________,E:________。 (2)写出反应的化学方程式。 ①A受热分解:_____________________________________________; ___________________。
- + ②与过量酸反应:CO2 + 2H ===H2O+CO2↑; 3
2- + - 与少量酸反应: CO 3 +H ===HCO3 , ③ 2- - 与 CO 、 H O 反应: CO + H O + CO ===2HCO 2 2 3 2 2 3 ; 2- - 与碱反应:HCO- + OH ===H O + CO 3 2 3 , ④ △ 受热分解:2NaHCO3===== Na2CO3+H2O+CO2↑;
②将D通入澄清石灰水中,先出现浑浊现象,然后又变澄清:___________;
(3)写出反应的离子方程式。 ①向B的水溶液中加入澄清石灰水,产生白色沉淀E:_______________; ②E溶于盐酸放出无色无味的气体D:_____________________________ _______________________________________。
答案
3.以下属于自然界中碳及其化合物间转化过程的是( B ) ①植物通过光合作用吸收二氧化碳形成葡萄糖 ②以无机化合物氰[(CN)2]与氨水为原料合成尿素[CO(NH2)2] ③钟乳石、石笋的形成 ④石油、天然气等化石燃料的形成 A.①②③④ C.①②③ 解析 的过程。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第1节 碳的多样性 第2课时 碳及其化合物间的转化
精选ppt
1
三、碳及其化合物间的 转化
• 1.自然界中碳及其化合物间的转化
• 2.生产和生活中碳及其化合物间的转化
• 高炉炼铁
• 木炭燃烧
• 水垢的形成
• 无机物和有机物间的转化
•
精选ppt
2
自然界中碳及其化合物间的转化
大气中光合的作二用氧化碳
绿色植物
火山 喷发
呼吸
森林草原 燃烧
光合作用 呼吸排泄
海洋 动物
化石燃料 燃烧
风化溶解
岩石
动植物遗体演变
精选ppt
3ቤተ መጻሕፍቲ ባይዱ
精选ppt
4
溶洞中的 石花、石笋、钟乳
【活动·探究】 模拟“溶洞的形成”
实验方案及实验记录:
实验内容 实验现象 离子方程式
澄清石灰水
持续通入CO2
开始出现白色沉淀 CO2过量时沉淀溶解
(9) (8)
Na2CO3
(12)
(13) NaHCO3
(3)
(4) (5) (7)
(11)
(6)
CO
注:不能重复
CaCO3
(14) (15)
(16) Ca(HCO3)2
精选ppt
9
高温
原理:Fe2O3+3CO==2Fe+3CO2
精选ppt
6
2、木炭燃烧
碳“三角”
C
CO
CO2
精选ppt
7
本节小结
•1、碳单质—同素异形体概 最念常及见的其碳单性质质有:金刚石、石墨、C60
2、 Na2CO3 和NaHCO3
精选ppt
8
1、写出下列反应的化学方程式
(10)
C
(1)
(2) CO2
Ca2+ + 2OH- + CO2 = Ca CO3↓+ H2O
Ca CO3 +CO2+ H2O = Ca2+ + 2 H CO3-
澄清溶液
加热
出现白色沉淀
Ca2+ + 2 H CO3- =△= Ca CO3 ↓ +CO2+ H2O
精选ppt
5
生产和生活中碳及其化合物间的转化
1、工业炼铁
原料:铁矿石、焦炭、 石灰石、空气
